Clear Sky Science · pl
LAM332 pochodzący od CAF wspiera powstawanie i przeżycie CTC poprzez ITGA3 oraz przyczynia się do przerzutów gruczolakoraka przewodowego trzustki
Dlaczego te badania mają znaczenie dla pacjentów
Rak trzustki jest znany z wczesnego i cichego rozprzestrzeniania się, często pozostawiając pacjentom niewiele opcji leczenia w chwili rozpoznania. Badanie to zagłębia się w jeden z najgroźniejszych etapów tego procesu: w to, jak komórki nowotworowe odrywają się od pierwotnego guza, przeżywają we krwi i zagnieżdżają się w narządach takich jak wątroba czy płuca. Odkrywając specyficzną „rozmowę” między komórkami nowotworu a komórkami podporowymi w otoczeniu guza, autorzy wskazują nowe możliwości przewidywania i potencjalnego zablokowania śmiertelnych przerzutów.
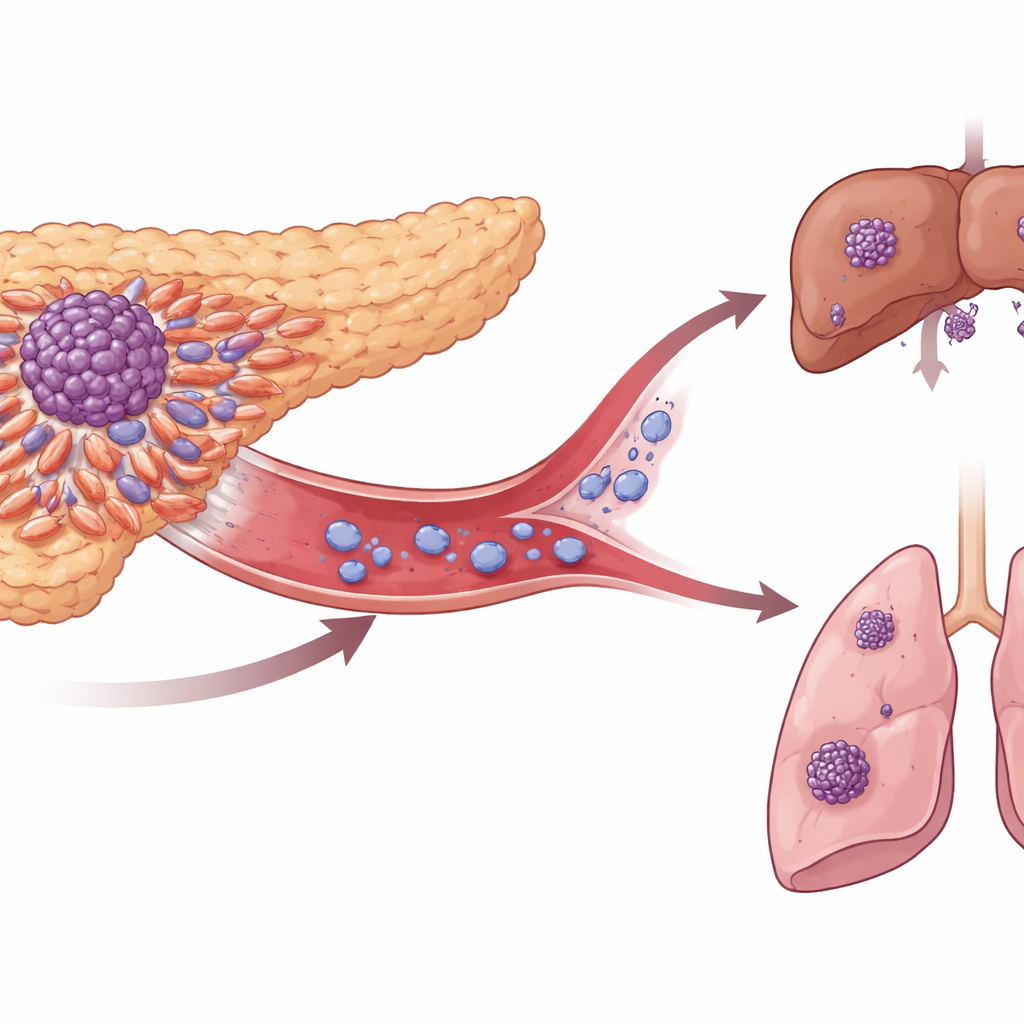
Ukryci podróżnicy we krwi
Gdy guzy trzustki się rozsiewają, robią to za pośrednictwem krążących komórek nowotworowych — zbiegłych komórek, które przedostają się do krwi. Zespół analizował próbki guza oraz obszerne zestawy danych genetycznych i białkowych od pacjentów z i bez takich komórek w naczyniach oraz od osób z chorobą ograniczoną miejscowo versus z przerzutami. Wielokrotnie wyróżniała się jedna cząsteczka powierzchniowa, nazwana ITGA3. Guzy i krążące komórki o wyższym poziomie ITGA3 występowały częściej w zaawansowanych stadiach choroby, szczególnie na inwazyjnej krawędzi guza, gdzie komórki pierwotnie się odrywają. Pacjenci, których guzy miały więcej ITGA3, mieli też zwykle więcej krążących komórek nowotworowych, cechy bardziej agresywne, takie jak naciekanie tkanek i naczyń, oraz krótsze przeżycie.
Jak komórki nowotworu zyskują zdolność odrywania się
Aby zrozumieć, co ITGA3 faktycznie robi, badacze manipulowali jego poziomem w liniach komórkowych raka trzustki i wszczepiali te komórki myszy. Gdy ITGA3 był zmniejszony, komórki nowotworowe rosły wolniej, poruszały się mniej i miały mniejszą zdolność do niszczenia otaczającej tkanki. Komórki przesuwały się również z powrotem w kierunku bardziej uporządkowanego, „epitelialnego” stanu, odzyskując silne połączenia międzykomórkowe i tracąc elastyczne, migrujące cechy ułatwiające ucieczkę. U myszy guzy pozbawione ITGA3 były mniejsze i wykazywały mniej cech inwazyjnych. Wyniki te sugerują, że ITGA3 działa jako kluczowy przełącznik, który pomaga komórkom guza poluzować więzi z masy głównej, przedostać się do naczyń krwionośnych i rozpocząć podróż jako krążące komórki nowotworowe.
Skupianie się razem, żeby przetrwać podróż
Życie we krwi jest brutalne dla pojedynczych komórek nowotworowych, ale klastry komórek wydają się znacznie lepiej przetrwać i zasiedlać przerzuty. Badanie wykazało, że ITGA3 jest szczególnie obfite na komórkach w takich klastrach. W hodowlach laboratoryjnych zaprojektowanych tak, by zapobiegać przywieraniu komórek do plastiku, komórki z prawidłowym poziomem ITGA3 łatwo tworzyły zwarte skupiska i opierały się śmierci komórkowej, podczas gdy komórki z wyłączonym ITGA3 pozostawały przeważnie rozdzielone i łatwiej umierały. W modelach mysich, gdzie guzy rosły w trzustce, utrata ITGA3 prowadziła do mniejszej liczby krążących klastrów, mniej kolonii przerzutowych w wątrobie i płucach oraz niższego ogólnego obciążenia chorobą odległą. Pokazuje to, że ITGA3 nie tylko ułatwia odrywanie się komórek, ale także pomaga im przylegać do siebie i przetrwać w nieprzyjaznych warunkach krążenia.
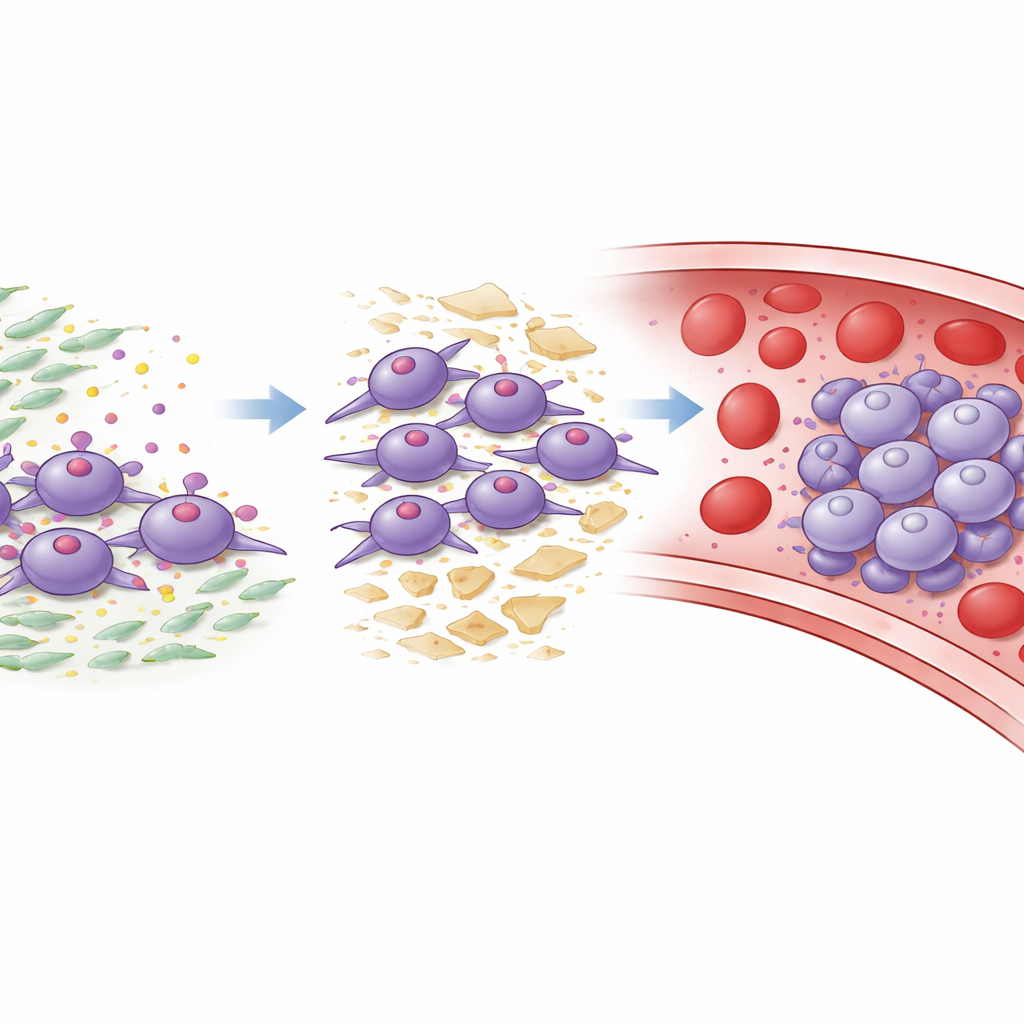
Rola wspierających komórek podścieliska
Guzom trzustki towarzyszy wiele fibroblastów związanych z rakiem, rodzaju komórek podporowych, które budują i przebudowują szkielet tkankowy wokół guza. Autorzy odkryli, że te fibroblasty są głównym źródłem lepkiego białka zwanego lamininą-332. Komórki nowotworowe posiadające ITGA3 wykorzystują je jako punkt zaczepienia dla lamininy-332. W eksperymentach komórkowych i zwierzęcych wiązanie lamininy-332 z ITGA3 wywoływało sygnały wewnątrz komórek nowotworowych, które zwiększały wzrost, ruch, inwazję tkanki oraz przejście w bardziej ruchliwy, agresywny stan. Sprzyjało to także tworzeniu klastrów i zmniejszało śmierć komórek, gdy znajdowały się w zawiesinie, naśladując warunki we krwi. Blokowanie lamininy-332 przeciwciałami lub zakłócanie ITGA3 bądź jego dalszych partnerów sygnałowych w dużej mierze odwracało te złośliwe zachowania i redukowało przerzuty u myszy.
Co to może oznaczać dla przyszłych terapii
Podsumowując, praca opisuje wyraźny łańcuch zdarzeń: fibroblasty w i wokół guzów trzustki uwalniają lamininę-332; to białko przyczepia się do ITGA3 na komórkach nowotworowych; następujący po tym sygnał pomaga komórkom odrywać się, skupiać w ochronne klastry, przetrwać w krążeniu i kolonizować odległe narządy. Dla laika kluczowy komunikat jest taki, że badacze zmapowali konkretną „linię zaopatrzenia”, której guzy używają, by wysyłać i chronić komórki rozsiewające się. Ponieważ ta ścieżka zależy od składników występujących głównie w guzie i jego zrębie, stanowi atrakcyjny cel dla nowych terapii. Leki lub przeciwciała blokujące lamininę-332, ITGA3 lub sygnały przez nie wywoływane mogłyby zmniejszyć liczbę i odporność krążących komórek nowotworowych, potencjalnie spowalniając lub zapobiegając śmiertelnym przerzutom w raku trzustki.
Cytowanie: Tang, H., Shi, W., Tan, S. et al. CAFs-derived LAM332 promotes CTCs formation and survival via ITGA3 and contributes to the metastasis of pancreatic ductal adenocarcinoma. Cell Death Dis 17, 369 (2026). https://doi.org/10.1038/s41419-026-08642-z
Słowa kluczowe: rak trzustki, przerzuty, krążące komórki nowotworowe, mikrośrodowisko guza, fibroblasty związane z nowotworem