Clear Sky Science · pl
Orkiestracja metaboliczna napędzana przez GGCT: przekierowywanie glutaminy do syntezy glutationu przy jednoczesnym wzmacnianiu anaplerozy glukozowej dla proliferacji guza
Dlaczego to ma znaczenie dla leczenia nowotworów
Komórki nowotworowe rosną szybko, a by to robić zużywają ogromne ilości paliwa i muszą nieustannie chronić się przed toksycznymi produktami własnego metabolizmu. To badanie ujawnia, jak mało znany enzym GGCT pomaga guzom wątroby i prostaty sprytnie przekierowywać dwa powszechne składniki odżywcze — glutaminę i glukozę — tak, by jednocześnie napędzać wzrost i kontrolować szkodliwe cząsteczki zwane reaktywnymi formami tlenu. Zrozumienie tego metabolicznego żonglowania może otworzyć nowe sposoby głodzenia guzów lub przeciążenia ich mechanizmów obronnych.
Jak komórki nowotworowe żonglują paliwem i ochroną
Komórki guza silnie polegają na glutaminie, aminokwasie pełniącym podwójną rolę: może być rozkładana, by zasilać główny cykl produkcji energii w komórce, a także dostarczać materiału do syntezy glutationu — silnego antyoksydantu neutralizującego reaktywne formy tlenu. Autorzy najpierw potwierdzili, że poziomy glutaminy są wyższe w guzach wątroby niż w sąsiedniej zdrowej tkance, i że komórki nowotworowe hodowane przy większej dostępności glutaminy dzielą się szybciej zarówno w hodowlach, jak i u myszy. Gdy glutaminy brakuje, komórki zwalniają, spadają kluczowe białka cyklu komórkowego, a guzy u zwierząt kurczą się — częściowo dlatego, że osłabiają się mechanizmy antyoksydacyjne i kumulują się reaktywne formy tlenu.
Przełącznik metaboliczny ukryty na widoku
Analiza próbek pacjentów i dużych baz danych nowotworowych wykazała, że enzym GGCT jest konsekwentnie bardziej obficie obecny w guzach wątroby i prostaty niż w tkankach prawidłowych, a wyższe poziomy GGCT przewidują gorsze wyniki kliniczne. W próbkach nowotworowych i komórkach hodowanych in vitro poziomy GGCT rosną wraz ze stężeniem glutaminy, co sugeruje, że guzy „odczytują” dostępność glutaminy przez to białko. Badacze wyjaśnili łańcuch kontroli: glutamina utrzymuje aktywność czynnika pro‑wzrostowego c‑Myc, który hamuje małe regulatorowe RNA miR‑29b‑3p; gdy miR‑29b‑3p jest niskie, zahamowanie GGCT ustaje i enzym się akumuluje. Przy niedoborze glutaminy ten łańcuch odwraca się — miR‑29b‑3p rośnie, informacyjne RNA GGCT są rozkładane szybciej, a poziom enzymu spada.
Przekierowywanie glutaminy i zwiększanie poboru glukozy
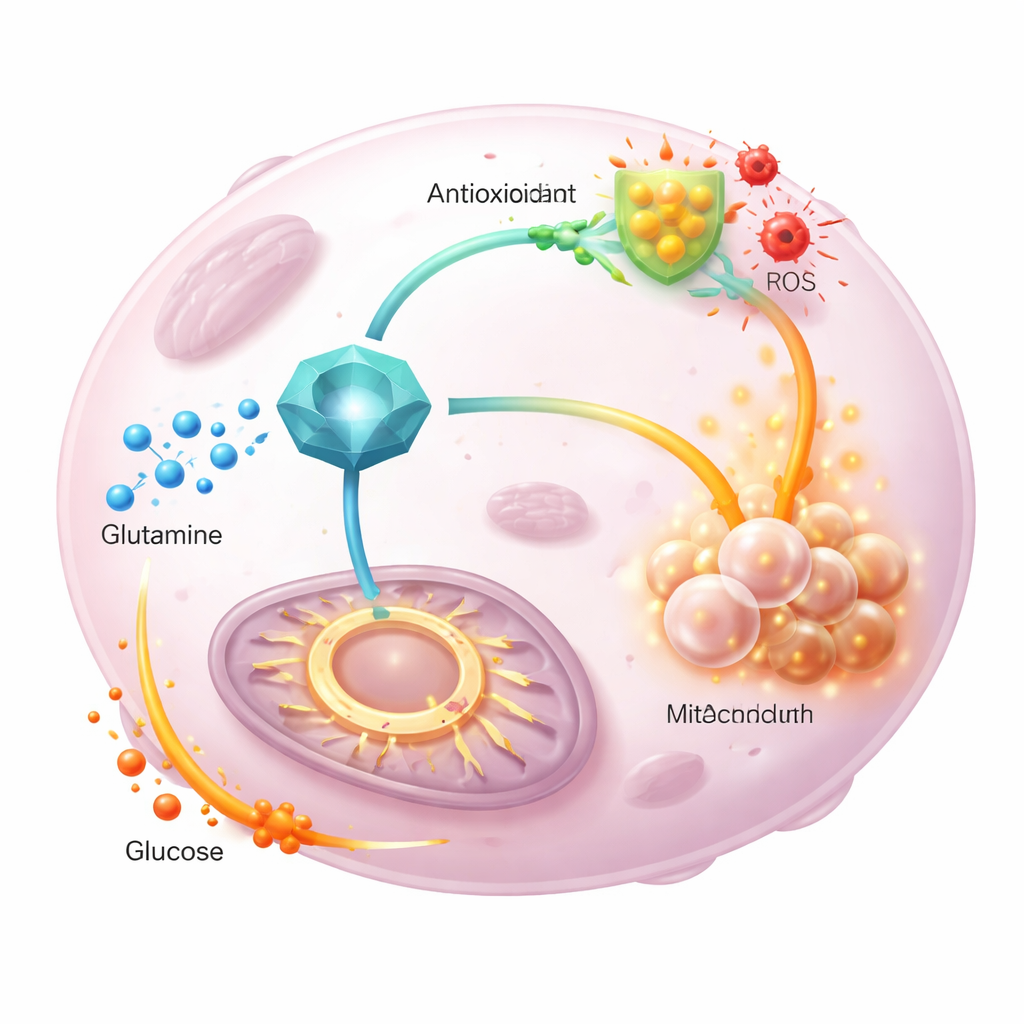
Aby sprawdzić, co GGCT robi wewnątrz komórki, autorzy zmniejszali lub zwiększali jego poziomy i mierzyli zachowanie komórek oraz setki metabolitów. Wyciszenie GGCT zatrzymywało komórki w cyklu podziałowym, zmniejszało ich kolonie i zdecydowanie obniżało poziom glutationu przy jednoczesnym wzroście reaktywnych form tlenu; dodanie chemicznego antyoksydantu częściowo ratowało wzrost. Pod mikroskopem mitochondria stawały się nienormalnie wydłużone i mniej efektywne w zużywaniu tlenu, nawet jeśli komórki próbowały kompensować to zwiększeniem glikolizy, pierwszego etapu rozkładu cukrów. Szczegółowe profilowanie metaboliczne wykazało, że pośrednie produkty centralnego cyklu energetycznego spadały przy utracie GGCT i rosły przy jego nadmiernej ekspresji.
Śledzenie losu atomów węgla
Zespół następnie śledził znakowane atomy glutaminy i glukozy, jak przepływają przez metabolizm guza. Przy nadekspresji GGCT mniej znakowanej glutaminy trafiało do cyklu energetycznego, a więcej było kierowane do nowo syntetyzowanego glutationu, wspierając obronę antyoksydacyjną. Równocześnie znakowana glukoza wnosiła silniejszy wkład do cyklu, rekompensując przekierowaną glutaminę. Mutant GGCT pozbawiony normalnej aktywności enzymatycznej nie potrafił wywołać tych zmian ani promować proliferacji, co dowodzi, że funkcja katalityczna GGCT jest kluczowa. Co ważne, dostarczenie dodatkowego pirogronianu lub zmiana wejścia do cyklu energetycznego przywracały poziomy energii komórkowej, ale nie obniżały reaktywnych form tlenu, wskazując, że GGCT głównie kontroluje równowagę redoks przez glutation, a nie prostymi zmianami podaży energii.
Co to oznacza dla przyszłych terapii
Podsumowując, wyniki stawiają GGCT jako centralnego koordynatora, który pozwala guzom rozdzielać role glutaminy: kieruje większą część tego składnika ku produkcji antyoksydantów, jednocześnie „zasysa” glukozę do cyklu energetycznego, by utrzymać podziały komórkowe. W modelach zwierzęcych wyciszenie GGCT spowalniało wzrost guza, zmniejszało poziom glutationu i zwiększało stres oksydacyjny, a te efekty można było częściowo odwrócić lekiem antyoksydacyjnym. Dla laika przesłanie jest takie, że niektóre nowotwory przetrwają, używając GGCT jako metabolicznej centrali; leki, które wyłączą ten przełącznik, mogłyby jednocześnie osłabić obronę guza przed uszkodzeniami oksydacyjnymi i zaburzyć jego elastyczne wykorzystanie składników odżywczych, zwiększając skuteczność standardowych terapii.
Cytowanie: Yang, L., Sun, H., Wang, R. et al. Metabolic orchestration driven by GGCT: diverting glutamine to glutathione biosynthesis while enhancing glucose anaplerosis for tumor proliferation. Cell Death Dis 17, 358 (2026). https://doi.org/10.1038/s41419-026-08619-y
Słowa kluczowe: metabolizm nowotworu, glutamina, glutation, stres oksydacyjny, enzym GGCT