Clear Sky Science · pl
Adipogenna transdifferencjacja przeprogramowuje komórki PDAC o wysokim poziomie EMT w stan podobny do adipocytów pozbawiony mitozy i ogranicza przerzuty
Przekształcanie agresywnych komórek nowotworowych w nieszkodliwy tłuszcz
Rak trzustki należy do najbardziej śmiertelnych nowotworów, w dużej mierze dlatego, że wcześnie daje przerzuty i opiera się standardowym terapiom. W tym badaniu rozważono zupełnie inne podejście: zamiast próbować truć lub głodzić komórki nowotworowe, co jeśli można by skłonić najbardziej niebezpieczne komórki raka trzustki do przekształcenia w komórki przypominające tłuszcz, które nie dzielą się już i nie rozprzestrzeniają po organizmie? Praca przedstawia, jak badacze wymusili na wysoce agresywnych komórkach raka trzustki przejście w stabilny, adipocytopodobny stan, co spowalniało wzrost guza i zmniejszało rozprzestrzenianie się u myszy, dając nadzieję na nowy sposób kontroli tej wyniszczającej choroby.
Dlaczego raka trzustki tak trudno zatrzymać
Gruczolakorak przewodowy trzustki, główna postać raka trzustki, ma bardzo niekorzystne rokowania: tylko około jedna na osiem osób żyje pięć lat po rozpoznaniu. Część problemu polega na tym, że wiele komórek nowotworowych w tym raku funkcjonuje w przemiennym stanie zwanym EMT, który zwiększa ich ruchliwość, inwazyjność i odporność na leki. Próby zablokowania licznych sygnałów napędzających ten stan przyniosły ograniczone korzyści. Jednocześnie trzustka i jej nowotwory wykazują zaskakującą tendencję do gromadzenia komórek tłuszczowych, co rodzi pytanie, czy tę ukrytą elastyczność tożsamości komórkowej można wykorzystać. Autorzy wysunęli hipotezę, że skoro komórki raka trzustki obfitujące w EMT już są przygotowane do zmiany, można by je przekierować w cichą, adipocytopodobną tożsamość zamiast w inwazyjną.
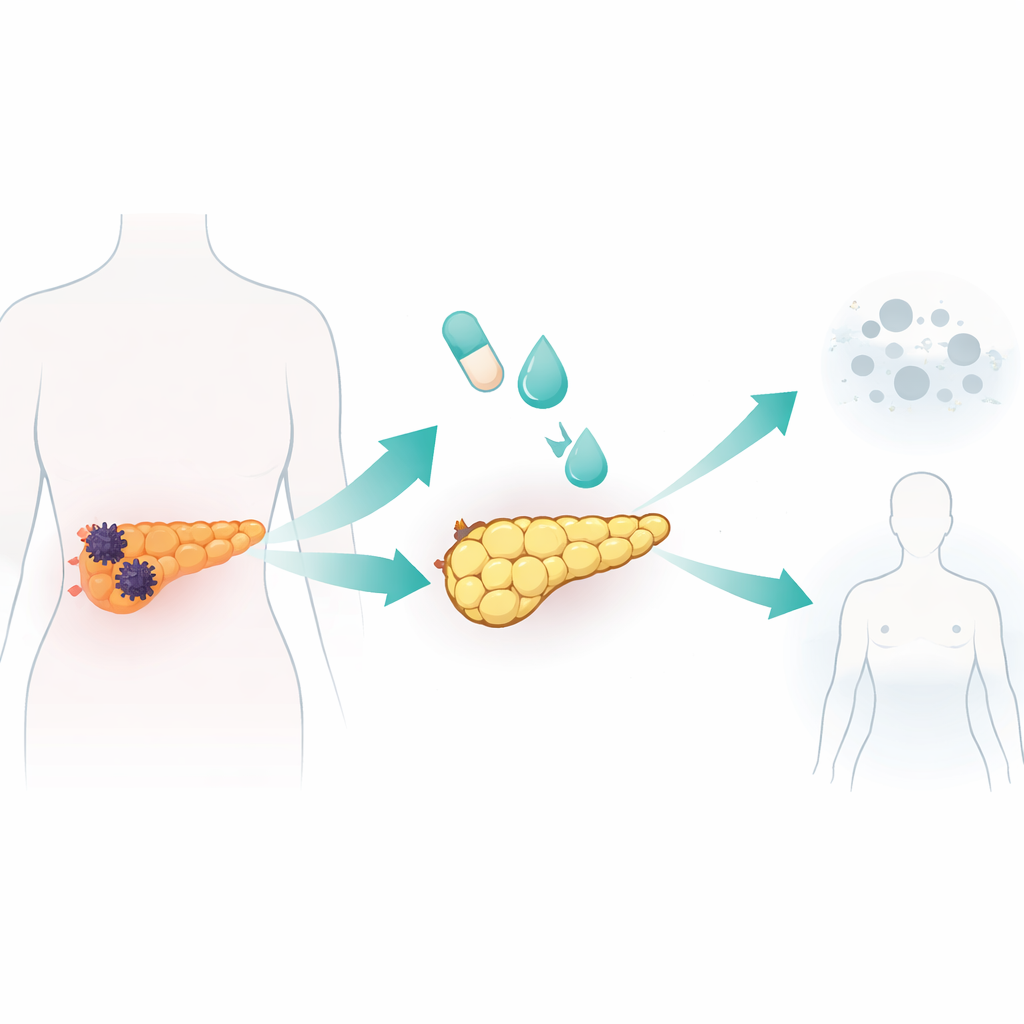
Przeprogramowanie komórek nowotworowych w komórki podobne do tłuszczowych w laboratorium
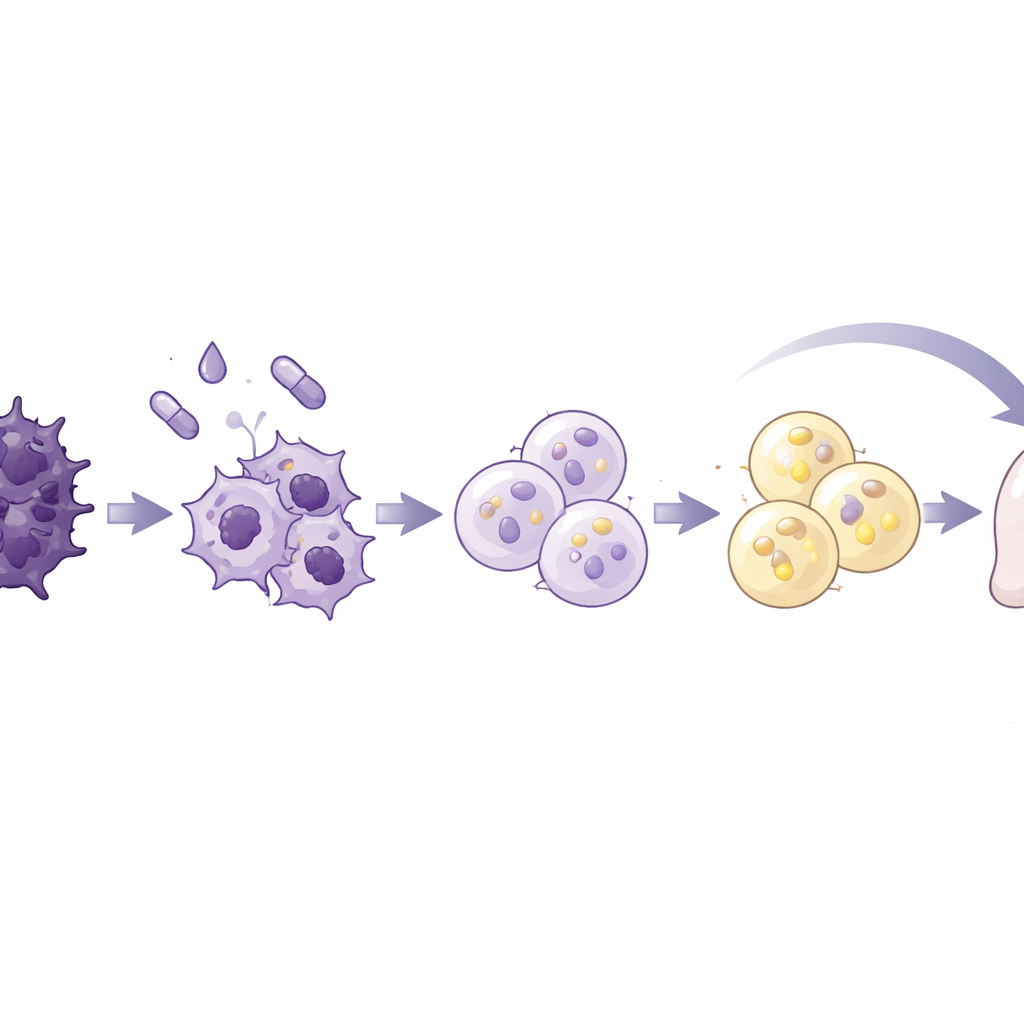
Zespół sprawdził standardowy koktajl indukujący różnicowanie w adipocyty, używany wcześniej w badaniach nad biologią tłuszczu i rakiem piersi, na siedmiu ludzkich liniach komórek raka trzustki oraz jednej linii normalnych komórek trzustkowych. Mieszanka łączyła insulinę i steroid z rozyglitazonem, lekiem aktywującym główny regulator adipogenezy, oraz białko sygnałowe BMP2, mające odblokować plastyczność komórkową. Jedna linia nowotworowa, nazwana AsPC-1, była szczególnie reaktywna. W ciągu dziesięciu dni komórki te stały się większe i bardziej okrągłe oraz wypełniły się kroplami lipidowymi — cechami charakterystycznymi komórek tłuszczowych. Włączyły geny i białka typowe dla dojrzałych adipocytów i wykazały intensywny metabolizm lipidów, w tym wydzielanie adiponektyny i zdolność rozkładu magazynowanych lipidów na żądanie. Co kluczowe, te przekształcone komórki przestały się proliferować, zatrzymały się we wczesnej fazie cyklu komórkowego oraz poruszały się i inwadowały znacznie mniej niż nieleczone komórki nowotworowe.
Wyłączanie programu nowotworowego głęboko wewnątrz komórki
Aby zbadać, co działo się na poziomie molekularnym, badacze przeanalizowali pakowanie DNA i aktywność genów w przekształconych komórkach. Stwierdzili szerokie zacieśnienie chromatyny, kompleksu DNA z białkami kontrolującego dostęp do genów, oraz globalne obniżenie ekspresji genów — obie cechy charakterystyczne dla komórek niedzielących się. Geny wspierające EMT, inwazję i tworzenie przerzutów, w tym enzymy degradujące macierz i kluczowe regulatory EMT, były mocno stłumione, podczas gdy geny związane z adipocytną funkcją zostały wzmocnione. Ogólne sygnatury genowe przesunęły się z mezenchymalnej, wysoce ruchliwej tożsamości w stronę takiej, która blisko przypominała dojrzałe adipocyty. Sygnały związane z wzrostem komórek i odpowiedzią na ważnego promotora EMT, TGF-beta, zostały przyciszone, natomiast szlaki związane z metabolizmem lipidów i adhezją komórkową — wzmocnione. Te zmiany sugerują, że komórki nie zostały jedynie spowolnione, ale zasadniczo przedefiniowane.
Sprawdzenie strategii na myszach
Naukowcy zapytali następnie, czy wymuszone przejście w adipocytopodobny stan może pomóc kontrolować guzy u żywych zwierząt. Implanto-wali ludzkie komórki raka trzustki do trzustki lub śledziony myszy, modelując guzy pierwotne i przerzuty do wątroby. Myszy leczone rozyglitazonem i BMP2 rozwijały mniejsze guzy trzustki i wykazywały bogatsze krople lipidowe oraz markery komórek tłuszczowych w obrębie guzów, wraz z niższym poziomem genów związanych z EMT i inwazją. W modelu przerzutów leczenie nie zmieniło wczesnego zasiewu guzów, ale z czasem spowolniło wzrost obciążenia nowotworowego w wątrobie w porównaniu z zwierzętami nieleczonymi. Co ważne, sąsiednia, normalna tkanka trzustkowa nie wykazywała oczywistej konwersji do komórek tłuszczowych, a adipocytopodobny stan w guzach utrzymywał się przynajmniej przez miesiąc po odstawieniu leków, sugerując pewien stopień trwałości i specyficzności.
Co to może oznaczać dla przyszłej opieki onkologicznej
To badanie wspiera prowokacyjną koncepcję: dla wysoce plastycznych, bogatych w EMT nowotworów trzustki może być możliwe „przekierowanie zamiast zabijania”, skierowanie niebezpiecznych, wędrujących komórek nowotworowych w stabilne, niedzielące się komórki podobne do adipocytów, które mają mniejszą zdolność do dawania przerzutów. Choć są to wczesne prace prowadzone na komórkach i modelach mysich, i nie wszystkie nowotwory trzustki reagują jednakowo, otwierają one nową drogę terapeutyczną działającą przez zmianę tożsamości komórkowej, a nie tylko blokowanie sygnałów wzrostu. W przyszłości takie podejścia transdifferencjacyjne mogłyby być łączone z lekami celowanymi lub immunoterapiami, aby utrzymać raka trzustki w spokojniejszym, łatwiejszym do kontrolowania stanie i zmniejszyć ryzyko śmiertelnych przerzutów.
Cytowanie: Qian, Y., Yan, Z., Wang, J. et al. Adipogenic transdifferentiation reprograms EMT-high PDAC cells into a post-mitotic adipocyte-like state and limits metastasis. Cell Death Dis 17, 330 (2026). https://doi.org/10.1038/s41419-026-08613-4
Słowa kluczowe: rak trzustki, plastyczność komórek, transdifferencjacja, przejście nabłonkowo-mezenchymalne, komórki podobne do adipocytów