Clear Sky Science · pl
Zależność od argininy w przerzutach do sieci tłuszczowej w nabłonkowym raku jajnika ujawnia podatność terapeutyczną
Dlaczego ma to znaczenie dla zdrowia kobiet
Nabłonkowy rak jajnika jest jednym z najbardziej śmiertelnych nowotworów dotykających kobiety, ponieważ zwykle jest wykrywany dopiero po tym, jak cicho rozprzestrzeni się w jamie brzusznej. Ulubionym miejscem osiedlania się tych wędrujących komórek nowotworowych jest fałda tłuszczowa nazywana siecią (omentum). Badanie odsłania ukrytą słabość tych przerzutów do sieci: wykazują one niezwykłe uzależnienie od aminokwasu dietetycznego — argininy. Śledząc, w jaki sposób komórki przerzutowe wykorzystują argininę do naprawy uszkodzonego DNA i przetrwania stresu, badacze wskazują nowe strategie terapeutyczne, które mogłyby zagłodzić przerzuty lub zablokować ich drogi ucieczki.
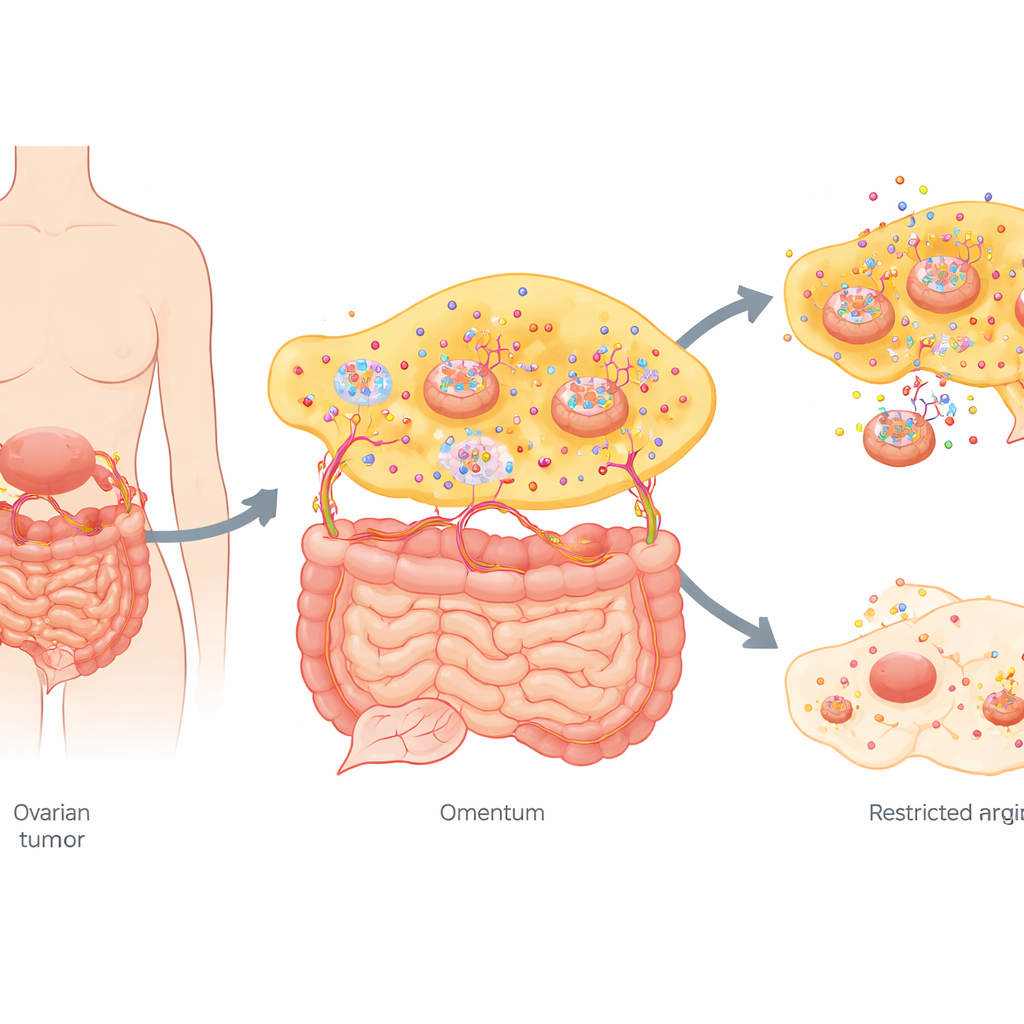
Głodny substancji odżywczych nowotwór w wyjątkowym niszowym środowisku
Guzy jajnika w zaawansowanym stadium często wysiewają maleńkie kolonie w jamie brzusznej, szczególnie w sieci, tkance bogatej w tłuszcz przysłaniającej jelita. Zespół porównał pierwotne guzy jajnika z odpowiadającymi im przerzutami w sieci od kobiet, które nie otrzymały jeszcze leczenia. Szerokie badanie setek małych cząsteczek wykazało, że „odcisk metaboliczny” przerzutów był uderzająco różny. Spośród wielu zmian wyróżniała się jedna: przerzuty w sieci gromadziły znacznie więcej argininy niż pierwotne guzy jajnika. Jednocześnie enzymy niezbędne do syntezy argininy wewnątrz komórki były osłabione, podczas gdy białka transportujące argininę z zewnątrz były nasilone, co wskazuje, że komórki przerzutowe stały się zależne od argininy ze środowiska zewnętrznego.
Głodzenie guzów przez ograniczenie dostaw argininy
Aby sprawdzić, czy to zależenie od argininy ma rzeczywiste znaczenie, badacze użyli modeli mysich raka jajnika. Gdy myszy z guzami zostały umieszczone na diecie pozbawionej argininy, zarówno główne guzy jajnika, jak i rozległe przerzuty w jamie brzusznej wyraźnie się zmniejszyły. Obrazowanie wykazało słabsze sygnały guza, mniej i mniejsze miejsca przerzutowe, mniejszy wysięk w jamie brzusznej oraz lepsze przeżycie w porównaniu z myszami na zwykłej diecie. W hodowlach komórek ludzkie komórki raka jajnika rosły wolniej, mniej migrowały i rzadziej inwadowały, gdy argininy brakowało. Podniesienie poziomu argininy do wartości podobnych lub wyższych niż obserwowane u pacjentek z przerzutami miało efekt przeciwny, przyspieszając wzrost i ruchliwość. Nadekspresja transportera argininy dodatkowo zwiększała te agresywne cechy, podkreślając, że guzy prosperują, gdy argininy jest pod dostatkiem.
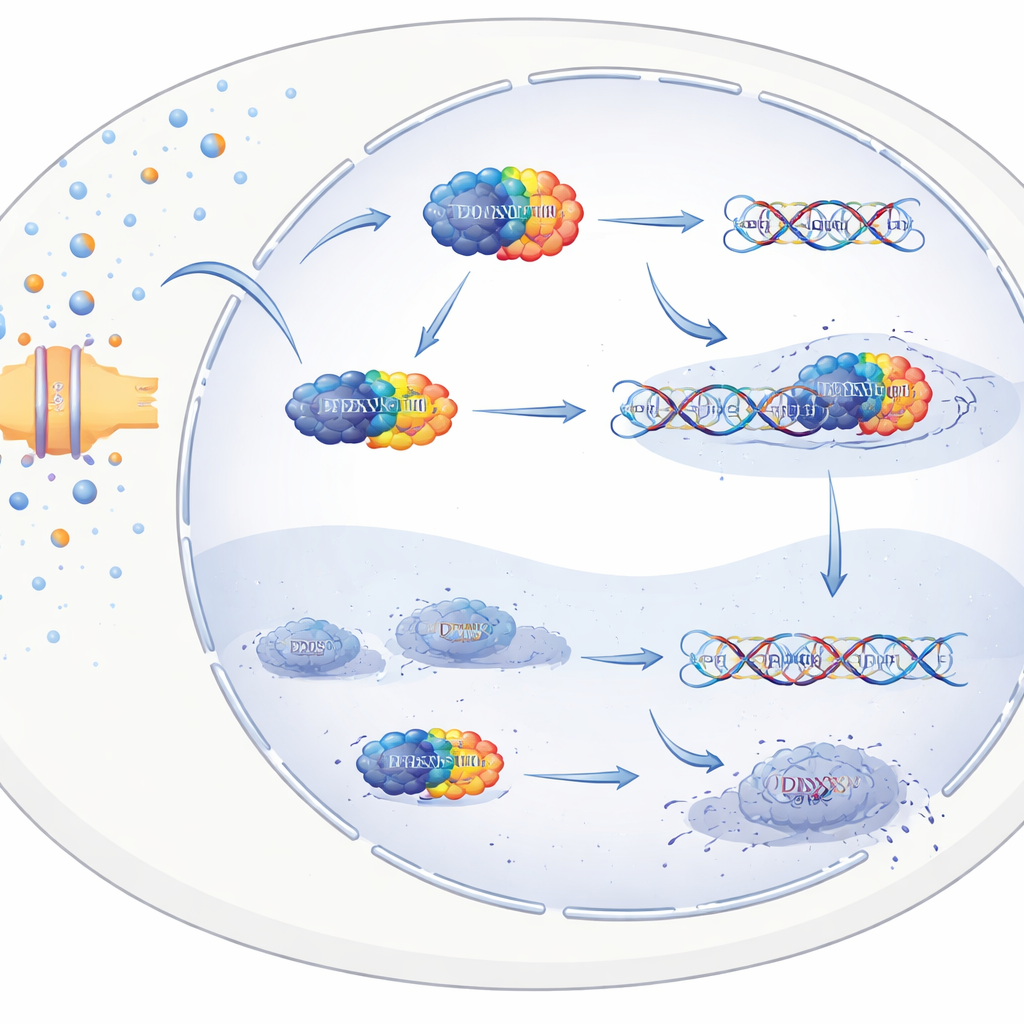
Jak arginina pomaga komórkom nowotworowym naprawiać ich DNA
Naukowcy następnie zapytali, jak arginina napędza przerzuty na poziomie molekularnym. Użyli chemicznego „zaczepu”, by wyłowić białka, które fizycznie wiążą argininę, i zidentyfikowali wiele białek obsługujących RNA, koncentrując się na jednym zwanym DDX3X. To białko występowało w większych ilościach w przerzutach niż w guzach pierwotnych i wiązało się z gorszymi wynikami pacjentów. Eksperymenty laboratoryjne i symulacje komputerowe pokazały, że arginina przyłącza się do konkretnego regionu DDX3X i zmienia jego lokalizację wewnątrz komórki. Przy wysokich poziomach argininy DDX3X gromadzi się w jądrze komórkowym, ponieważ arginina zakłóca sygnał, który normalnie eksportuje DDX3X z powrotem do cytoplazmy. Raz w jądrze, DDX3X łączy się z DNA i zwiększa aktywność genów zaangażowanych w szlaki odpowiedzi na uszkodzenia DNA, w szczególności osi ATM–CHK2–p53, która wykrywa pęknięcia DNA i koordynuje ich naprawę.
Przetrwanie stresu w niebezpiecznym otoczeniu
Komórki przerzutowe w sieci mierzą się z intensywnym stresem oksydacyjnym i wykazują więcej uszkodzeń DNA niż guzy pierwotne, co w zasadzie zagraża ich przetrwaniu. Badanie wykazało, że przerzuty bogate w argininę miały także wyższe poziomy markerów aktywnej naprawy DNA. Gdy do komórek narażonych na chemioterapię lub stres oksydacyjny dodano argininę, pęknięcia DNA były naprawiane wydajniej i mniej komórek ginęło. Usunięcie DDX3X lub zablokowanie białek ATM albo CHK2 działających poniżej niego niwelowało ten efekt ochronny. Innymi słowy, arginina pozwala komórkom przerzutowym raka jajnika wyczuwać środowisko odżywcze i przez DDX3X włączać silne programy naprawy DNA, które pomagają im przetrwać zarówno w wrogiej niszy sieci, jak i podczas terapii przeciwzaknowotworowej.
Zamiana łaknienia na substancję odżywczą w okazję terapeutyczną
Ponieważ długotrwałe ograniczanie argininy u pacjentek może być trudne, autorzy zbadali strategie oparte na lekach. U myszy usuwanie argininy z krwiobiegu za pomocą enzymu lub bezpośrednie hamowanie DDX3X małą cząsteczką spowolniło wzrost guzów, zmniejszyło rozsiew przerzutowy i wydłużyło przeżycie. Połączenie deplecji argininy z inhibicją DDX3X działało jeszcze lepiej, a blokada DDX3X uczulila także komórki oporne na cisplatynę na chemioterapię, zmniejszając oporne guzy u myszy. Razem wyniki ujawniają, że przerzuty w sieci w raku jajnika są metabolicznie uzależnione od zewnętrznej argininy, którą kierują przez DDX3X, by utrzymać naprawę DNA i przeżycie. Celowanie w układ arginina–DDX3X–naprawa DNA, poprzez ograniczenie argininy lub hamowanie DDX3X, może otworzyć nowe drogi zapobiegania i leczenia przerzutowego raka jajnika oraz przezwyciężania oporności na leki.
Cytowanie: Tian, J., Lei, T., Du, Y. et al. Arginine dependency in omental metastasis of epithelial ovarian cancer reveals a therapeutic vulnerability. Cell Death Dis 17, 354 (2026). https://doi.org/10.1038/s41419-026-08606-3
Słowa kluczowe: rak jajnika, metabolizm argininy, przerzuty nowotworowe, naprawa uszkodzeń DNA, DDX3X