Clear Sky Science · pl
Mechanizm sprzężenia zwrotnego z komórek raka prostaty do makrofagów, wzmacniany przez STAT1, reguluje postęp guza i oporność na radioterapię
Dlaczego te badania są ważne
Radioterapia jest podstawową metodą leczenia raka prostaty, jednak wiele guzów stopniowo przestaje na nią reagować, co pozwala chorobie na odnowę lub rozsiew. Badanie ujawnia ukrytą chemiczną „rozmowę” między komórkami raka prostaty a pobliskimi komórkami odpornościowymi zwanymi makrofagami, która pomaga nowotworom przetrwać napromienianie. Dekodując tę pętlę, naukowcy wskazują nowe cele farmakologiczne, które mogłyby zwiększyć skuteczność radioterapii u mężczyzn z zaawansowanym rakiem prostaty.
Komórki nowotworowe, które inaczej spalają cukier
Komórki raka prostaty, jak wiele guzów, polegają na zmienionej formie spalania cukru zwanej glikolizą tlenową. Zamiast pełnego rozkładu cukru z udziałem tlenu wybierają szybszą, lecz mniej wydajną ścieżkę, która produkuje duże ilości kwasu mlekowego. Zespół zidentyfikował białko wewnątrz komórek nowotworowych, STAT1, jako kluczowy przełącznik uruchamiający ten „głodny cukru” stan. STAT1 zwiększa aktywność trzech podstawowych enzymów napędzających glikolizę, podnosząc zarówno pobieranie cukru, jak i produkcję kwasu mlekowego. W hodowlach komórkowych i modelach mysich guzy z wyższym poziomem STAT1 rosły szybciej i były bardziej oporne na promieniowanie, podczas gdy blokada glikolizy osłabiała te agresywne cechy. 
Jak odpady z guza przekształcają komórki odpornościowe
Kwas mlekowy często bywa postrzegany jako metaboliczne „odpady”, ale w otoczeniu guza działa raczej jak sygnał. Naukowcy wykazali, że kwas mlekowy wydzielany przez komórki raka prostaty jest pobierany przez makrofagi za pośrednictwem transportera błonowego MCT1. Po wejściu aktywuje wewnętrzny system alarmowy znany jako szlak NFκB, który popycha makrofagi w stronę stanu pomocniczego nazwanego M2. Zamiast atakować raka, makrofagi M2 zwykle tłumią odpowiedzi immunologiczne i wspierają wzrost guza, na przykład promując tworzenie naczyń krwionośnych. Gdy naukowcy zablokowali glikolizę w komórkach nowotworowych, zahamowali produkcję kwasu mlekowego lub uniemożliwili jego wejście do makrofagów, komórki odpornościowe odchylały się od wspierającego guz stanu M2 i przechodziły w bardziej obronny profil.
Makrofagi wysyłają sygnały wzrostu z powrotem do guza
Historia nie kończy się na samych zmianach charakteru makrofagów. Gdy kwas mlekowy aktywuje w nich NFκB, makrofagi zaczynają produkować i wydzielać silny czynnik sygnałowy zwany MCP-1. Cząsteczka ta dyfunduje z powrotem do komórek raka prostaty i wiąże się z receptorem powierzchniowym CCR2. To wiązanie uruchamia kolejny wewnętrzny szlak w komórkach nowotworowych, obejmujący białka JAK i STAT1. Innymi słowy, ten sam STAT1, który początkowo napędzał nadmierne spalanie cukru, zostaje ponownie włączony przez sygnał wywodzący się ostatecznie od kwasu mlekowego, który on sam pomógł wygenerować. Gdy badacze dodali MCP-1 do komórek raka prostaty, glikoliza wzrosła, komórki proliferowały i poruszały się łatwiej, a także efektywniej naprawiały uszkodzenia DNA wywołane promieniowaniem. Blokada CCR2 lub JAK zapobiegała tym efektom.
Samo-wzmacniająca się pętla przetrwania
W całości wyniki ujawniają samo-wzmacniającą się pętlę między komórkami raka a makrofagami. STAT1 w komórkach raka prostaty zwiększa rozkład cukru i uwalnianie kwasu mlekowego. Ten kwas mlekowy jest importowany do makrofagów, gdzie aktywuje NFκB i popycha je w stronę wspierającego guz stanu M2, jednocześnie wywołując produkcję MCP-1. MCP-1 następnie wraca do komórek nowotworowych, aktywuje CCR2 i szlak JAK/STAT1, dodatkowo wzmacniając glikolizę i oporność na radioterapię. Eksperymenty na zwierzętach wykazały, że leki blokujące CCR2 lub JAK, szczególnie w połączeniu z radioterapią, spowalniały wzrost guza i zmniejszały obecność makrofagów M2, podkreślając kliniczny potencjał ukierunkowania tej pętli. 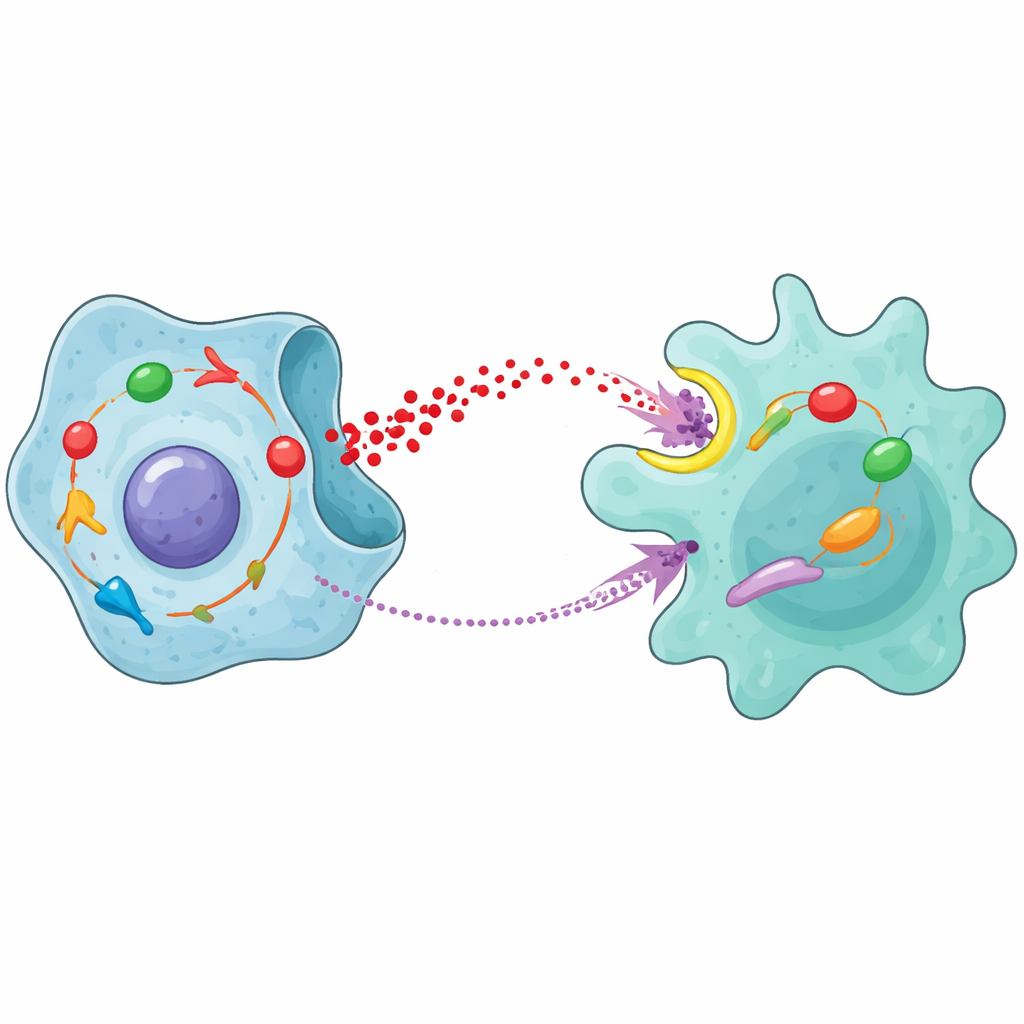
Co to oznacza dla pacjentów
Dla osoby nietechnicznej kluczowa idea jest taka, że guzy prostaty i niektóre komórki odpornościowe tworzą chemiczne partnerstwo, które pomaga nowotworowi przetrwać leczenie radiacyjne. Komórki guza zmieniają sposób wykorzystania cukru, produkując kwas mlekowy, który przeprogramowuje pobliskie makrofagi na sojuszników zamiast wrogów. Te przeprogramowane komórki następnie wysyłają sygnały z powrotem, które czynią guzy bardziej odporne i trudniejsze do zniszczenia. Przerywając tę pętlę — na poziomie obróbki kwasu mlekowego, sygnału MCP-1 lub dalszego szlaku JAK/STAT1 — przyszłe terapie mogłyby osłabić obronę guza i umożliwić skuteczniejsze działanie radioterapii, dając nadzieję mężczyznom z trudnym do leczenia rakiem prostaty.
Cytowanie: Chen, JY., Xue, YT., Lin, B. et al. A feedback mechanism from prostate cancer cells to macrophages, reinforced by STAT1, regulates tumor progression and resistance to radiotherapy. Cell Death Dis 17, 282 (2026). https://doi.org/10.1038/s41419-026-08577-5
Słowa kluczowe: rak prostaty, oporność na radioterapię, mikrośrodowisko guza, makrofagi, metabolizm mleczanu