Clear Sky Science · pl
Inhibicja kinazy powiązanej z Vaccinia 2 ujawnia wrażliwość metabolizmu glutationu w raku trzustki
Dlaczego to ma znaczenie dla raka trzustki
Rak trzustki należy do najbardziej śmiertelnych nowotworów, częściowo dlatego, że standardowe terapie często zawodzą. To badanie ujawnia ukrytą słabość niektórych guzów trzustki: zależność od komórkowej „tarczy” chroniącej przed toksycznymi produktami ubocznymi reaktywnego tlenu. Zrozumienie, kiedy ta tarcza jest kruche i jak gen nowotworowy VRK2 ją wzmacnia, pozwala badaczom zaproponować nowe sposoby selektywnego zatruwania komórek rakowych przy minimalnym uszkodzeniu tkanek zdrowych.
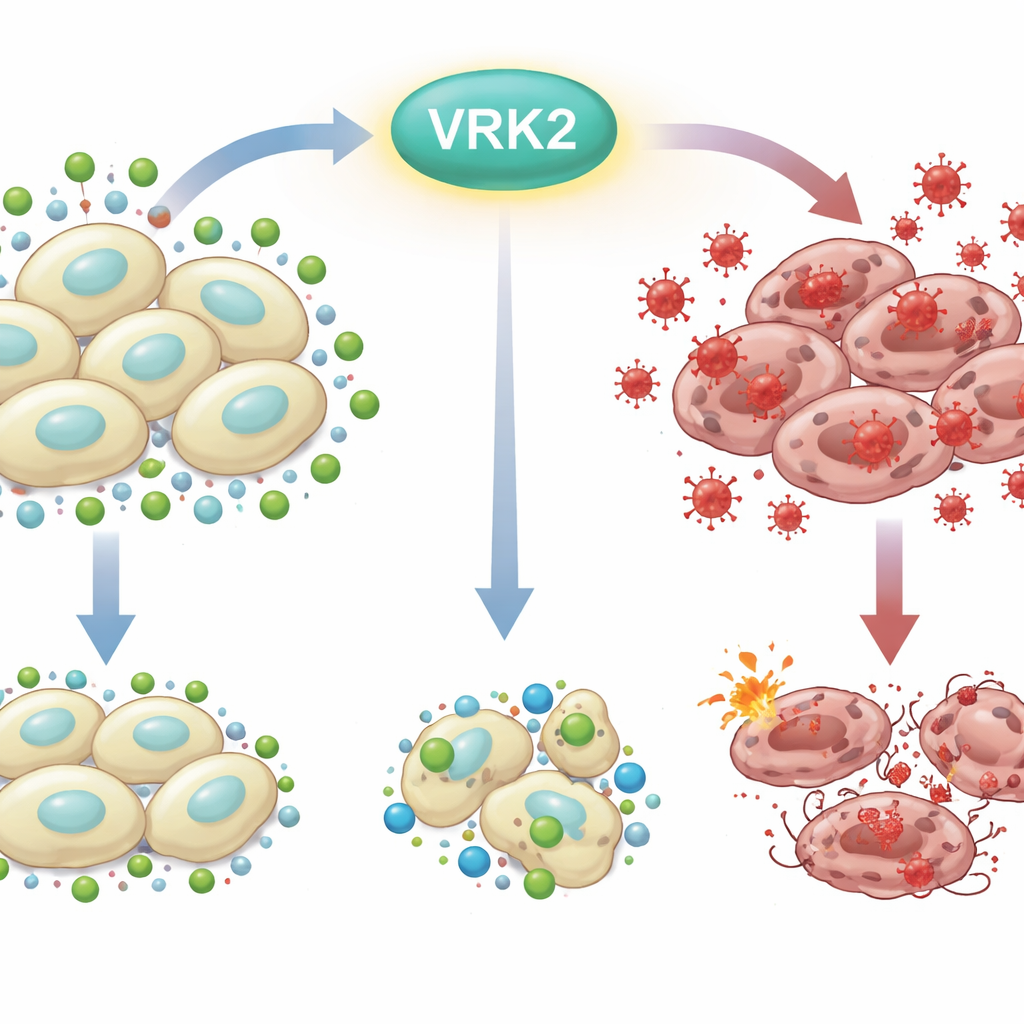
Problem rdzy w komórce
Każda komórka nieustannie walczy z „rdzewieniem od środka” wywoływanym przez reaktywne formy tlenu — silnie reaktywne postacie tlenu, które mogą uszkadzać DNA, lipidy i białka. Aby przetrwać, komórki korzystają z chemicznych mechanizmów obronnych, z glutationem jako jednym z najważniejszych elementów ochronnych. Komórki raka trzustki, które żyją w trudnych warunkach i szybko rosną, silnie polegają na metabolicznych sztuczkach, by utrzymać wystarczające zapasy glutationu. Zakłócenie równowagi między szkodliwymi utleniaczami a ochronnymi przeciwutleniaczami może popchnąć komórki nowotworowe za granę przeżycia i doprowadzić do ich śmierci.
Odnalezienie ukrytego punktu słabości
Badacze zaczęli od wyłączenia VRK2, genu sprzyjającego nowotworzeniu i wcześniej powiązanego z gorszymi wynikami w raku trzustki, a następnie przetestowali 281 związków celujących w metabolizm. Odkryli, że komórki pozbawione VRK2 były niezwykle wrażliwe na leki blokujące produkcję glutationu. W tych komórkach poziom glutationu spadł, a reactive oxygen gwałtownie wzrosły, co doprowadziło do ich śmierci. Dostarczenie dodatkowych przeciwutleniaczy lub związków podobnych do glutationu je uratowało, potwierdzając, że kluczowa słabość tkwiła w upośledzonej zdolności do detoksykacji stresu oksydacyjnego.
Jak VRK2 wzmacnia zbroję komórek nowotworowych
Następnie zespół zadał pytanie, dlaczego VRK2 wpływa na metabolizm glutationu. Skoncentrowali się na białku transportującym o nazwie SLC7A11, które osadzone w błonie komórkowej przemyca cystynę — składnik niezbędny do syntezy glutationu. Zaskakująco, VRK2 nie zmieniał ogólnej ilości produkowanego SLC7A11; zamiast tego kontrolował, czy ten transporter trafia skutecznie na powierzchnię komórki. W zdrowych komórkach z aktywnym VRK2, SLC7A11 przemieszcza się z retikulum endoplazmatycznego przez aparat Golgiego na błonę. VRK2 wspomaga ten transport, chemicznie modyfikując białko sortujące ładunek o nazwie Sec24C, które pomaga załadować SLC7A11 do pęcherzyków transportowych. Gdy VRK2 jest nieobecny lub zablokowany, SLC7A11 utknie wewnątrz komórki, mniej transporterów trafia na powierzchnię, a tarcza z glutationu słabnie.
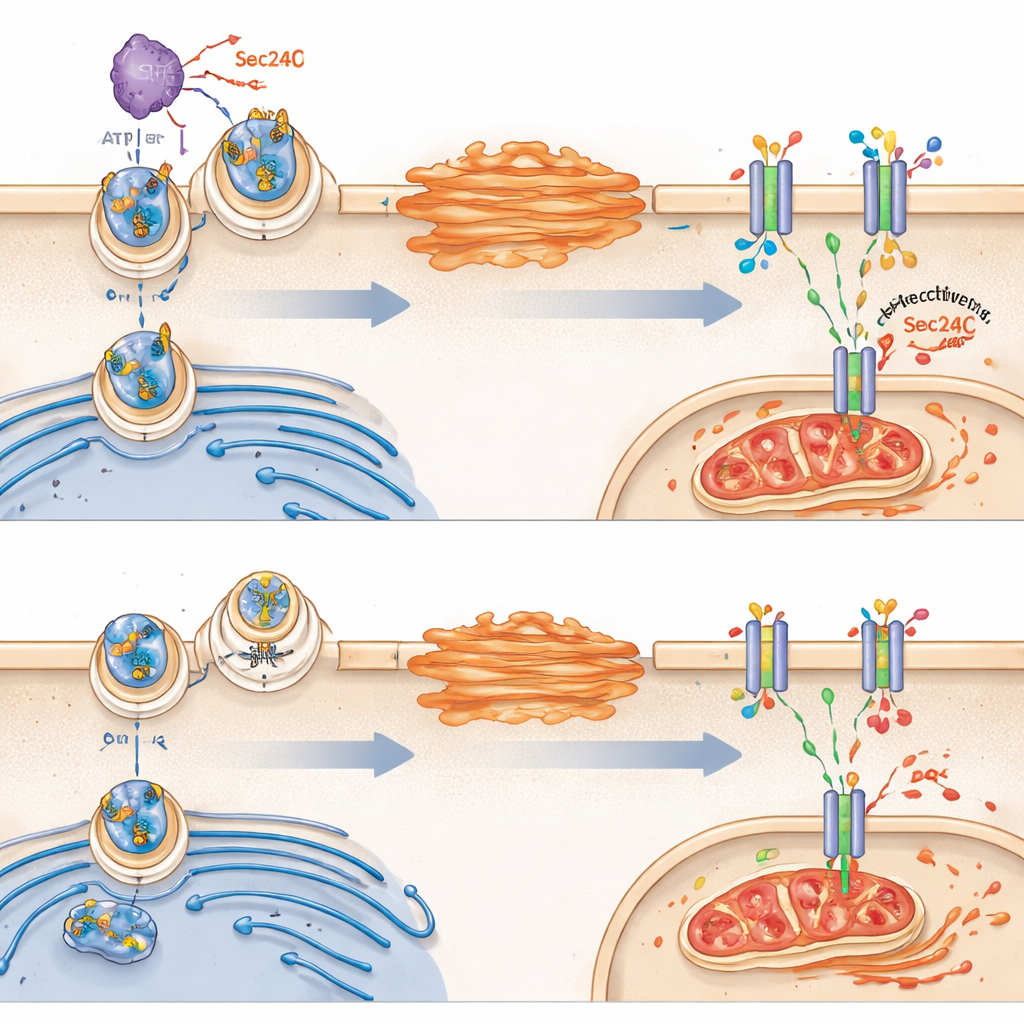
Od złamanej tarczy do ferroptozy
Bez wystarczającej ilości SLC7A11 w błonie komórkowej, komórki pozbawione VRK2 mają trudności z importem cystyny i utrzymaniem poziomu glutationu. Czyni to je szczególnie podatnymi na rodzaj śmierci komórkowej zależnej od żelaza zwany ferroptozą, charakteryzujący się niekontrolowaną oksydacją lipidów błony komórkowej i uszkodzeniem mitochondriów. Badanie wykazało, że leki hamujące syntezę glutationu wywoływały cechy ferroptozy w komórkach pozbawionych VRK2, w tym zdeformowane mitochondria i nagromadzenie produktów utleniania lipidów. Zablokowanie ferroptozy, ale nie innych typów śmierci komórkowej, chroniło te komórki, podkreślając, że ich piętą Achillesową jest niezdolność do opanowania uszkodzeń oksydacyjnych.
Wskazówki dla spersonalizowanych decyzji terapeutycznych
Na koniec badacze przeszli do modeli zwierzęcych i komórek świeżo pobranych od pacjentów. Guzy o niskim poziomie VRK2 kurczyły się po leczeniu lekiem celującym w glutation, podczas gdy guzy o wysokiej ekspresji VRK2 w dużej mierze mu się opierały. Jednak gdy guzy o wysokim VRK2 otrzymały dodatkowo związek blokujący VRK2, odzyskały wrażliwość na hamowanie glutationu. To sugeruje, że poziom VRK2 może podzielić pacjentów na grupy: tych, których guzy są naturalnie podatne na terapię ukierunkowaną na glutation, oraz tych, którzy mogliby skorzystać z dwufazowej strategii — najpierw wyłączenia VRK2, a potem ataku na metabolizm glutationu.
Co to oznacza dla pacjentów
Mówiąc wprost, praca ta pokazuje, że niektóre nowotwory trzustki przetrwają dzięki VRK2, które utrzymuje silną tarczę antyoksydacyjną. Usuń VRK2, a tarcza staje się cieńsza; dodatkowo zablokuj glutation i komórki nowotworowe załamią się pod naporem stresu oksydacyjnego. Pomiar VRK2 w guzach mógłby więc pomóc lekarzom zdecydować, którzy pacjenci najprawdopodobniej skorzystają z leków zaburzających metabolizm glutationu, a którzy najpierw będą potrzebować terapii celującej w VRK2. Choć potrzebne są dalsze badania kliniczne, praca wytycza jasną drogę do bardziej dopasowanych, opartych na metabolizmie terapii dla nowotworu, który pilnie potrzebuje lepszych opcji leczenia.
Cytowanie: Chen, S., Fu, X., Zhang, T. et al. Vaccinia-related kinase 2 inhibition elicits vulnerability of glutathione metabolism in pancreatic cancer. Cell Death Dis 17, 325 (2026). https://doi.org/10.1038/s41419-026-08573-9
Słowa kluczowe: rak trzustki, metabolizm glutationu, VRK2, ferroptoza, SLC7A11