Clear Sky Science · pl
Tłumienie EGFR przez nowy biguanid 4C zwiększa wrażliwość raka jajnika na inhibitory PARP poprzez obniżenie poziomu BRCA2 i Rad51
Dlaczego to badanie ma znaczenie
Dla wielu osób z rozpoznanym rakiem jajnika obecne leki celowane działają jedynie u niewielkiej mniejszości pacjentów, których guzy mają określone wady genetyczne. To badanie bada sposób na rozszerzenie korzyści ważnej klasy leków, zwanych inhibitorami PARP, na znacznie większą grupę pacjentów, których guzy nie noszą tych mutacji. Poprzez połączenie nowego związku eksperymentalnego z istniejącymi lekami, autorzy pokazują strategię, która skłania komórki nowotworowe do śmiertelnej „ślepej uliczki”, przy jednoczesnym oszczędzaniu tkanek zdrowych.
Przeszkoda w obecnym leczeniu raka jajnika
Rak jajnika jest często wykrywany w późnym stadium i pozostaje jednym z najśmiertelniejszych nowotworów u kobiet. Inhibitory PARP, takie jak olaparib, mogą być wyjątkowo skuteczne, ale głównie u pacjentów, których guzy mają już defekty w szlaku naprawy DNA związanym z genami BRCA1 i BRCA2. Większość guzów jednak ma nadal sprawny mechanizm naprawczy i potrafi naprawiać uszkodzenia DNA wywołane przez te leki, co pozwala komórkom nowotworowym przetrwać. Kluczową rolę w tej naprawie odgrywają dwa białka, BRCA2 i Rad51, które pomagają złączyć przerwane nici DNA w procesie zwanym homologicznie uzależnioną rekombinacją. Znalezienie sposobów selektywnego osłabienia tego szlaku naprawczego w komórkach nowotworowych mogłoby uczynić inhibitory PARP użytecznymi dla znacznie większej liczby pacjentów.
Rola dobrze znanego przełącznika wzrostu
Zespół skupił się na dobrze znanej cząsteczce powiązanej z rakiem — receptorze naskórkowego czynnika wzrostu (EGFR), który znajduje się na powierzchni wielu komórek nowotworowych i napędza ich wzrost. Stwierdzili oni, że EGFR robi więcej niż tylko przekazywać sygnały wzrostu: w komórkach raka jajnika z prawidłowymi genami BRCA wysoki poziom EGFR wiązał się z gorszym przeżyciem pacjentów i opornością na inhibitory PARP. Gdy EGFR został zredukowany lub wyłączony w hodowlach komórkowych i u myszy, guzy stały się znacznie bardziej wrażliwe na olaparib. Badacze wykazali, że EGFR pomaga sprowadzać BRCA2 i Rad51 do jądra komórkowego po uszkodzeniu DNA, gdzie mogą naprawiać pęknięcia i osłabiać efekt leczenia. Sama blokada aktywności enzymatycznej EGFR nie wystarczała; należało obniżyć całkowitą ilość białka EGFR, aby istotnie zakłócić ten szlak naprawczy.
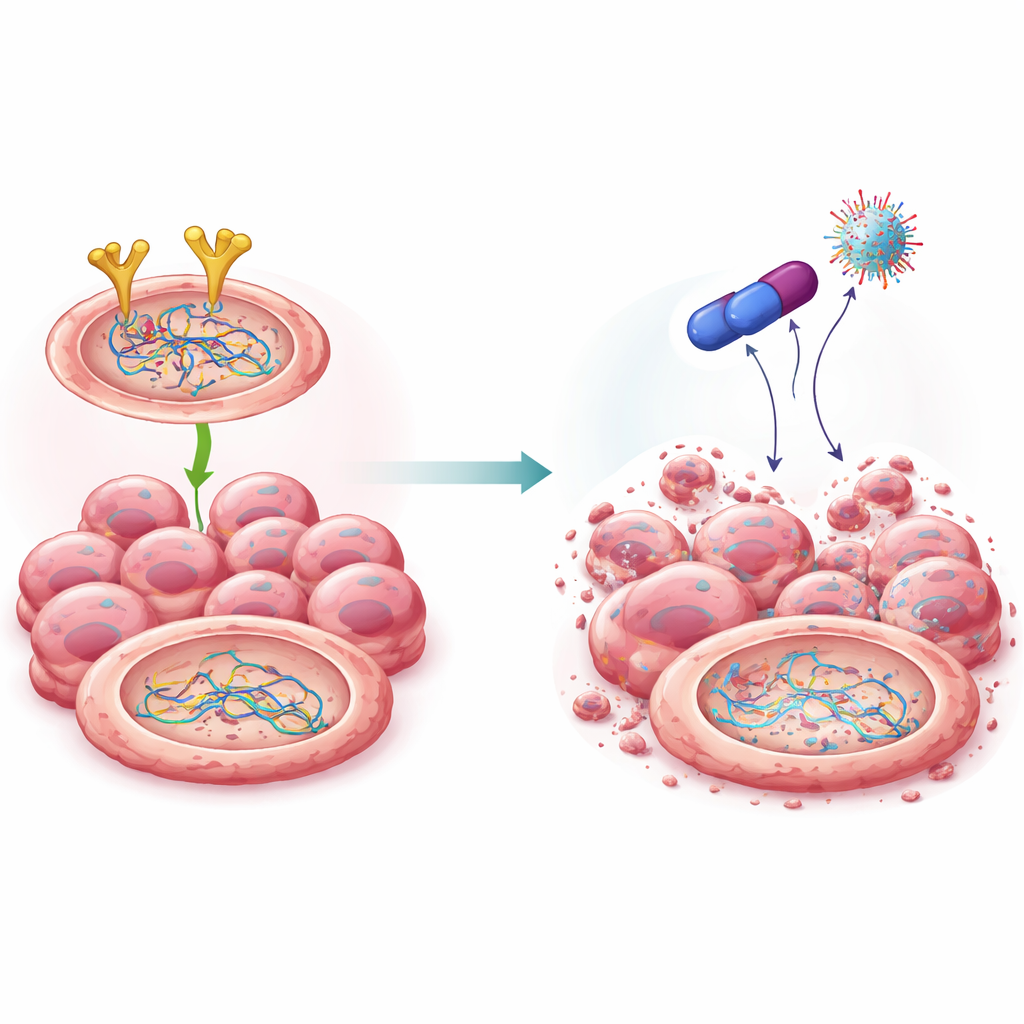
Nowy związek, który unieszkodliwia załogę naprawczą
Opierając się na wcześniejszych badaniach nad rodziną leków znanych jako biguanidy, naukowcy zsyntetyzowali kilka chemicznych krewnych i zidentyfikowali jeden wyróżniający się związek, nazwany 4C. Ten związek był silnie toksyczny dla komórek raka jajnika, a stosunkowo łagodny dla komórek normalnych. Modele komputerowe i testy laboratoryjne wskazały, że 4C wiąże się bezpośrednio z EGFR i oznacza go do zniszczenia w komórkowym systemie degradacji białek. W odróżnieniu od niektórych istniejących leków przeciw EGFR, 4C zmniejszał całkowitą ilość EGFR, zamiast jedynie wygaszać jego aktywność. W miarę spadku poziomu EGFR spadła też stabilność BRCA2 i Rad51: były one oznaczane do usunięcia, rozkładane i nie były już w stanie wspierać efektywnej naprawy DNA. Co ważne, te zmiany zachodziły na poziomie białek bez zmiany samych genów.
Blokowanie drogi ratunkowej wewnątrz komórki
Badanie ujawniło bardziej szczegółowy ciąg zdarzeń łączący uszkodzenie DNA z przeżyciem guza. Po tym jak inhibitory PARP uszkadzają DNA, inny białkowy czujnik zwany ATM wysyła sygnał z jądra do ciała komórkowego. W odpowiedzi EGFR współdziała z BRCA2 i Rad51 i pomaga im przemieścić się do jądra, gdzie naprawiają uszkodzenia. Naukowcy odkryli, że trzecie białko, c-Cbl, normalnie działa jak rodzaj „etykietera” wskazującego BRCA2 i Rad51 do utylizacji. EGFR konkuruje z c-Cbl o dostęp do tych białek naprawczych, chroniąc je przed oznaczeniem do zniszczenia. Gdy 4C obniża poziom EGFR, c-Cbl może łatwiej wiązać się z BRCA2 i Rad51, co prowadzi do ich oznaczania, rozkładu i utraty. Przy mniejszej liczbie białek naprawczych w jądrze, uszkodzenia DNA się kumulują, a komórki nowotworowe stają się znacznie bardziej wrażliwe na inhibitory PARP.
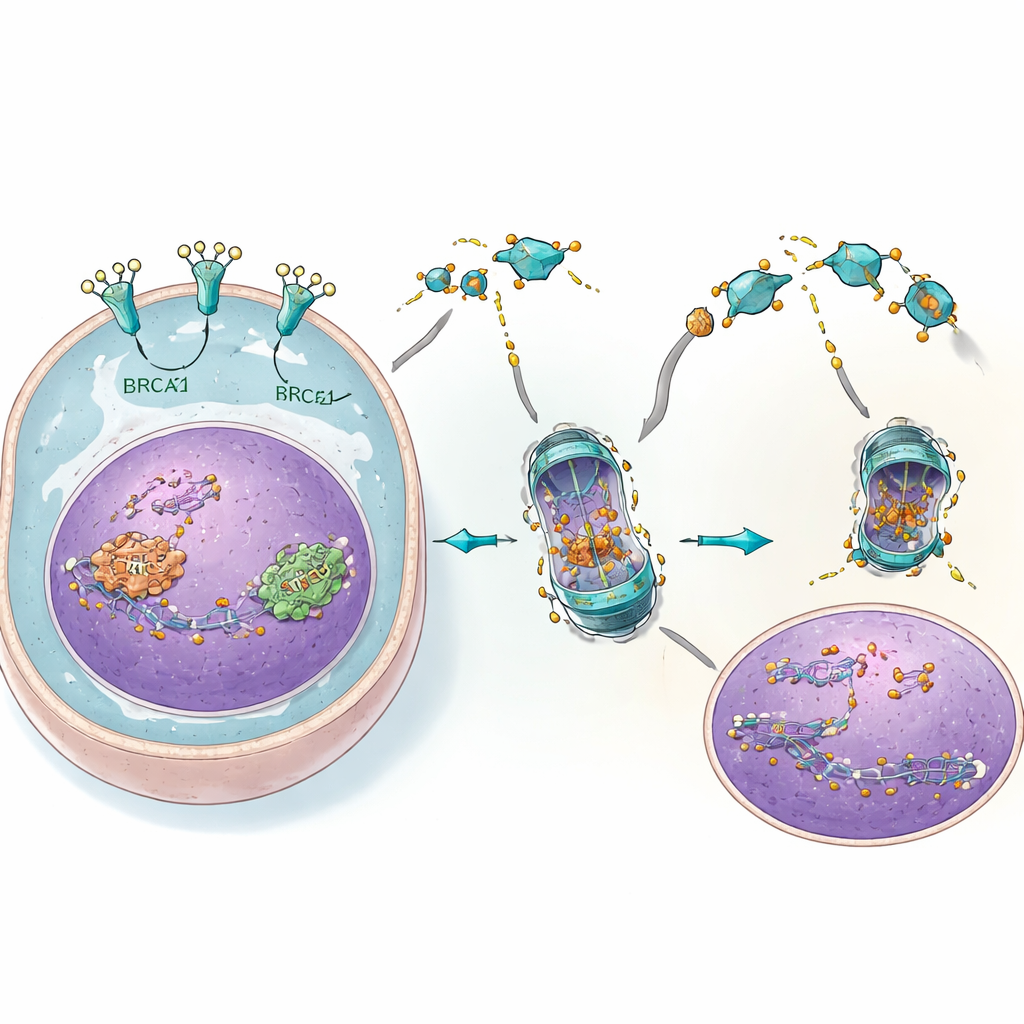
Od komórek do zwierząt: silne połączenie
W hodowlach komórkowych i modelach mysich połączenie 4C z inhibitorami PARP dało silny efekt synergiczny. Guzy z prawidłowymi genami BRCA, które opierały się na pojedynczym leczeniu, drastycznie się zmniejszały lub przestawały rosnąć po ekspozycji na oba leki jednocześnie. Markery uszkodzeń DNA gwałtownie wzrosły, co jest zgodne z hipotezą o przeładowaniu mechanizmów naprawy. Jednocześnie komórki normalne i ważne narządy, takie jak wątroba i nerki, wykazywały niewiele oznak uszkodzenia, prawdopodobnie dlatego, że mają znacznie niższe poziomy EGFR i w mniejszym stopniu polegają na tej konkretnej drodze naprawczej. Korzyści z kombinacji obejmowały także zmniejszenie zdolności komórek raka jajnika do rozsiewu w organizmie.
Co to może znaczyć dla pacjentów
Praca ta proponuje sposób przekształcenia siły komórki nowotworowej w jej słabość. Poprzez ukierunkowanie EGFR nowym związkiem 4C, badacze pozbawiają ochrony, którą zapewniały BRCA2 i Rad51, powodując, że guzy z normalną naprawą DNA zachowują się podobnie do nowotworów z mutacjami BRCA w reakcji na inhibitory PARP. Ta wymuszona podatność, znana jako „syntetyczna śmiertelność”, mogłaby rozszerzyć zastosowanie istniejących leków na wiele więcej kobiet z rakiem jajnika, przy zachowaniu kontrolowalnych efektów ubocznych. Chociaż 4C jest wciąż związkiem eksperymentalnym i wymaga obszernego testowania w bardziej zaawansowanych modelach i badaniach klinicznych, badanie przedstawia klarowny plan, w jaki sposób rozmontowanie określonych pomocników naprawy w komórkach nowotworowych może poprawić wyniki leczenia.
Cytowanie: Xiao, D., Yao, J., Yang, X. et al. Repression of EGFR by new biguanide 4C potentiated ovarian cancer to PARP inhibitors through down-regulation of BRCA2 and Rad51. Cell Death Dis 17, 317 (2026). https://doi.org/10.1038/s41419-026-08556-w
Słowa kluczowe: rak jajnika, inhibitory PARP, EGFR, naprawa DNA, terapia celowana