Clear Sky Science · pl
Utrata PRKACB ułatwia przerzuty raka żołądka typu rozlanego poprzez aktywację sygnalizacji RhoA
Dlaczego to badanie ma znaczenie dla raka żołądka
Rak żołądka typu rozlanego to szczególnie agresywna postać nowotworu żołądka, która często szeroko rozprzestrzenia się w jamie brzusznej, co utrudnia leczenie i zwiększa śmiertelność. Badanie to analizuje, dlaczego te guzy tak chętnie dają przerzuty, odkrywając molekularny mechanizm hamujący, który normalnie powstrzymuje komórki nowotworowe przed wędrówką — oraz pokazując, co się dzieje, gdy ten hamulec zawodzi. Zrozumienie tego ukrytego przełącznika może otworzyć nowe drogi do przewidywania pacjentów z najwyższym ryzykiem i do opracowania leków, które spowalniają lub zatrzymują niebezpieczne rozprzestrzenianie się.
Groźna postać raka żołądka
Nie wszystkie raki żołądka zachowują się tak samo. Guzy typu jelitowego mają tendencję do tworzenia bardziej uporządkowanych mas, podczas gdy rak żołądka typu rozlanego (DGC) składa się z rozproszonych komórek, które łatwo oddzielają się od guza pierwotnego. Pacjenci z DGC mają wyższe ryzyko zgonu niż osoby z rakiem typu jelitowego, częściowo dlatego, że ich guzy łatwiej zasiają nowe ogniska wzrostu w całej jamie brzusznej. Wcześniejsze badania genetyczne powiązały DGC z nawracającymi zmianami w genie RHOA, który wpływa na ruch i kształt komórek. Nie było jednak jasne, jak te zmiany łączą się z szerszymi sieciami sygnalnymi, które kontrolują, czy komórki nowotworowe pozostaną na miejscu, czy zaczną migrować.
Odnalezienie brakującego hamulca w próbkach guzów
Naukowcy skoncentrowali się na białku PRKACB, katalitycznej podjednostce dobrze znanego enzymu kinazy białkowej A, która modyfikuje wiele zachowań komórkowych przez fosforylację innych białek. Wcześniejsze badanie proteomiczne zasugerowało, że poziomy PRKACB są nietypowo niskie w agresywnym DGC. Aby to sprawdzić, zespół przeanalizował próbki guzów od 376 pacjentów, porównując nowotwory typu rozlanego i jelitowego oraz ich pobliskie tkanki niezmienione chorobowo. Stwierdzili, że poziomy PRKACB były wyraźnie obniżone w guzach typu rozlanego, szczególnie w zaawansowanych stadiach, ale nie w rakach typu jelitowego. Pacjenci, których guzy miały niewielką ilość PRKACB, mieli istotnie gorsze przeżycie ogólne, nawet po uwzględnieniu innych czynników klinicznych, co sugeruje, że PRKACB pełni rolę supresora guza w tym kontekście.
W jaki sposób niski poziom PRKACB sprzyja ucieczce komórek
Aby sprawdzić, co PRKACB robi w komórkach nowotworowych, zespół użył hodowanych linii komórkowych modelujących rak żołądka typu rozlanego. Gdy sztucznie obniżono poziom PRKACB, komórki stały się bardziej ruchliwe i inwazyjne w testach laboratoryjnych, łatwiej przeciskały się przez bariery i tworzyły palcowate wypustki zwane pseudopodiami, które pomagają komórkom pełzać. Komórki te przeszły również ze stanu bardziej uporządkowanego, nabłonkowego, do luźniejszego, przypominającego mezenchymalny, związanego z przerzutami, tracąc cząsteczkę adhezji E‑kadherynę, która normalnie pomaga komórkom trzymać się razem. Z kolei zwiększenie poziomu PRKACB uczyniło komórki mniej zmotoryzowanymi i mniej inwazyjnymi. Co ważne, zmiany te nie wpływały na szybkość podziałów komórkowych, co wskazuje na specyficzną rolę PRKACB w umożliwianiu rozprzestrzeniania się, a nie wzrostu.
Przybliżenie się do przełącznika sygnalizacji RhoA
Naukowcy zapytali następnie, jak PRKACB wywiera ten efekt przeciwprzerzutowy. Używając metod badania interakcji białko–białko i modelowania strukturalnego, wykazali, że PRKACB bezpośrednio wiąże się z RhoA, molekularnym przełącznikiem, który przechodzi między formami nieaktywnymi i aktywnymi, kontrolując kształt i ruch komórek. PRKACB dodaje grupę fosforanową w konkretnym miejscu na RhoA (seryna 188), co wycisza RhoA i tłumi dalsze szlaki ROCK i FAK, które napędzają przebudowę cytoszkieletu i ruchliwość komórek. Gdy PRKACB był wyciszony, RhoA było mniej fosforylowane, bardziej aktywne, a sygnalizacja ROCK/FAK nasiliła się, prowadząc do bardziej agresywnego ruchu komórek. W modelach mysich, gdzie wszczepiono guzy przypominające ludzkie do ściany żołądka, obniżenie PRKACB skutkowało większą liczbą i większymi guzkami przerzutowymi w jamie brzusznej oraz wcześniejszym pojawieniem się widocznych przerzutów, ponownie bez zmiany tempa wzrostu już ugruntowanych przerzutów.
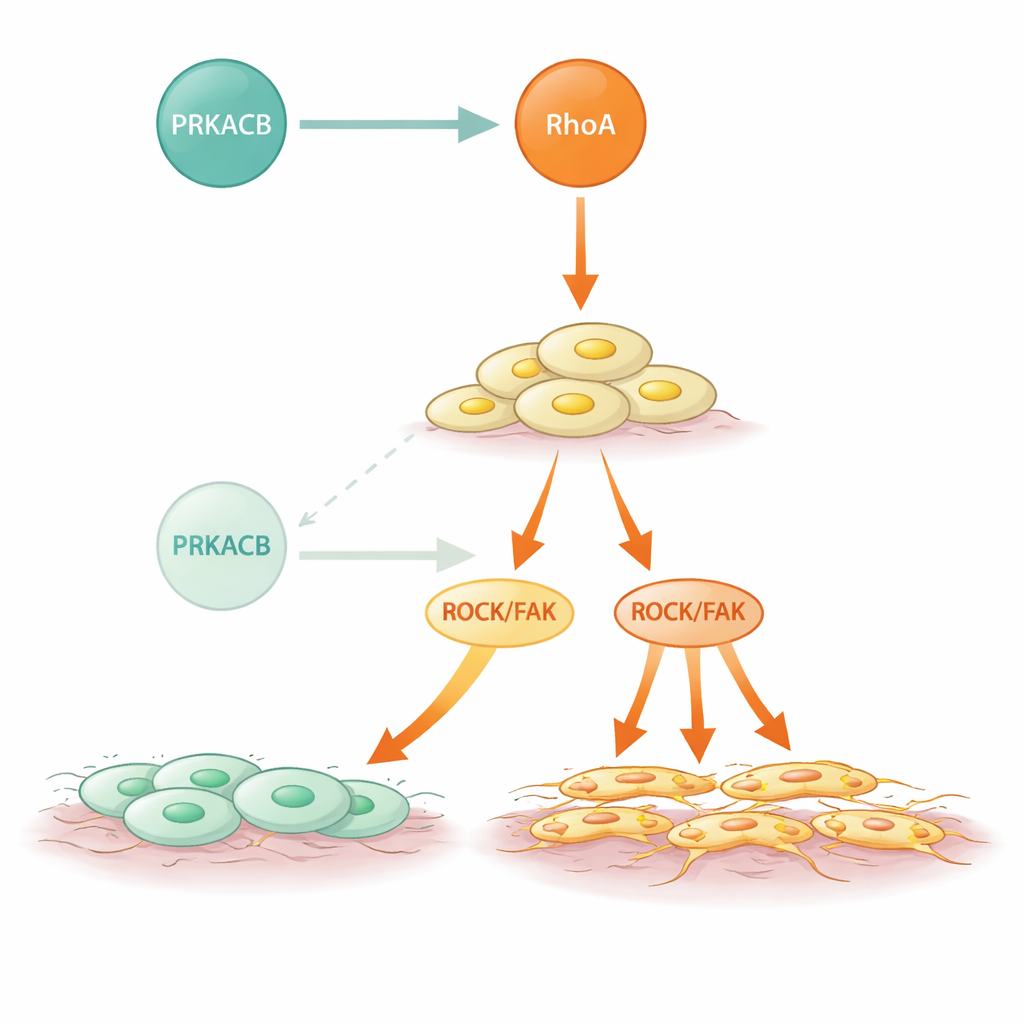
Mutacje w sygnalizacji i możliwy sposób interwencji
Raki żołądka typu rozlanego często noszą mutacje w RHOA, a to badanie pokazuje, jak niektóre z tych zmian potęgują problem. Kilka często występujących w DGC mutacji w RhoA osłabiło lub znosiło jego wiązanie z PRKACB, ale nie zakłócało zdolności RhoA do aktywacji swoich dalszych partnerów. W rezultacie te zmutowane formy uniknęły hamującej fosforylacji przez PRKACB i wykazywały zwiększoną aktywność ROCK oraz silniejsze zachowania inwazyjne. Co istotne, gdy badacze podawali komórkom i myszom związek blokujący RhoA, dodatkowe przerzuty wywołane niskim PRKACB zostały w dużej mierze zredukowane. Sugeruje to, że nawet w guzach, gdzie naturalny hamulec jest słaby lub nieobecny, bezpośrednie ukierunkowanie nadaktywnego szlaku RhoA może powstrzymać rozprzestrzenianie się.
Co to oznacza dla pacjentów i przyszłych terapii
Mówiąc prosto, praca ta identyfikuje PRKACB jako kluczowy element wewnętrznego obwodu „antymigracyjnego” w raku żołądka typu rozlanego. Gdy poziomy PRKACB spadają, lub gdy RhoA jest zmutowane tak, że PRKACB nie może się z nim związać i go zmodyfikować, sygnalizacja RhoA pracuje intensywniej, a komórki nowotworowe stają się bardziej zdolne do odrywania się i kolonizowania jamy brzusznej. Pomiar statusu PRKACB i RhoA w guzach mógłby pomóc lekarzom ocenić, jak prawdopodobne jest wystąpienie przerzutów u pacjenta i kto może najbardziej skorzystać na lekach hamujących szlak RhoA–ROCK–FAK. Chociaż takie terapie będą wymagać dalszego rozwoju i testów klinicznych, badanie to wytycza jasną molekularną ścieżkę od brakującego hamulca do śmiertelnych przerzutów — i wskazuje nowe sposoby spowolnienia tej drogi.
Cytowanie: Sun, J., Zhao, J., Yang, X. et al. Loss of PRKACB facilitates metastasis of diffuse-type gastric cancer through RhoA signaling activation. Cell Death Dis 17, 281 (2026). https://doi.org/10.1038/s41419-026-08553-z
Słowa kluczowe: rak żołądka typu rozlanego, przerzuty, PRKACB, sygnalizacja RhoA, szlak ROCK FAK