Clear Sky Science · pl
PD-1 chroni proliferujące ludzkie limfocyty T przed przedwczesną śmiercią wywołaną ponowną stymulacją, modulując sygnalizację TCR i CD28
Dlaczego powstrzymywanie „przyjaznych ostrzałów” w układzie odpornościowym ma znaczenie
Nasz układ odpornościowy opiera się na armiach limfocytów T, które szybko się mnożą, by zwalczać infekcje i nowotwory. Jednak ten gwałtowny wzrost jest niebezpieczny: jeżeli zbyt wiele komórek T pozostanie aktywnych zbyt długo, mogą uszkadzać zdrowe tkanki lub napędzać choroby autoimmunizacyjne. W tym badaniu analizowano, jak dobrze znana „hamulcowa” cząsteczka PD‑1 pomaga proliferującym ludzkim limfocytom T uniknąć przedwczesnej śmierci wywołanej nadmierną aktywacją. Zrozumienie tej równowagi jest kluczowe dla bezpieczniejszych immunoterapii przeciwnowotworowych i zapobiegania szkodliwym nadreakcjom immunologicznym.
Wbudowany mechanizm samodestrukcji, który musi być precyzyjnie wyregulowany
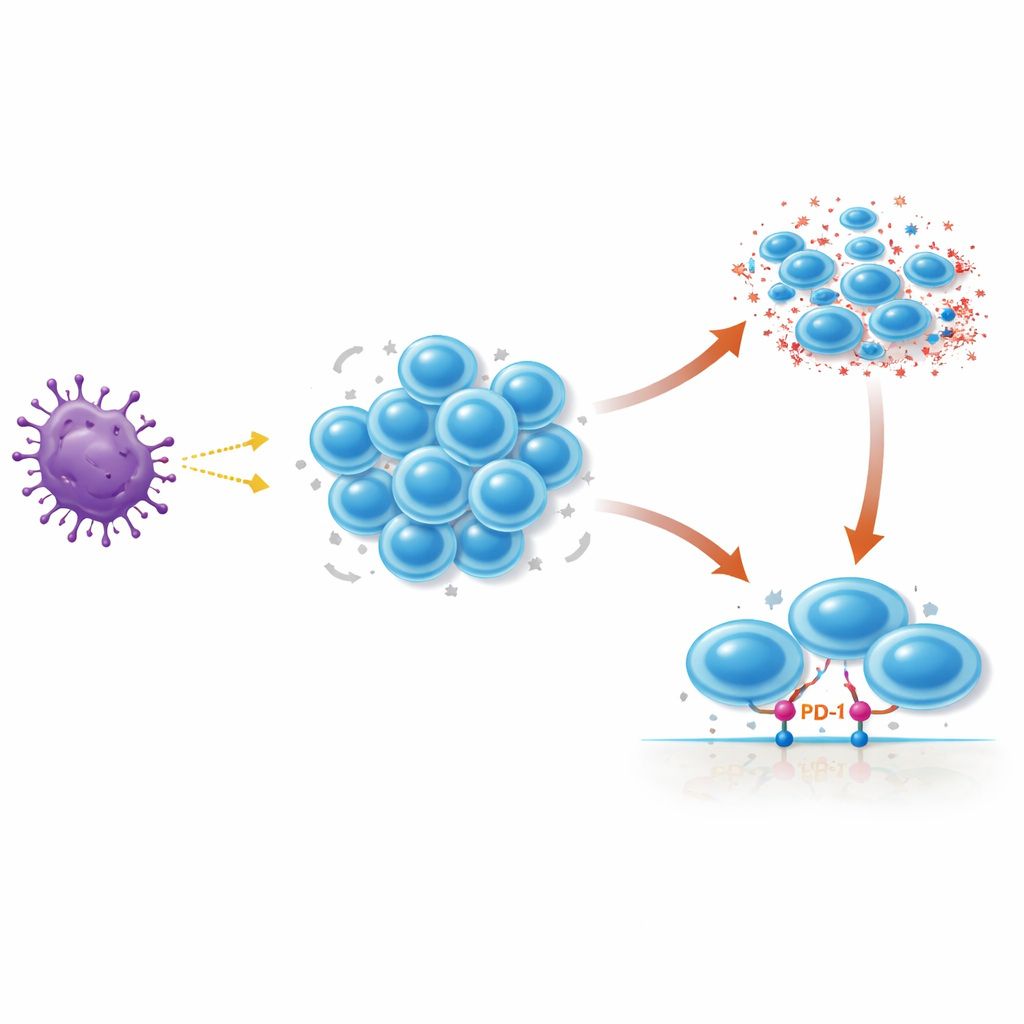
Gdy komórki T rozpoznają zagrożenie, dzielą się, tworząc duże klony identycznych „żołnierzy”. Aby zapobiec wymknięciu się tej odpowiedzi spod kontroli, komórki T posiadają wbudowany program samodestrukcji zwany śmiercią komórkową indukowaną ponowną stymulacją (RICD). Kiedy już aktywowana komórka T zostanie silnie pobudzona ponownie przez swój główny czujnik — receptor komórkowy T (TCR) — może zostać włączony mechanizm RICD prowadzący do jej eliminacji. Pomaga to zmniejszyć armię po ustąpieniu zagrożenia i zapobiega chorobom związanym z nadmiernym gromadzeniem się limfocytów. Jednak we wczesnej fazie odpowiedzi komórki T potrzebują czasu na ekspansję, zanim droga samodestrukcji stanie się dominująca, a sposób kontroli tego timing u ludzi nie był dotąd w pełni jasny.
Zaskakująca ochronna rola „hamulca” odpornościowego
PD‑1 jest znany jako cel leków „checkpoint” stosowanych w terapii nowotworów, gdzie jego blokada może przywracać aktywność wyczerpanych komórek T w guzach. Tradycyjnie postrzegany jako cząsteczka osłabiająca aktywność T, PD‑1 jest szybko włączany, gdy ludzkie komórki T po raz pierwszy napotkają bodziec, i utrzymuje się na umiarkowanych poziomach podczas ich wczesnej ekspansji. W tym badaniu naukowcy wyizolowali ludzkie limfocyty CD4 i CD8 od zdrowych dawców, aktywowali je w hodowli i śledzili poziomy PD‑1 oraz jego partnera PD‑L1 w czasie. Stwierdzili, że PD‑1 i PD‑L1 osiągają szczyt w ciągu kilku dni od aktywacji — dokładnie wtedy, gdy komórki T się mnożą — a następnie maleją w miarę dojrzewania komórek. Gdy zespół zablokował PD‑1 lub PD‑L1 podczas wielokrotnej stymulacji, więcej komórek T ulegało śmierci, co wskazuje, że prawidłowa sygnalizacja PD‑1 rzeczywiście chroni te proliferujące komórki przed przedwczesnym RICD.
Jak PD‑1 przekształca „rozmowę” na powierzchni komórki
Aby dokładniej zbadać tę ochronę, naukowcy skonstruowali sztuczne „zastępcze” kuleczki prezentujące antygen, powlekane sygnałami aktywującymi (symulującymi receptor TCR i jego głównego pomocnika, CD28) i w niektórych przypadkach PD‑L1. Gdy proliferujące komórki T były ponownie stymulowane kuleczkami zawierającymi PD‑L1, konsekwentnie traciły znacznie mniej komórek niż po stymulacji kontrolnymi kuleczkami, a standardowe markery wczesnej i późnej apoptozy spadły do poziomów zbliżonych do wyjściowych. Ten wzrost przeżywalności zależał od ilości PD‑L1 i od umiejscowienia PD‑L1 tuż obok sygnałów aktywujących, co odzwierciedla ścisłą organizację naturalnej synapsy immunologicznej. Co ciekawe, efekt ochronny był najsilniejszy, gdy CD28 był zaangażowany jednocześnie z receptorem TCR, co sugeruje, że PD‑1 hamuje oba szlaki aktywujące jednocześnie. Bez PD‑1 CD28 zwiększał podatność na RICD, ale dodanie PD‑L1 niwelowało tę dodatkową wrażliwość.
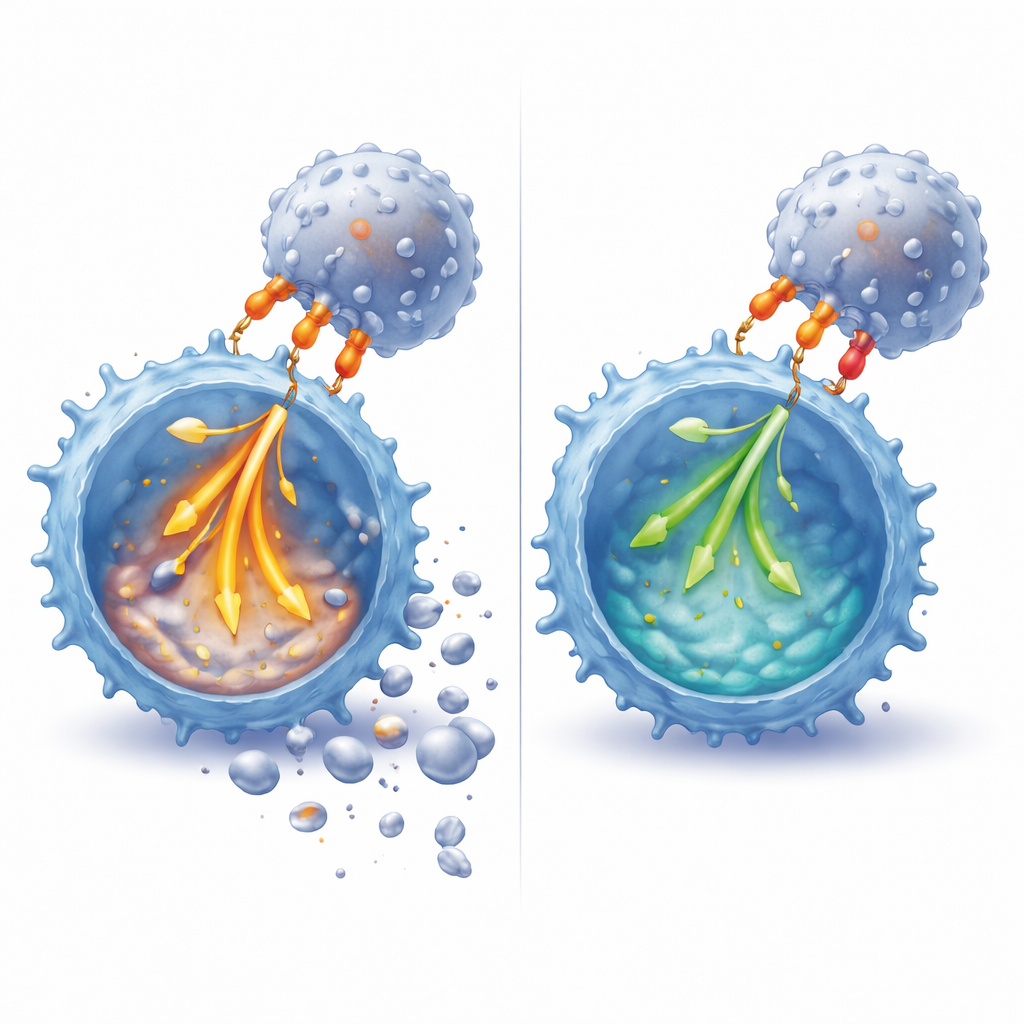
Przytłumienie sygnałów i przesunięcie molekuł przeżycia
Wnikając do wnętrza komórek, badacze odkryli, że zaangażowanie PD‑1 tłumi szeroki zakres wczesnych zdarzeń sygnałowych następujących po ponownej stymulacji komórki T. Znaczniki fosforanowe na kluczowych białkach sygnałowych — w tym na składnikach bezpośrednio związanych z receptorem oraz na centralnym enzymie przekaźnikowym ERK — były wyraźnie zredukowane w obecności PD‑L1. To stłumienie było szczególnie widoczne, gdy równocześnie zaangażowany był CD28, co odzwierciedlało większy wpływ na RICD w tym ustawieniu. Sygnalizacja PD‑1 również wpływała na cykl komórkowy, zatrzymując większą liczbę komórek w fazie kontrolnej G1 zamiast popychać je agresywnie do replikacji DNA — stanu znanego z podwyższonej wrażliwości na sygnały śmierci. Na poziomie białek PD‑1 przesuwał równowagę między molekułami pro‑zgonu i pro‑przeżyciowymi: osłabiał indukcję liganda FAS, kluczowego wyzwalacza zabijania limfocytów T, i pomagał zachować survivin, czynnik wspierający zarówno przeżycie, jak i kontrolowaną proliferację komórek T.
Co te odkrycia znaczą dla terapii i zdrowia immunologicznego
Łącznie wyniki ujawniają, że PD‑1 nie jest po prostu przełącznikiem wyłączającym komórki T, lecz subtelnym regulatorem, który chroni nowo aktywowane ludzkie limfocyty T przed przedwczesną śmiercią podczas ich ekspansji. Przez osłabianie siły powtarzanych sygnałów zarówno przez receptor TCR, jak i CD28, oraz poprzez faworyzowanie molekuł sprzyjających przeżyciu nad wyzwalaczami śmierci, PD‑1 pozwala na utworzenie silnej, a zarazem kontrolowanej armii komórek T, zanim program samodestrukcji w pełni zadziała. Dla pacjentów oznacza to, że leki blokujące PD‑1 — potężne narzędzia w onkologii — mogą także zwiększać podatność niektórych komórek T na RICD, potencjalnie zmieniając równowagę układu odpornościowego lub przyczyniając się do działań niepożądanych. Przyszłe terapie i zabiegi komórkowe, takie jak CAR‑T, mogą zyskać na celowym modulowaniu PD‑1 i powiązanych szlaków, by zachować wystarczającą populację długotrwałych, skutecznych komórek T przy jednoczesnym zapobieganiu szkodliwej nadaktywności układu odpornościowego.
Cytowanie: Lee, K.P., Elster, S., Epstein, B. et al. PD-1 protects expanding human T cells from premature restimulation-induced cell death by modulating TCR and CD28 signaling. Cell Death Dis 17, 272 (2026). https://doi.org/10.1038/s41419-026-08530-6
Słowa kluczowe: sygnalizacja PD-1, przetrwanie limfocytów T, punkty kontrolne odporności, aktywacja-indukowana śmierć komórkowa, immunoterapia przeciwnowotworowa