Clear Sky Science · pl
Sygnał leptyny‑LEPR w szpiku przestawia mitochondrialny metabolizm tlenowy, nadając oporność na chemioterapię w ostrej białaczce szpikowej
Dlaczego tłuszcz w szpiku kostnym ma znaczenie dla leczenia białaczki
Wielu ludzi wie, że tkanka tłuszczowa wpływa na choroby takie jak cukrzyca czy choroby serca, ale niewielu zdaje sobie sprawę, że tłuszcz ukryty wewnątrz kości może także modyfikować odpowiedź nowotworów krwi na leczenie. W niniejszym badaniu analizowano, jak hormon produkowany przez komórki tłuszczowe — leptyna — chroni komórki ostrej białaczki szpikowej (AML) przed standardową chemioterapią. Zrozumienie tego ukrytego mechanizmu ochronnego może wskazać nowe sposoby zwiększenia skuteczności istniejących leków.
Hormon, który przechyla szalę przeciwko chemioterapii
Naukowcy zaczęli od badania próbek szpiku kostnego u dorosłych z niedawno rozpoznaną AML. Mierzyli poziomy leptyny w szpiku i oceniali, jak dobrze pacjenci oczyszczali się z komórek białaczkowych po otrzymaniu powszechnie stosowanego leku cytarabiny. Pacjenci z wyższym poziomem leptyny w szpiku oraz większą liczbą receptorów leptyny na komórkach białaczkowych rzadziej odpowiadali na leczenie i mieli krótsze przeżycie. Nawet po uwzględnieniu innych czynników ryzyka, leptyna pozostawała silnym wskaźnikiem słabej odpowiedzi na chemioterapię. To sugerowało, że hormon pochodzący z tłuszczu robi więcej niż tylko odzwierciedla ciężkość choroby — jest aktywnie powiązany z opornością.
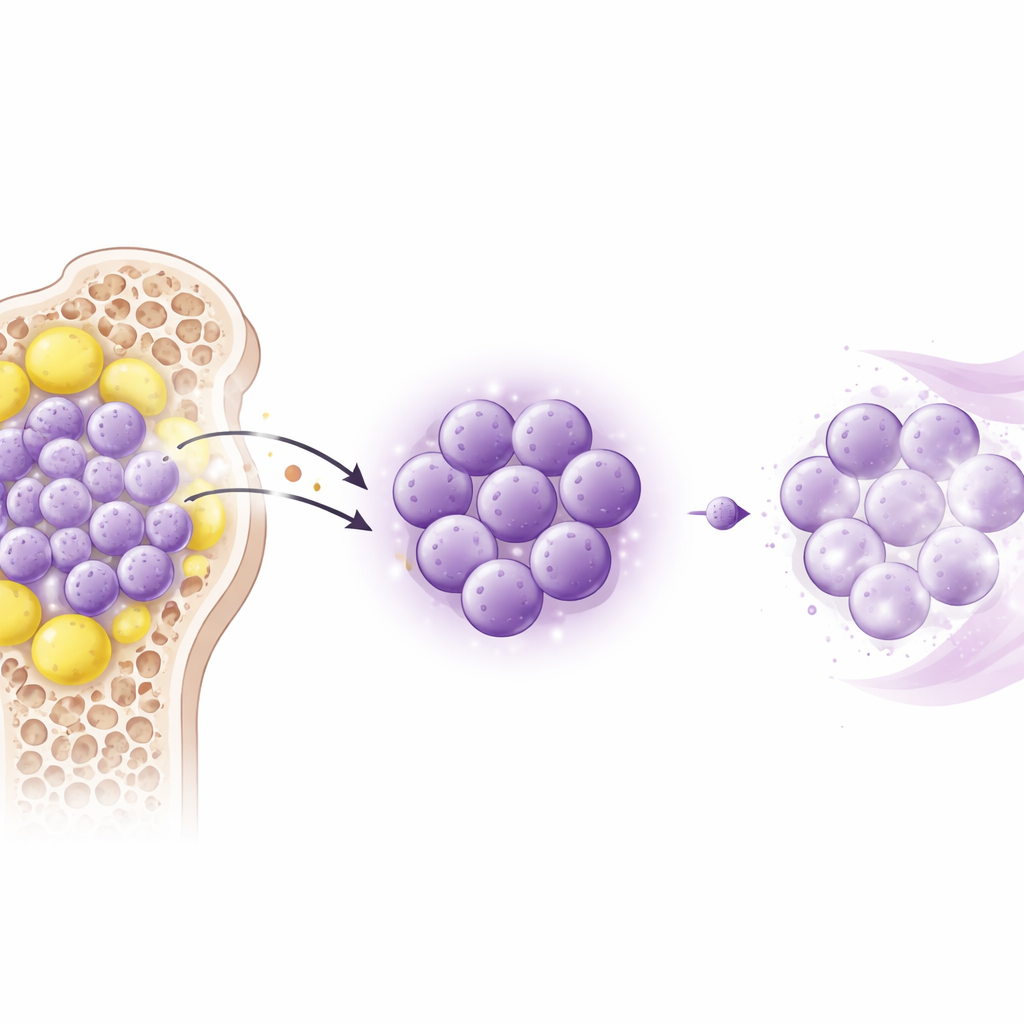
Modele zwierzęce odsłaniają ukrytą tarczę
Aby sprawdzić, czy leptyna rzeczywiście powoduje oporność na leki, zespół sięgnął po dwa modele mysie AML wiernie odwzorowujące chorobę u ludzi. Myszy otrzymywały cytarabinę samotnie, cytarabinę wraz z dodatkiem leptyny albo cytarabinę razem z małym peptydem blokującym receptor leptyny. Dodanie leptyny skróciło przeżycie, powiększyło śledzionę i wątrobę oraz pozwoliło komórkom białaczkowym zalać te narządy pomimo chemioterapii. Natomiast blokada receptora sama w sobie nie spowalniała wzrostu białaczki, ale znacząco wzmocniła działanie cytarabiny, zmniejszając rozmiary zajętych narządów i obciążenie nowotworowe. Wyniki te pokazują, że główny efekt leptyny nie polega na bezpośrednim przyspieszaniu rozrostu nowotworu, lecz na utrudnianiu eliminacji komórek białaczkowych przez chemioterapię.
Rozkręcanie „elektrowni” komórkowej
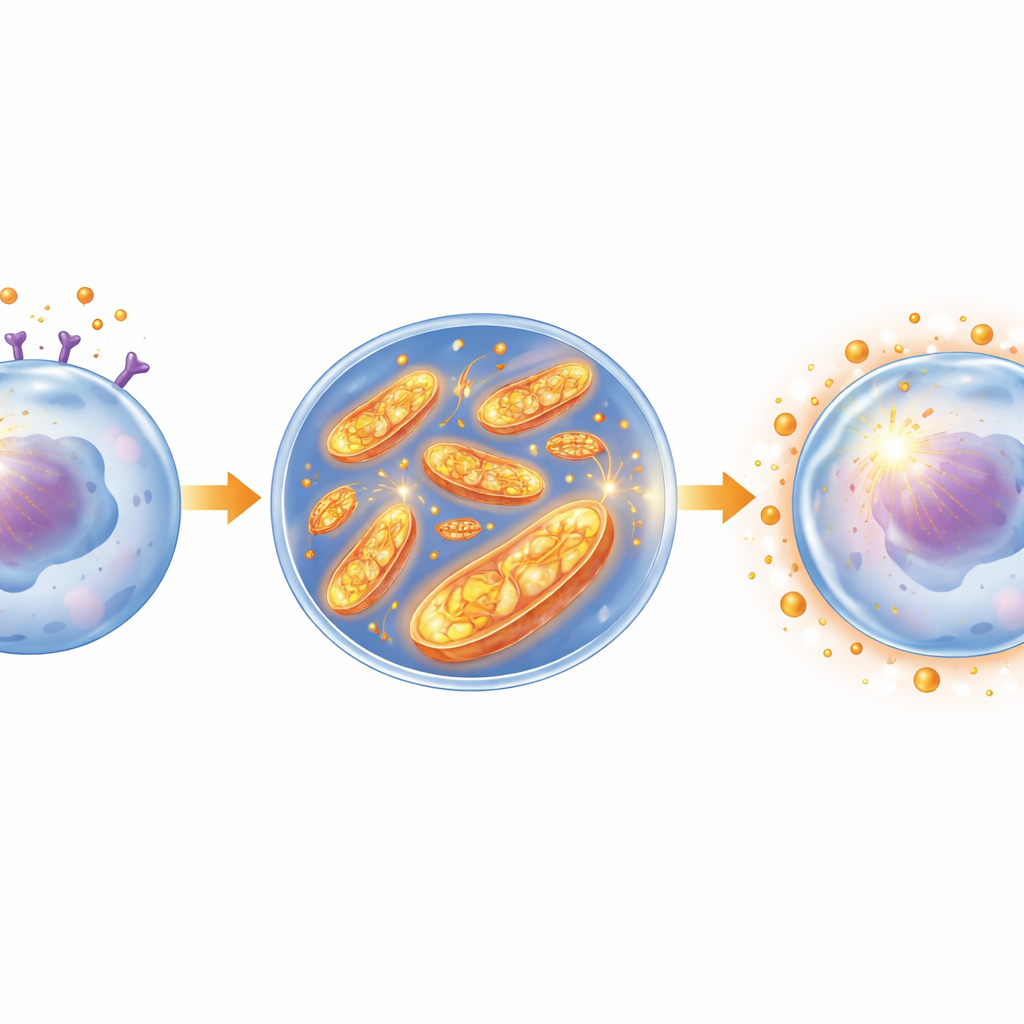
Głębiej badacze zbadali, jak leptyna zmienia metabolizm komórek białaczkowych. Odkryli, że leptyna uruchamia wewnątrzkomórkowy szlak sygnałowy JAK2/STAT3, który z kolei napędza mitochondria — maleńkie elektrownie produkujące energię. Zarówno w mysich komórkach białaczkowych, jak i w ludzkich liniach AML, leptyna zwiększała aktywność jednego kluczowego elementu mitochondrialnego, kompleksu I, i podnosiła ogólny metabolizm tlenowy. Ta zmiana generowała więcej reaktywnych form tlenu wewnątrz mitochondriów. Paradoksalnie, zamiast uszkadzać komórki, przewlekły wzrost tych reaktywnych cząsteczek wywoływał odpowiedź adaptacyjną: komórki białaczkowe zwiększały swoje mechanizmy antyoksydacyjne, takie jak glutation i enzymy detoksyfikujące, tworząc potężną wewnętrzną tarczę.
Kiedy stres staje się zbroją
Zespół wykazał, że ta tarcza jest kluczowa dla oporności na chemioterapię. Komórki białaczkowe traktowane leptyną wykazywały większą całkowitą pojemność antyoksydacyjną i były mniej wrażliwe na cytarabinę oraz inny lek, daunorubicynę. Usunięcie receptora leptyny za pomocą edycji genów osłabiło tę sieć antyoksydacyjną, obniżyło poziomy cząsteczek ochronnych i uczyniło komórki znacznie bardziej podatnymi na leczenie, nawet bez obecności leptyny. Dodatkowe eksperymenty potwierdziły, że ostry wyrzut stresu mitochondrialnego może również uruchomić podobny program ochronny, podczas gdy odsysanie tych reaktywnych cząsteczek rozbijało tarczę i przywracało wrażliwość na leki. Co ważne, blokada sygnalizacji JAK2/STAT3 lub samego receptora leptyny zapobiegała aktywacji kompleksu I, zmniejszała sygnały stresu mitochondrialnego, załamywała barierę antyoksydacyjną i ponownie umożliwiała skuteczność chemioterapii.
Wykorzystanie słabości jako nowego kierunku terapii
Dla pacjentów przesłanie badania jest takie, że komórki białaczkowe mogą wykorzystywać hormon produkowany przez pobliskie komórki tłuszczowe, by przetrwać chemioterapię. Leptyna ze szpiku kostnego wiąże się z receptorem na komórkach białaczkowych, przestawia ich mitochondria na wysoki poziom produkcji energii i wykorzystuje wynikający z tego niskopoziomowy stres do uruchomienia antyoksydacyjnej siatki bezpieczeństwa. Ta siatka chroni komórki przed silniejszymi uszkodzeniami wywoływanymi przez leki przeciwnowotworowe. Blokując receptor leptyny lub jego szlaki sygnałowe, lekarze mogą w przyszłości zdołać zdjąć tę ochronę i pozwolić istniejącym chemioterapiom działać zgodnie z zamierzeniem, bez konieczności zwiększania dawek leków. W ten sposób lepsze zrozumienie, jak tłuszcz w szpiku komunikuje się z komórkami białaczkowymi, może bezpośrednio przełożyć się na trwalsze remisje u osób z AML.
Cytowanie: Liao, X., Dai, W., Xu, X. et al. Marrow leptin-LEPR signaling rewires mitochondrial oxidative metabolism to confer chemoresistance in acute myeloid leukemia. Cell Death Dis 17, 249 (2026). https://doi.org/10.1038/s41419-026-08528-0
Słowa kluczowe: ostra białaczka szpikowa, leptyna, oporność na chemioterapię, mitochondria, stres oksydacyjny