Clear Sky Science · pl
Jądrowa miozyna 1 łączy architekturę genomu z przebudową tkanki tłuszczowej, zapaleniem metabolicznym i otyłością u myszy
Dlaczego szkielet komórki ma znaczenie dla tkanki tłuszczowej
Otyłość często przypisuje się temu, co jemy i ile się ruszamy, ale głęboko wewnątrz komórek sposób pakowania i odczytu DNA również może przechylić szalę. Badanie to ujawnia, że mały białkowy motor — jądrowa miozyna 1 (NM1), która pomaga organizować DNA w jądrze komórkowym — odgrywa zaskakującą rolę w powstawaniu komórek tłuszczowych, magazynowaniu energii i wywoływaniu zapalenia. Analiza myszy pozbawionych tego białka wykazała bezpośrednie powiązanie między fizyczną architekturą naszych genów a rozwojem niezdrowego tłuszczu trzewnego i zaburzeń metabolicznych.
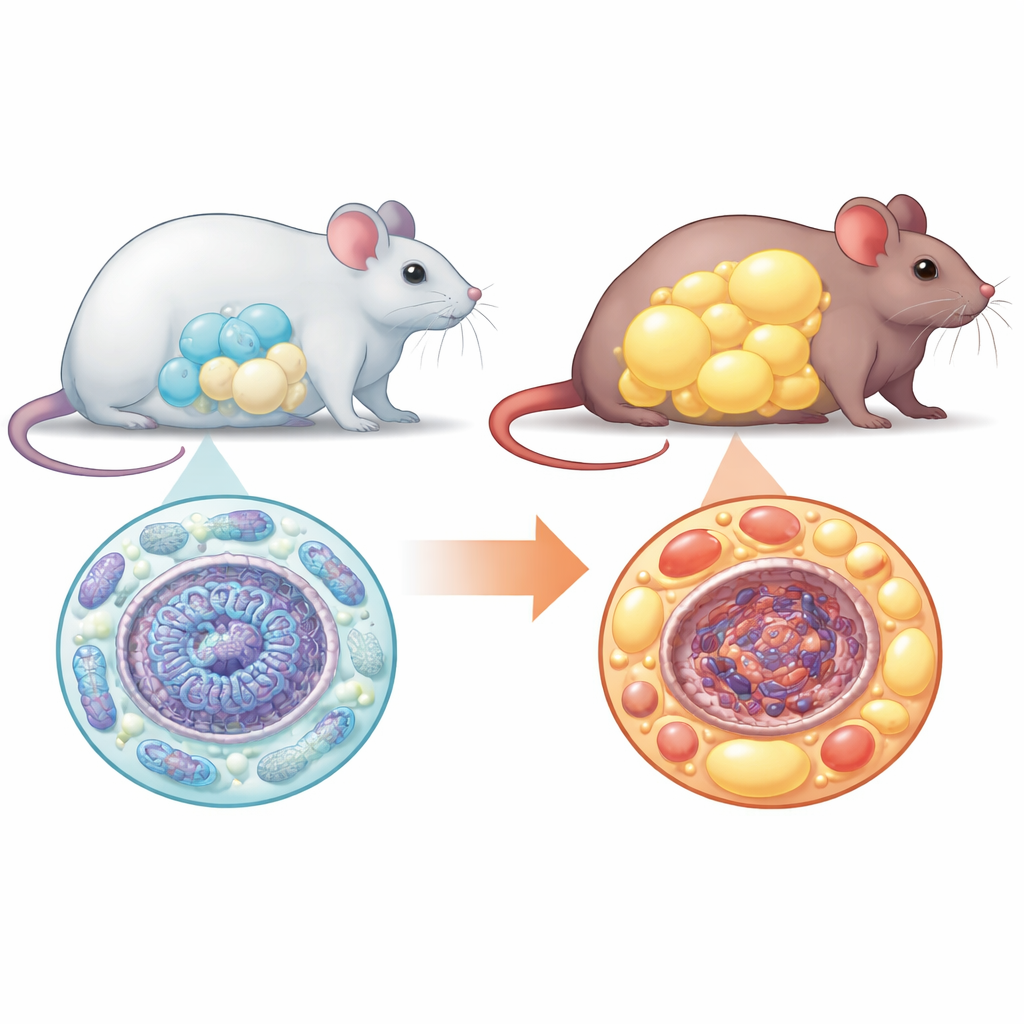
Od komórek macierzystych do adipocytów
Komórki tłuszczowe rozwijają się z wszechstronnych prekursorów zwanych mezenchymalnymi komórkami macierzystymi. Zwykle te prekursory dzielą się, zmieniają sposób wykorzystania energii i dojrzewają do wielu małych, dobrze funkcjonujących adipocytów, które bezpiecznie magazynują nadmiar kalorii. Zespół odkrył, że bez NM1 ten uporządkowany proces się załamuje. Gdy hodowali komórki macierzyste pochodzące od myszy normalnych i pozbawionych NM1 w warunkach sprzyjających tworzeniu adipocytów, znacznie mniej komórek ukończyło przejście w przypadku braku NM1. Komórki, które dojrzały, były wyraźnie większe niż normalnie, wypełnione tłuszczem, ale pozbawione typowych cech zdrowych adipocytów na poziomie genów i białek. Ten wzorzec — mniej komórek, ale każda powiększona — jest znamienny dla niezdrowej tkanki tłuszczowej.
Jak upakowanie genów kształtuje zachowanie adipocytów
NM1 działa w jądrze komórkowym, gdzie pomaga utrzymywać fragmenty DNA w stanie dostępnym, aby ważne geny mogły zostać włączone. Aby zrozumieć, jak jego utrata zmienia zachowanie komórek, badacze nałożyli mapy otwartych regionów DNA na pomiary aktywności genów w komórkach z NM1 i bez niego. Zaobserwowali, że wiele genów niezbędnych do tworzenia adipocytów, obsługi kropli tłuszczu i utrzymania mitochondriów straciło zarówno dostępność, jak i aktywność w przypadku braku NM1. Jednocześnie inne geny powiązane ze szlakami wzrostu i sygnalizacji stały się bardziej otwarte i aktywne. Wskazuje to na rolę NM1 jako kluczowego kontrolera ruchu: pomaga utrzymać zrównoważony krajobraz otwartych i zamkniętych regionów DNA, tak aby odpowiednie sieci genów kierowały zdrowym rozwojem adipocytów i metabolizmem.
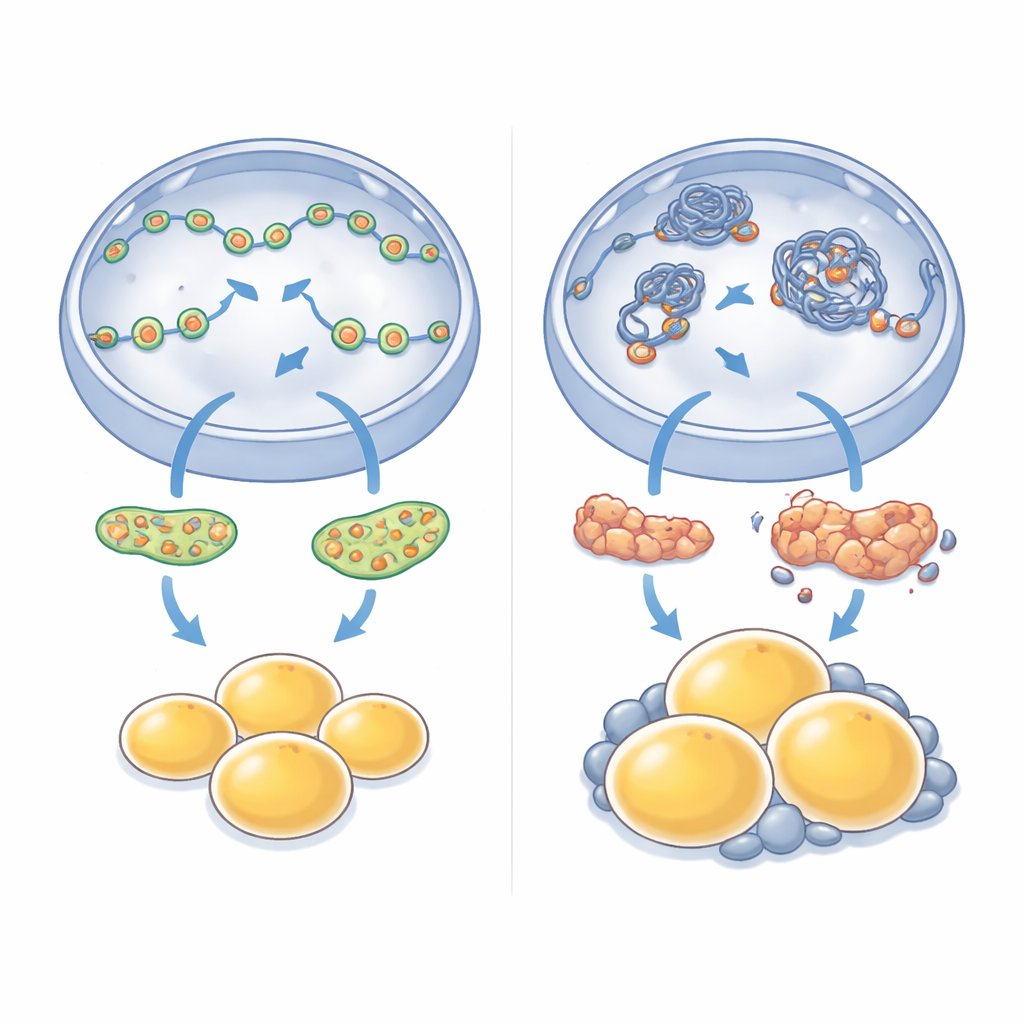
Gdy lokalne zmiany prowadzą do przyrostu masy ciała
Konsekwencje utraty tego pojedynczego jądrowego motoru nie pozostały ograniczone do komórek w probówce. Myszy pozbawione NM1 stopniowo stawały się cięższe od swoich normalnych miotów, mimo że nie jadły więcej. Badania obrazowe i analiza tkanek wykazały wyraźne nagromadzenie tłuszczu, szczególnie wokół narządów wewnętrznych w jamie brzusznej, a poszczególne adipocyty w tych obszarach były uderzająco powiększone. Gdy badacze zmierzyli, które geny były w tym tłuszczu trzewnym włączone lub wyciszone, znaleźli szeroko zakrojone zmiany: szlaki związane z wykorzystaniem energii, sygnalizacją insuliny i przebudową tkanki zostały przeprogramowane. Geny związane ze wzrostem i rozszerzaniem adipocytów często były wzmocnione, podczas gdy kilka centralnych regulatorów zdrowego tworzenia adipocytów zostało stłumionych, co odzwierciedla defekty widziane w hodowanych komórkach macierzystych.
Zapalony tłuszcz i zaburzone „silniki” energetyczne
Poza samym rozmiarem, tkanka tłuszczowa u myszy bez NM1 wykazywała oznaki zapalenia i stresu metabolicznego. Szczegółowa analiza szlaków uwypukliła silną aktywację sygnałów immunologicznych prowadzonych przez cząsteczki takie jak interferon gamma i czynnik martwicy nowotworów, które są znane z przyczyniania się do insulinooporności i chorób metabolicznych. Jednocześnie regulatory sprzyjające spokojnej, energooszczędnej tkance tłuszczowej zostały stłumione. Badanie powiązało także utratę NM1 z zaburzonymi mitochondriami — „silnikami” energetycznymi komórki. Geny, które normalnie nadzorują kontrolę jakości mitochondriów i przełączanie między wydajną produkcją energii a szybkim metabolizmem glikolitycznym, były niewłaściwie regulowane, co sugeruje, że w przypadku braku NM1 adipocyty przyjmują mniej efektywną, bardziej podatną na stres strategię energetyczną.
Wspólne sygnały u myszy i ludzi
Aby sprawdzić, czy ta ścieżka jądrowego motoru może mieć znaczenie u ludzi, autorzy przeanalizowali duże zbiory danych genetycznych pochodzących z ludzkiego tłuszczu trzewnego. Skoncentrowali się na ludzkim odpowiedniku NM1, zwanym MYO1C, i zbadali sieci wariantów, które modulują aktywność pobliskich genów. Stwierdzili, że wiele tych samych motywów obserwowanych u myszy — kontrola cytoszkieletu, sygnalizacja immunologiczna i regulacja metaboliczna — pojawia się w ludzkich sieciach genowych skupionych wokół MYO1C. Kilka genów zmienionych w tłuszczu myszy pozbawionym NM1 było również osadzonych w tych ludzkich sieciach i wiązano je z przebudową tkanki tłuszczowej i metabolizmem. To pokrywanie się między gatunkami sugeruje, że podobne mechanizmy jądrowe mogą wpływać na ryzyko otyłości u ludzi.
Co to oznacza dla otyłości i zdrowia metabolicznego
Podsumowując, praca pokazuje, że NM1 jest znacznie więcej niż pomocnikiem jądrowym; jest centralnym węzłem łączącym organizację DNA z tym, jak adipocyty rosną, magazynują energię i komunikują się z układem odpornościowym. Gdy brak NM1, przełączniki genów w prekursorach tłuszczu są ustawione nieprawidłowo, mitochondria działają słabo, adipocyty powiększają się zamiast mnożyć, a tłuszcz trzewny ulega zapaleniu — kombinacja przypominająca niezdrową tkankę tłuszczową obserwowaną w otyłości i insulinooporności. Dla czytelnika niebędącego specjalistą przesłanie jest takie, że fizyczne rozmieszczenie DNA i jego pomocników w jądrze może predysponować tkanki do zdrowego lub szkodliwego rozszerzania tłuszczu. Białka takie jak NM1 i jego ludzki odpowiednik MYO1C mogą kiedyś stać się celami terapii mających na celu przebudowę tkanki tłuszczowej „od środka”, oferując bardziej precyzyjne podejście do zwalczania chorób związanych z otyłością.
Cytowanie: Khalaji, S., Venit, T., Lukáčová, Z. et al. Nuclear Myosin 1 links genomic architecture to adipose tissue remodeling, metabolic inflammation and obesity in mice. Cell Death Dis 17, 270 (2026). https://doi.org/10.1038/s41419-026-08525-3
Słowa kluczowe: adipogeneza, chromatyna, mitochondria, tłuszcz trzewny, zapalenie metaboliczne