Clear Sky Science · pl
Makrofagi M2 sprzyjają przerzutom do węzłów chłonnych przez regulację translokacji jądrowej PKM2 w raku piersi potrójnie ujemnym
Dlaczego te badania są ważne
Dla osób z rozpoznaniem raka piersi potrójnie ujemnego jednym z największych obaw jest rozsiew nowotworu do pobliskich węzłów chłonnych, co stanowi kluczowy krok w kierunku uogólnienia choroby. Badanie to analizuje, jak pewne komórki układu odpornościowego, które powinny nas chronić, zamiast tego pomagają temu typowi raka piersi w inwazji układu limfatycznego, oraz identyfikuje molekularny „przełącznik”, który można by celować lekami, by spowolnić lub zatrzymać to rozsiewanie.
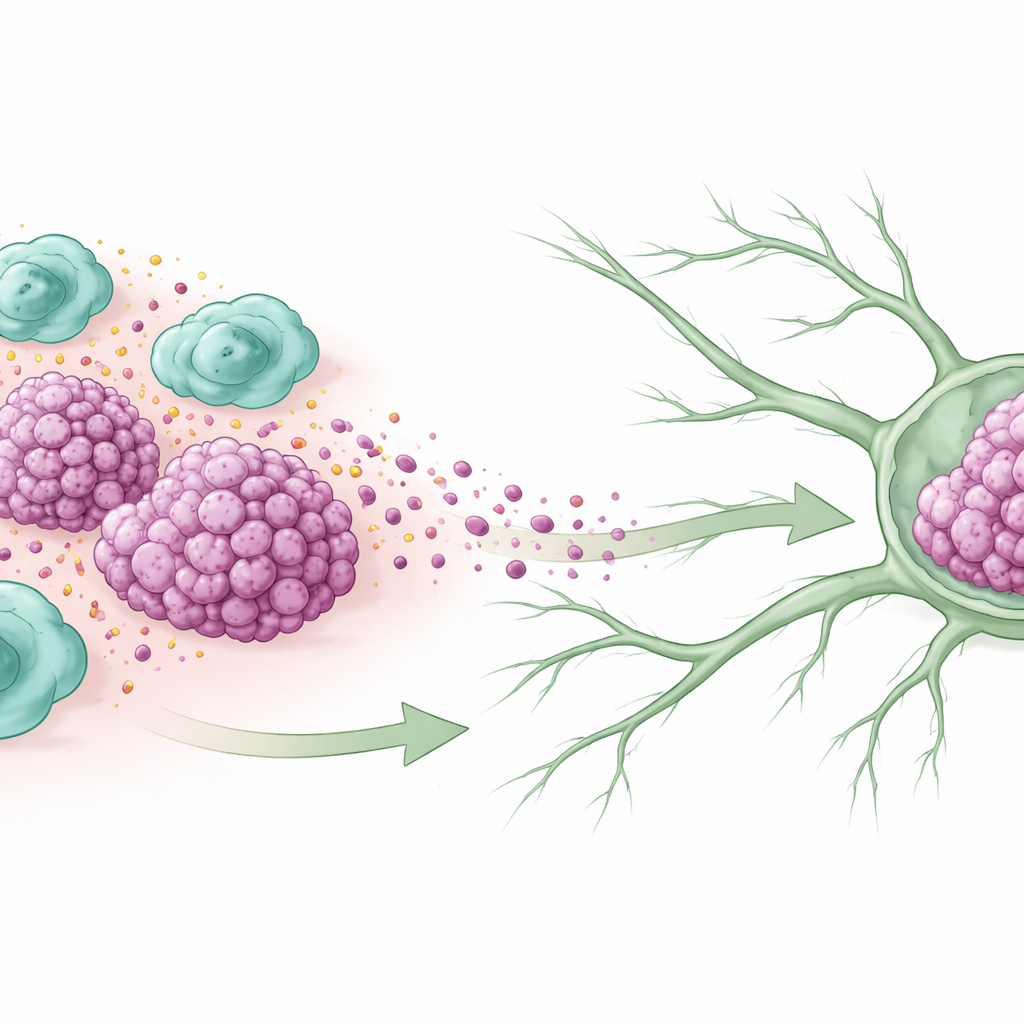
Pomocnicy odpornościowi zmieniający się w wspólników
W wielu guzach gromadzą się komórki odpornościowe zwane makrofagami. Część z nich przyjmuje przeciwzapalny, naprawczy stan zwany M2, który w kontekście nowotworu często zamiast walczyć z guzem — mu pomaga. Badacze przebadali tkanki od kobiet z rakiem piersi potrójnie ujemnym i stwierdzili, że guzy, które już rozsiewały do węzłów chłonnych, zawierały znacznie więcej makrofagów typu M2. Pacjentki, których guzy były obfitujące w te komórki, miały zwykle większe guzy, bardziej agresywne cechy i krótszy czas przeżycia, co sugeruje, że te „przyjazne” komórki odpornościowe ściśle wiążą się z pogorszeniem choroby.
Budowanie nowych „autostrad” limfatycznych dla komórek nowotworowych
Komórki nowotworowe rzadko trafiają do węzłów chłonnych przypadkowo; często podróżują wzdłuż nowo utworzonych naczyń limfatycznych, drobnych kanalików odprowadzających płyn z tkanek. W tym badaniu guzy bogate w makrofagi M2 miały również więcej naczyń limfatycznych przecinających tkankę. W hodowlach komórkowych, gdy komórki raka piersi były hodowane w obecności makrofagów M2, uwalniały sygnały, które powodowały, że ludzkie komórki limfatyczne tworzyły sieci rurkowate i szybciej migrowały, naśladując wzrost nowych kanałów limfatycznych. U myszy komórki nowotworowe uprzednio eksponowane na makrofagi M2 wytwarzały więcej naczyń limfatycznych w guzie i częstsze przerzuty do pobliskich węzłów chłonnych, potwierdzając, że te komórki odpornościowe aktywnie pomagają budować drogi ucieczki.
Ukryty łańcuch sygnałów wewnątrz komórek nowotworowych
Zespół pytał następnie, jakie komunikaty chemiczne wysyłają makrofagi M2, by skłonić guzy do rozsiewu limfatycznego. Wskazali na dobrze znaną cząsteczkę TGF-β, wydzielaną w większych ilościach przez makrofagi M2. Ten sygnał powodował, że komórki raka piersi zwiększały produkcję dwóch czynników wzrostu, VEGFC i VEGFD, które są silnymi driverami wzrostu naczyń limfatycznych. Kluczowe było wykazanie, że enzym metaboliczny w komórkach nowotworowych, PKM2, pełni rolę centralnego przełącznika w tym procesie. Pod wpływem TGF-β PKM2 nie tylko zwiększa aktywność metabolizmu glukozy, ale również ulega modyfikacjom chemicznym i przemieszcza się do jądra, gdzie pomaga w włączaniu genów VEGFC i VEGFD. Bez PKM2, lub gdy zablokowano jego wejście do jądra, komórki nowotworowe wytwarzały znacznie mniej tych sygnałów stymulujących rozwój naczyń limfatycznych i miały mniejszą zdolność do ich indukowania.
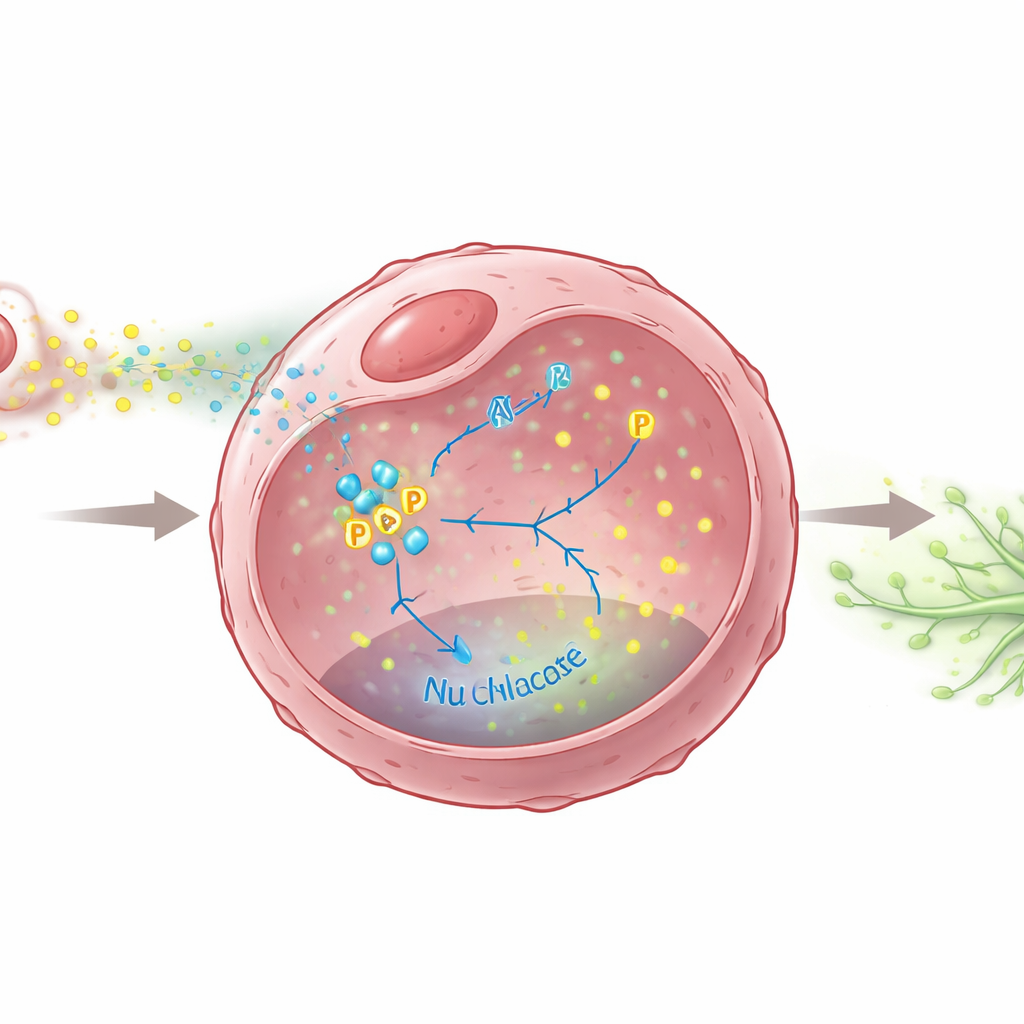
Testowanie możliwego hamulca rozsiewu
Ponieważ PKM2 leży w tym kluczowym miejscu łączącym zmieniony metabolizm i pro‑przerzutowe sygnalizowanie, naukowcy sprawdzili, czy jego zablokowanie może spowolnić rozsiew limfatyczny. Użyli shikoniny, związku, który zakłóca aktywację PKM2 i jego wejście do jądra. W eksperymentach komórkowych shikonina silnie zmniejszyła poziomy VEGFC i VEGFD oraz osłabiła zdolność wydzielin komórek nowotworowych do wywoływania wzrostu i migracji naczyń limfatycznych. W modelach mysich leczenie shikoniną zmniejszyło liczbę i rozmiar przerzutów do węzłów chłonnych oraz gęstość naczyń limfatycznych w guzach, bez oczywistych toksycznych efektów u zwierząt. Wyniki te sugerują, że blokowanie PKM2 może jednocześnie pozbawić komórki nowotworowe niektórych metabolicznych korzyści i osłabić ich zdolność do przebudowy sieci limfatycznej na swoją korzyść.
Co to oznacza dla pacjentów
W sumie badanie proponuje jasny łańcuch zdarzeń: makrofagi M2 w guzach raka piersi potrójnie ujemnego wydzielają TGF-β, które przekształca PKM2 w komórkach nowotworowych w rolę podwójną — napędzając wysokie zużycie glukozy i działając w jądrze jako aktywator VEGFC i VEGFD. Te czynniki następnie stymulują wzrost naczyń limfatycznych, z których komórki nowotworowe korzystają, by dotrzeć do węzłów chłonnych i dalej. Identyfikując PKM2 jako krytyczny węzeł tego ciągu, praca wskazuje nowe sposoby przewidywania i potencjalnego leczenia rozsiewu limfatycznego, zwłaszcza u pacjentów, których guzy wykazują wysokie poziomy makrofagów M2, PKM2 lub VEGFC/D. Choć potrzebne są dalsze badania u ludzi, ukierunkowanie tej ścieżki mogłoby pomóc przekształcić układ limfatyczny z „autostrady” raka z powrotem w barierę.
Cytowanie: Yang, Y., Ye, H., Zhong, D. et al. M2 macrophages promote lymphatic metastasis by regulating PKM2 nuclear translocation in triple-negative breast cancer. Cell Death Dis 17, 262 (2026). https://doi.org/10.1038/s41419-026-08524-4
Słowa kluczowe: rak piersi potrójnie ujemny, przerzuty do węzłów chłonnych, makrofagi związane z guzem, PKM2, laktangiogeneza