Clear Sky Science · pl
Trimetyloamina lizyny 36 histonu H3 przez SETD2 kształtuje epigenetyczny krajobraz w komórkach macierzystych jelita, organizując metabolizm lipidów i łagodząc starzenie komórek
Dlaczego komórki macierzyste jelita mają znaczenie w miarę starzenia się
Głęboko w wyściółce naszych jelit niewielkie komórki macierzyste pracują bez przerwy, odnawiając tkankę odpowiadającą za trawienie i wchłanianie składników odżywczych. W miarę starzenia się organizmu te komórki wyczerpują się, co czyni jelito bardziej podatnym na choroby i wolniej gojącym się. W badaniu tym analizowano, jak subtelne chemiczne oznaki na białkach pakujących DNA pomagają utrzymać młodość komórek macierzystych jelita, w jaki sposób ich utrata zakłóca spalanie tłuszczów wewnątrz komórek oraz jak starannie dobrane leki mogą pewnego dnia spowolnić ten spadek.
Starzejące się komórki w wymagającym środowisku
Wewnętrzna powierzchnia jelita jest jedną z najszybciej odnawiających się tkanek w organizmie. Komórki macierzyste usadowione u podstaw małych kieszonek zwanych kryptami dzielą się, by wymieniać miliardy komórek co kilka dni. Ta nieustanna praca wymaga stałego dopływu energii, w dużej mierze z rozkładu tłuszczów. Jednocześnie komórki te są sterowane przez „kod” epigenetyczny — chemiczne oznaki na histonach, które wpływają na to, które geny są aktywne, a które wyciszone. Autorzy skupili się na jednym z takich znaków, znanym jako trimetylacja H3K36, wytwarzanym przez enzym SETD2, i zastanawiali się, czy zmiany w tym znaku mogą pomóc wyjaśnić, dlaczego komórki macierzyste jelita tracą wigor z wiekiem.
Oznaka ochronna, która blednie z wiekiem
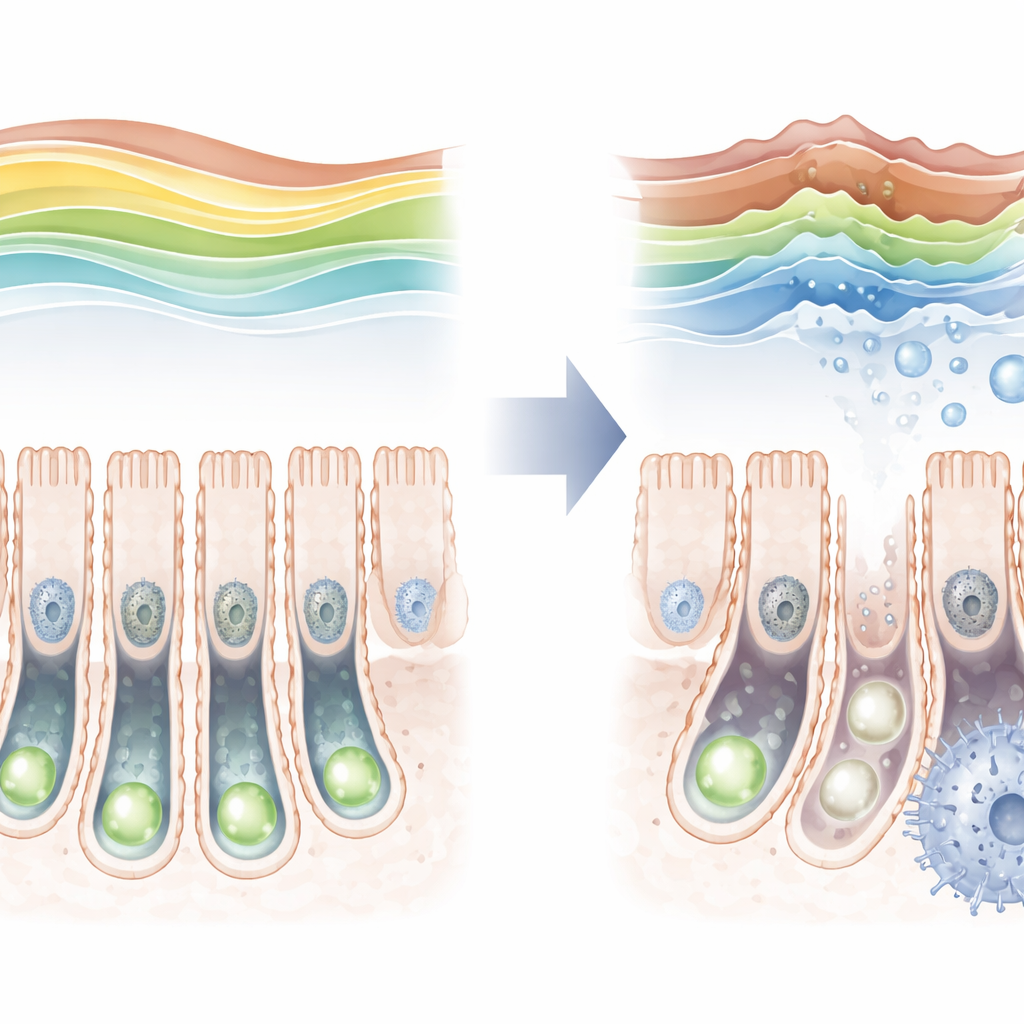
Analizując jelita myszy w różnych etapach życia, badacze odkryli, że trimetylacja H3K36 nie jest stała. Jest stosunkowo niska tuż po urodzeniu, następnie rośnie do szczytu u młodych dorosłych, po czym ponownie spada w podeszłym wieku. Wraz z obniżeniem tej oznaki u starszych zwierząt wzrastały markery starzenia komórkowego w komórkach macierzystych, co sugerowało związek między nimi. Aby to sprawdzić bezpośrednio, zespół skonstruował myszy, w których SETD2 można było usunąć tylko w komórkach macierzystych jelita. Po usunięciu tego enzymu ochronna oznaka niemal zniknęła, komórki macierzyste dzieliły się rzadziej i miały trudności z wytworzeniem pełnego spektrum wyspecjalizowanych typów komórek jelitowych.
Jak zmiany epigenetyczne psują spalanie tłuszczu
Utrata tego pojedynczego znaku histonowego wywołała kaskadę zmian w komórkach macierzystych. Pomiary aktywności genów wykazały, że wiele genów związanych z cyklem komórkowym i kopiowaniem DNA zostało wyciszonych, podczas gdy geny związane ze stresem i starzeniem się zostały włączone. Co uderzające, najsilniejszy sygnał wskazywał na zaburzenia w gospodarce lipidowej: geny normalnie wspierające utlenianie kwasów tłuszczowych — kontrolowane spalanie tłuszczów dla uzyskania energii — były stłumione, a tłuszcze zaczęły gromadzić się w kryptach. Profilowanie metabolitów potwierdziło nagromadzenie kwasów tłuszczowych o długich łańcuchach, co świadczy o zawodzeniu zwyczajowych szlaków przetwarzania tłuszczów. Jednocześnie fizyczne upakowanie DNA w jądrze uległo przesunięciu: wiele obszarów stało się bardziej odsłoniętych lub bardziej ściśle zamkniętych, przeformowując zestaw genów, do których komórka miała łatwy dostęp.
Przebudowywacze chromatyny i marsz ku senescencji
Aby zrozumieć, skąd biorą się te zmiany w pakowaniu DNA, autorzy zmapowali zarówno otwarte regiony chromatyny, jak i zestaw innych oznak histonowych w całym genomie. Gdy zniknęła trimetylacja H3K36, duże fragmenty DNA zyskały „aktywne” oznaki i stały się bardziej dostępne, szczególnie w pobliżu genów związanych z metabolizmem i starzeniem. Kluczowym graczem w tej przemianie był kompleks remodelujący chromatynę SWI/SNF, napędzany przez podjednostkę SMARCA4. W komórkach macierzystych pozbawionych SETD2 poziomy SMARCA4 wzrosły, a kompleks zdawał się pomagać rozszerzać obszary uruchamiające programy senescencji. Gdy badacze zmniejszyli aktywność SMARCA4 genetycznie lub za pomocą specyficznego inhibitora, komórki macierzyste odzyskały część zdolności do tworzenia zdrowych organoidów jelitowych in vitro, a markery starzenia zmalały — co sugeruje, że nadmierna przebudowa popycha te komórki w kierunku zmęczonego, senescentnego stanu.
Przywracanie szlaków energetycznych, by uratować komórki macierzyste
Ponieważ zaburzone spalanie tłuszczów okazało się centralnym problemem, zespół sprawdził, czy wzmocnienie tego szlaku może przeciwdziałać starzeniu komórek macierzystych. Użyli leku aktywującego PPARα, główny regulator utleniania kwasów tłuszczowych. W organoidach pochodzących z komórek macierzystych pozbawionych SETD2 to leczenie zwiększyło wzrost, przywróciło rozgałęzione struktury charakterystyczne dla żywych komórek macierzystych i zmniejszyło gromadzenie tłuszczu. U żywych myszy ta sama interwencja częściowo odnowiła pulę komórek macierzystych, obniżyła markery senescencji i znormalizowała odkładanie lipidów w kryptach jelitowych. Wyniki te wskazują, że utlenianie kwasów tłuszczowych stanowi kluczowe ogniwo między kontrolą epigenetyczną a zdrowiem komórek macierzystych.
Co to oznacza dla zdrowego starzenia się
Wszystko razem pokazuje, że specyficzny znak histonowy, nakładany przez SETD2, pomaga utrzymać zrównoważony epigenetyczny krajobraz w komórkach macierzystych jelita. Gdy ta oznaka zanika, chromatyna ulega nieprawidłowej przebudowie, szlaki spalania tłuszczów zawodzą, lipidy się kumulują, a komórki dryfują w stronę senescencji, osłabiając system naprawczy jelita. Poprzez przytłumienie nadaktywnej machiny przebudowy lub przywrócenie metabolizmu lipidów za pomocą wyspecjalizowanych leków można potencjalnie zachować funkcję komórek macierzystych i zdrowie jelit w późniejszym życiu. Choć odkrycia pochodzą od myszy, odbijają wzorce obserwowane w ludzkich chorobach jelit, co stwarza perspektywę, że precyzyjnie dobrane terapie metaboliczne mogłyby kiedyś pomóc przeciwdziałać wiekowej utracie sprawności naszych własnych komórek macierzystych jelita.
Cytowanie: Xu, Y., Wang, Z., Feng, W. et al. Histone 3 lysine 36 trimethylation by SETD2 shapes an epigenetic landscape in intestinal stem cells to orchestrate lipid metabolism and attenuate cell senescence. Cell Death Dis 17, 273 (2026). https://doi.org/10.1038/s41419-026-08518-2
Słowa kluczowe: komórki macierzyste jelita, epigenetyka, utlenianie kwasów tłuszczowych, starzenie komórkowe, SETD2