Clear Sky Science · pl
RNA powiązane z Lamp2a wydzielane przez ADSC zapobiega sprzężeniu zwrotnemu ENO1–laktylacja–glikoliza i zachowaniom złośliwym komórek w raku piersi potrójnie ujemnym
Dlaczego to ma znaczenie dla pacjentów
Rak piersi potrójnie ujemny jest jedną z najbardziej agresywnych postaci raka piersi i pozbawiony jest celów hormonalnych lub związanych z czynnikami wzrostu, które czynią inne podtypy bardziej podatnymi na leczenie. Badanie to ujawnia, jak te guzy przebudowują swój metabolizm energetyczny, by przetrwać w warunkach niskiej dostępności tlenu, i opisuje pomysłowy sposób atakowania tego układu. Dla czytelników daje to wgląd w to, jak zrozumienie metabolizmu nowotworów może prowadzić do nowych, wysoce ukierunkowanych terapii, różniących się wyraźnie od tradycyjnej chemioterapii.
Jak te guzy się zasilają
Wiele nowotworów silnie polega na szybkim, lecz mało efektywnym sposobie wytwarzania energii zwanym glikolizą, która przekształca cukier w produkt uboczny — lakton. Analizując próbki pacjentów, publiczne bazy genów i wiele linii komórkowych raka piersi, badacze wykazali, że guzy potrójnie ujemne jeszcze mocniej opierają się na glikolizie niż inne raki piersi. Kluczowy enzym w tej ścieżce, ENO1, występuje w tych nowotworach w szczególnie wysokim stężeniu i wiąże się z gorszym przeżyciem. Gdy poziomy ENO1 zostały zmniejszone w hodowanych w laboratorium komórkach potrójnie ujemnych, komórki przestawiły się z glikolizy na bardziej normalne wytwarzanie energii w mitochondriach, rosły wolniej i miały mniejszą zdolność do inwazji czy tworzenia kolonii.
Niebezpieczne sprzężenie zwrotne w komórkach nowotworowych
Pogłębiając badania, zespół odkrył, że sam lakton wzmacnia ENO1 i wpędza komórki nowotworowe w błędne koło. Lakton może chemicznie modyfikować białka w procesie zwanym laktylacją. W komórkach potrójnie ujemnych nadmiar laktonu zwiększał laktylację ENO1, co z kolei podnosiło aktywność i stabilność enzymu, przyspieszając glikolizę i wytwarzanie jeszcze większej ilości laktonu. W warunkach niskiego tlenu — typowych dla guzów litych — ten mechanizm ulegał wzmocnieniu, pomagając komórkom nowotworowym opierać się śmierci komórkowej i nadal proliferować. Blokowanie aktywności ENO1 przy pomocy inhibitora małocząsteczkowego lub redukcja produkcji laktonu osłabiały to sprzężenie, hamowały glikolizę i spowalniały wzrost guza u myszy.
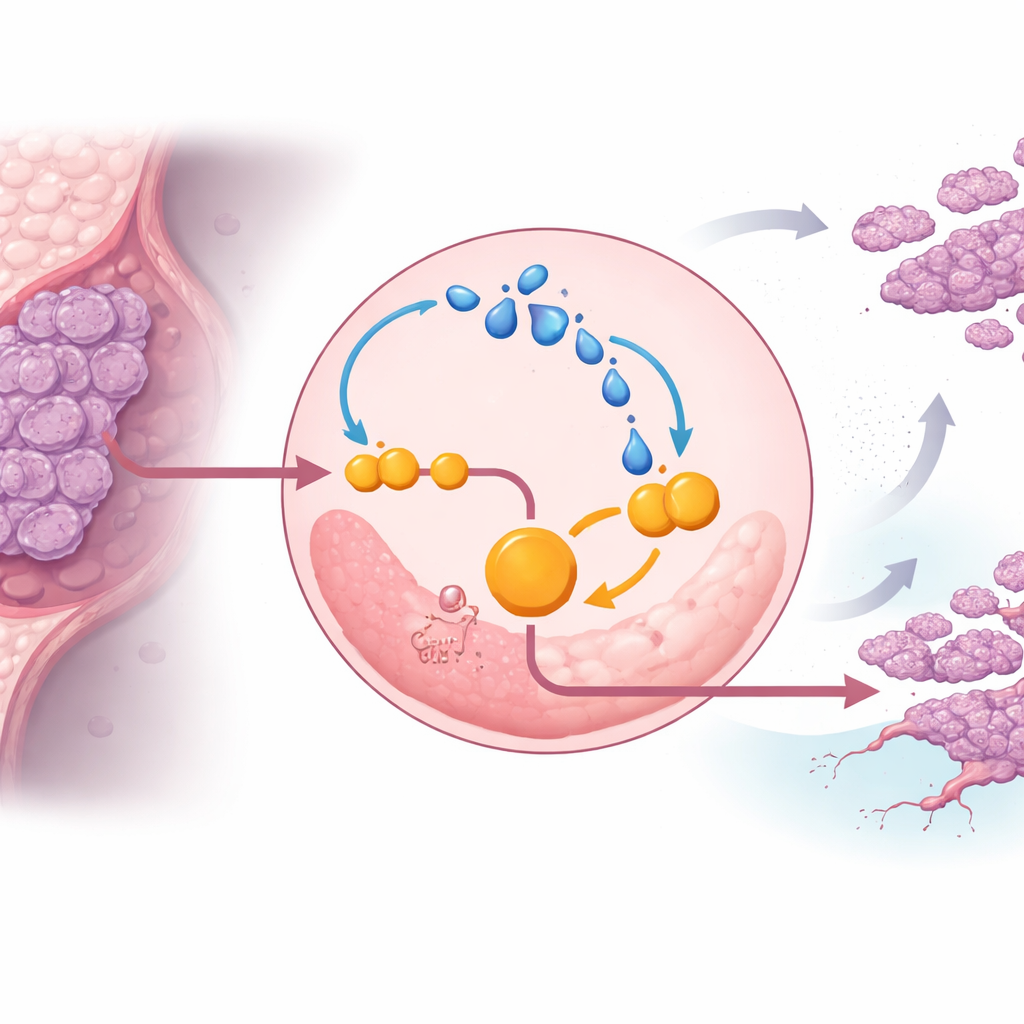
Przełącznik molekularny chroniący ENO1
W badaniu zidentyfikowano konkretne miejsce kontroli na ENO1, które umożliwia działanie tego mechanizmu. Białko znane jako EP300 dodaje znaczniki oparte na laktonie do kilku aminokwasów lizyny w ENO1, przy czym jedno miejsce, określone jako K262, okazało się kluczowe. Gdy to miejsce zostało zmienione tak, że nie mogło być laktylowane, ENO1 była szybko kierowana do komórkowych centrów recyklingu — lizosomów — i tam rozkładana. Bez tej ochronnej modyfikacji komórki potrójnie ujemne traciły dużą część swojego napędu glikolitycznego oraz zdolności do tworzenia guzów i przerzutów w modelach zwierzęcych. Wyróżnia to laktylację ENO1 w pozycji K262 jako molekularny przełącznik, który chroni enzym przed zniszczeniem i podtrzymuje zmieniony metabolizm nowotworu.
Nowy sposób oznaczania ENO1 do zniszczenia
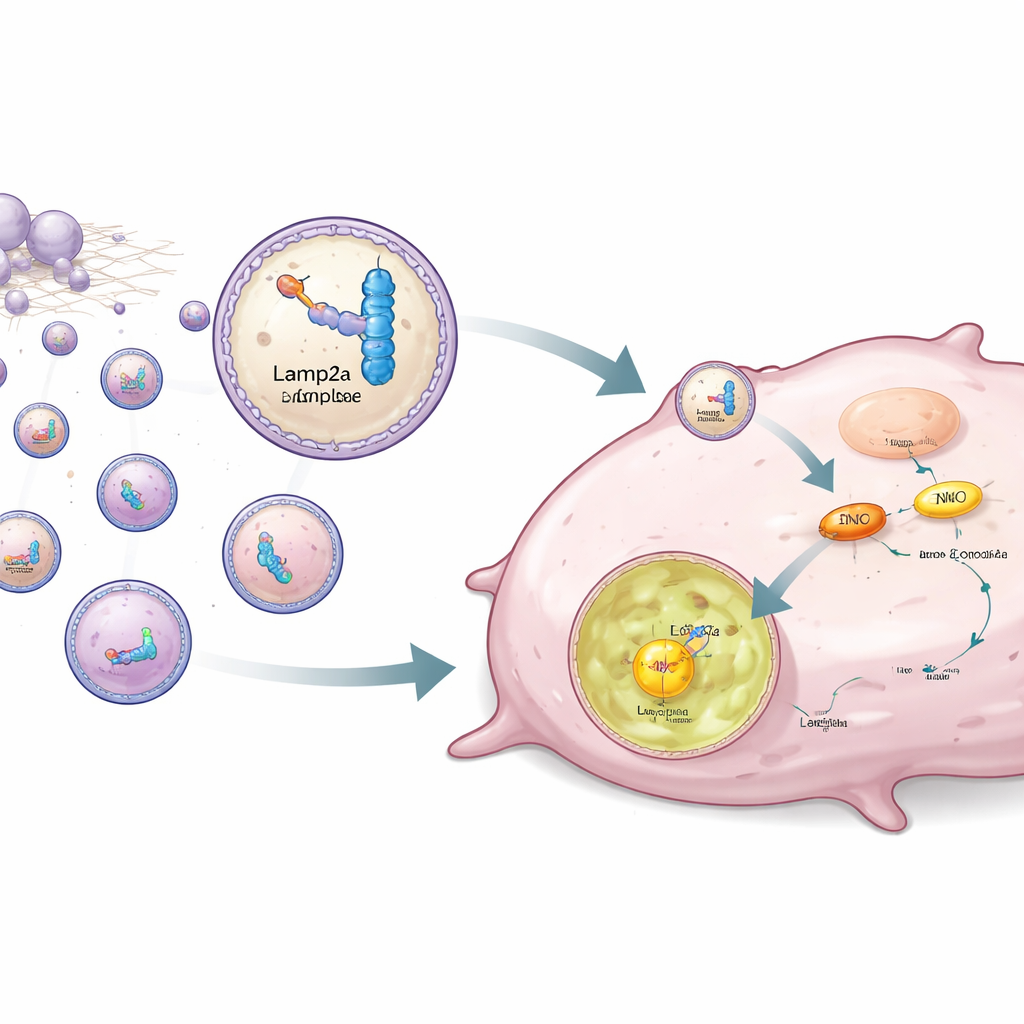
Zamiast jedynie blokować ENO1, autorzy opracowali strategię selektywnego usuwania go z komórek nowotworowych. ENO1 działa także jako białko wiążące RNA, rozpoznające określone krótkie sekwencje RNA. Zespół skonstruował syntetyczne fragmenty RNA, które silnie wiążą ENO1, a następnie połączył je z Lamp2a — białkiem błony lizosomalnej zaangażowanym w ukierunkowane rozkładanie białek. Ludzka tkanka tłuszczowa będąca źródłem komórek macierzystych została zmodyfikowana genetycznie tak, by produkować tę parę RNA–Lamp2a i pakować ją do małych pęcherzyków zwanych egzosomami. Gdy te zmodyfikowane egzosomy dodano do komórek potrójnie ujemnych, część RNA przyczepiła się do ENO1, a część Lamp2a skierowała cały kompleks do lizosomów, gdzie ENO1 był degradowany nawet jeśli posiadał stabilizującą laktylację.
Testowanie podejścia ukierunkowanego rozkładu u zwierząt
Aby przybliżyć ten pomysł do praktycznej terapii, badacze hodowali zmodyfikowane komórki macierzyste na biodegradowalnym rusztowaniu i wszczepili ten konstrukcja pod skórę myszy, w pobliżu guzów potrójnie ujemnych. Z tej lokalizacji komórki macierzyste stale uwalniały egzosomy niosące kompleksy celujące w ENO1. Guzy u tych myszy wykazywały wyraźnie niższe poziomy białka ENO1, ograniczoną glikolizę, mniej dzielących się komórek i więcej oznak śmierci komórkowej w porównaniu z osobnikami kontrolnymi. Guzy rosły wolniej, a ich złośliwe zachowanie zostało wyraźnie osłabione, co pokazuje, że kierowanie ENO1 do lizosomów może skutecznie pozbawić nowotwór preferowanej ścieżki energetycznej.
Co to może oznaczać dla przyszłego leczenia
Dla odbiorcy niebędącego specjalistą najważniejszy wniosek jest taki, że praca ta ujawnia zarówno słabość, jak i potencjalny nowy kierunek leczenia raka piersi potrójnie ujemnego. Słabością jest zależność guza od samonapędzającej pętli energetycznej skoncentrowanej wokół ENO1 i laktonu, szczególnie w obszarach o niskim poziomie tlenu. Kierunkiem terapeutycznym jest system ukierunkowanego rozkładu białek wykorzystujący niestandardowe RNA i egzosomy pochodzące z komórek macierzystych, by sprowadzić ENO1 do komórkowych mechanizmów utylizacji. Choć droga do zastosowań klinicznych jest długa, podejście to ilustruje, jak dogłębne zrozumienie metabolicznych sztuczek nowotworu może zainspirować precyzyjne terapie mające na celu unieszkodliwienie, zamiast jedynie zatruć, komórki złośliwe.
Cytowanie: Cheng, S., Xia, B., Li, L. et al. A Lamp2a-linked RNA secreted by ADSCs prevents ENO1–lactylation–glycolysis feedback and cell malignant behavior in triple-negative breast cancer. Cell Death Dis 17, 288 (2026). https://doi.org/10.1038/s41419-026-08517-3
Słowa kluczowe: rak piersi potrójnie ujemny, metabolizm nowotworu, sygnalizacja laktem, ukierunkowane rozkładanie białek, enzym ENO1