Clear Sky Science · pl
Fosfataza Shp1 reguluje stabilność białka CXCR2 i inwazyjność zależną od IL8 w raku piersi
Dlaczego te badania mają znaczenie dla raka piersi
Rak piersi pozostaje jedną z głównych przyczyn zgonów z powodu nowotworów u kobiet, w dużej mierze dlatego, że niektóre guzy stają się inwazyjne i rozsiewają się do odległych narządów. W tym badaniu rozjaśniono, w jaki sposób powszechny w guzie sygnał zapalny, zwany IL8, komunikuje się z komórkami raka piersi oraz jak molekularny „hamulec” o nazwie Shp1 pomaga zdecydować, czy te komórki pozostaną na miejscu, czy staną się bardziej agresywne. Zrozumienie tej molekularnej rozgrywki może otworzyć nowe sposoby spowolnienia lub zatrzymania rozsiewu trudnych do leczenia nowotworów piersi, zwłaszcza potrójnie ujemnego raka.
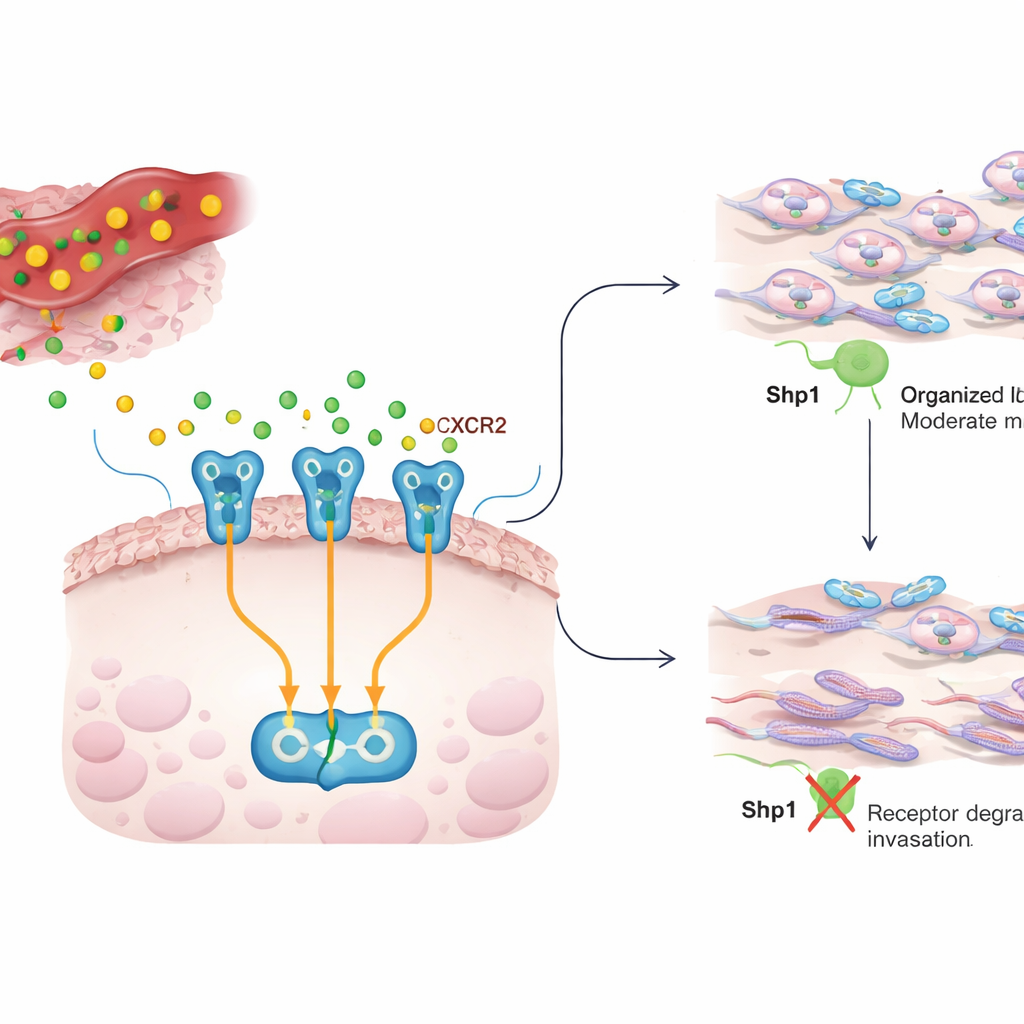
Rozmowa między zapaleniem a komórkami nowotworowymi
W obrębie guza komórki nowotworowe otoczone są przez komórki odpornościowe i podporowe, które uwalniają komunikatory chemiczne, czyli cytokiny. IL8 jest jednym z takich komunikatorów i często występuje w wysokich stężeniach w wielu nowotworach, gdzie napędza wzrost, tworzenie naczyń krwionośnych i zdolność komórek nowotworowych do przemieszczania się i inwazji. IL8 działa przez receptor na powierzchni komórki nowotworowej zwany CXCR2. Gdy IL8 wiąże się z CXCR2, uruchamia kilka wewnętrznych szlaków, które reorganizują cytoszkielet komórki, ułatwiając jej przemieszczanie się przez tkanki i rozsiew. W niniejszej pracy badano, jak kontrolowana jest ta rozmowa IL8–CXCR2 i czy Shp1, enzym zwykle postrzegany jako hamulec sygnałów sprzyjających rozrostowi, również kształtuje zachowania inwazyjne.
Ukryta rola Shp1 w ruchu komórek
Naukowcy najpierw usunęli lub chemicznie zablokowali Shp1 w szeroko stosowanej linii komórkowej raka piersi typu luminalnego (MCF7) i zmierzyli, jak dobrze komórki migrują i inwazują przez żel naśladujący tkankę. Bez Shp1 komórki nowotworowe szybciej zamykały rany i dwukrotnie do trzykrotnie sprawniej przeciskały się przez żel, co wykazało, że Shp1 normalnie hamuje ruch. Analiza danych pacjentów wykazała także, że u kobiet, których guzy wykazywały mniejsze poziomy Shp1, przeżycie było gorsze, a czas do nawrotu krótszy. Razem te wyniki sugerują, że Shp1 ogranicza agresywne zachowanie komórek raka piersi, a utrata tego hamulca wiąże się z gorszymi wynikami.
Jak IL8 przełącza Shp1 i reprogramuje kluczowy receptor
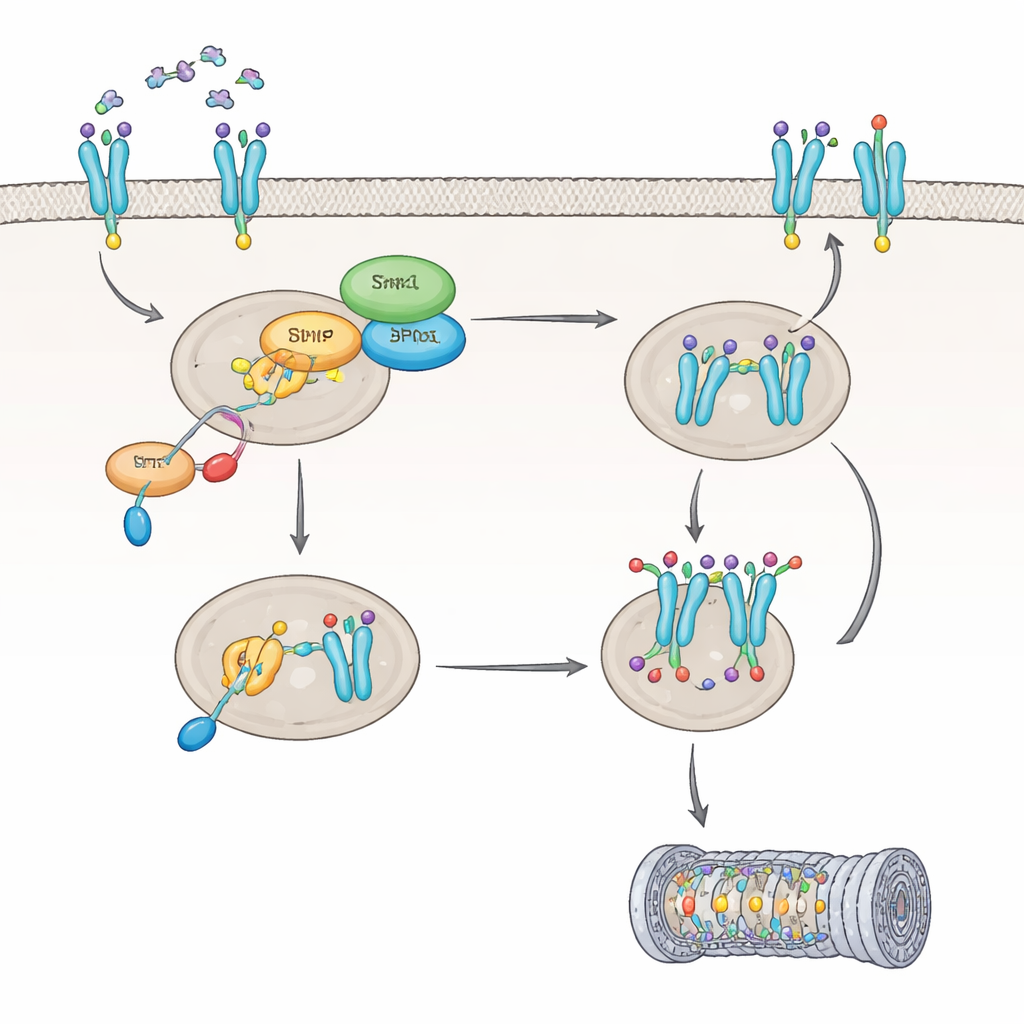
Następnie zespół badał, jak IL8 wpływa na samą Shp1. Odkryli, że IL8 aktywuje białko PKC, które oznacza Shp1 w konkretnym miejscu, obniżając jego aktywność enzymatyczną o około 60 procent. Gdy Shp1 jest w ten sposób przytłumiony, inny enzym, PP2A, staje się mniej aktywny, a receptor CXCR2 pozostaje w silnie zmodyfikowanym stanie, co zmienia jego los w komórce. Zamiast być oczyszczonym i ponownie dostarczonym na powierzchnię komórki, CXCR2 zostaje oznaczony do degradacji, głównie przez aparat rozkładu białek komórkowych — proteasom. Szczególna modyfikacja CXCR2, w reszcie aminokwasowej nazwanej Ser347, okazała się kluczowa dla przyłączania znaczników degradacyjnych. W komórkach pozbawionych Shp1 CXCR2 był silniej oznakowany i rozkładany szybciej, co prowadziło do mniejszej liczby receptorów na powierzchni komórki i osłabionej odpowiedzi na IL8 w czasie.
Różne typy raka piersi — różne połączenia sygnałowe
Rak piersi nie jest jedną chorobą; guzy klasyfikuje się na podtypy luminalny, HER2-dodatni i potrójnie ujemny na podstawie wzorców receptorowych. Badacze testowali obwód IL8–CXCR2–Shp1 w kilku liniach komórkowych reprezentujących każdy z podtypów. W komórkach luminalnych i potrójnie ujemnych IL8 uruchamiał kaskadę Shp1–PP2A–CXCR2, a blokada Shp1 zarówno zwiększała inwazyjność w stanie wyjściowym, jak i znosiła zwykły proinwazyjny efekt IL8. Natomiast komórki HER2-dodatnie nadal reagowały na IL8, ale blokada Shp1 niemal nie zmieniała ich zachowania, co sugeruje, że w tych guzach Shp1 jest zaangażowany w inne sygnały, takie jak HER2, i jest mniej dostępny do regulacji CXCR2. Analizy dużych zbiorów ekspresji genów potwierdziły ten obraz: linie potrójnie ujemne miały tendencję do niższych poziomów Shp1, zmienionej sygnalizacji związanej z GPCR i wyższego IL8, co odpowiada bardziej agresywnemu, napędzanemu stanem zapalnym profilowi.
Co to oznacza dla przyszłych terapii
Dla osoby niebędącej specjalistą główne przesłanie jest takie, że enzym Shp1 działa jak kontroler ruchu dla receptora IL8, CXCR2 — decyduje, czy receptor jest ponownie wykorzystywany, czy niszczony, a w konsekwencji jak silnie komórki raka piersi reagują na sygnały zapalne. W rakach piersi luminalnych i potrójnie ujemnych punkt ten wydaje się szczególnie istotny: gdy poziomy Shp1 są niskie albo jego aktywność jest zablokowana, komórki stają się bardziej inwazyjne, a wyniki leczenia gorsze. Ponieważ poziom lub aktywność Shp1 można zwiększyć lub modulować za pomocą niektórych istniejących leków, ukierunkowanie osi Shp1–CXCR2, być może w połączeniu z inhibitorami IL8 lub CXCR2, mogłoby być nową strategią ograniczania inwazji i metastaz w agresywnych podtypach raka piersi.
Cytowanie: Monti, M., Amendola, P.G., Filograna, A. et al. Shp1 phosphatase regulates CXCR2 protein stability and IL8-mediated invasiveness in breast cancer. Cell Death Dis 17, 297 (2026). https://doi.org/10.1038/s41419-026-08516-4
Słowa kluczowe: inwazja raka piersi, sygnalizacja IL8, receptor CXCR2, fosfataza Shp1, potrójnie ujemny rak piersi