Clear Sky Science · pl
CRMP2 hamuje tworzenie przerzutów, osłabiając ILF3‑zależną stabilizację mRNA CXCL10 w raku piersi
Dlaczego zatrzymanie rozprzestrzeniania się raka ma znaczenie
Większość zgonów z powodu raka piersi nie wynika z pierwotnego guza, lecz z tego, że komórki nowotworowe wędrują do istotnych narządów, takich jak płuca, i tworzą tam nowe ogniska choroby. W tym badaniu opisano wbudowane białko ochronne w komórkach raka piersi, które potrafi spowolnić, a nawet zablokować to rozprzestrzenianie, zmieniając „powitalną matę”, jaką odległe narządy przygotowują dla przemieszczających się komórek nowotworowych. Zrozumienie tego ukrytego przełącznika bezpieczeństwa może otworzyć drogę do nowych terapii, które uniemożliwią zakorzenienie się raka w innych częściach ciała.
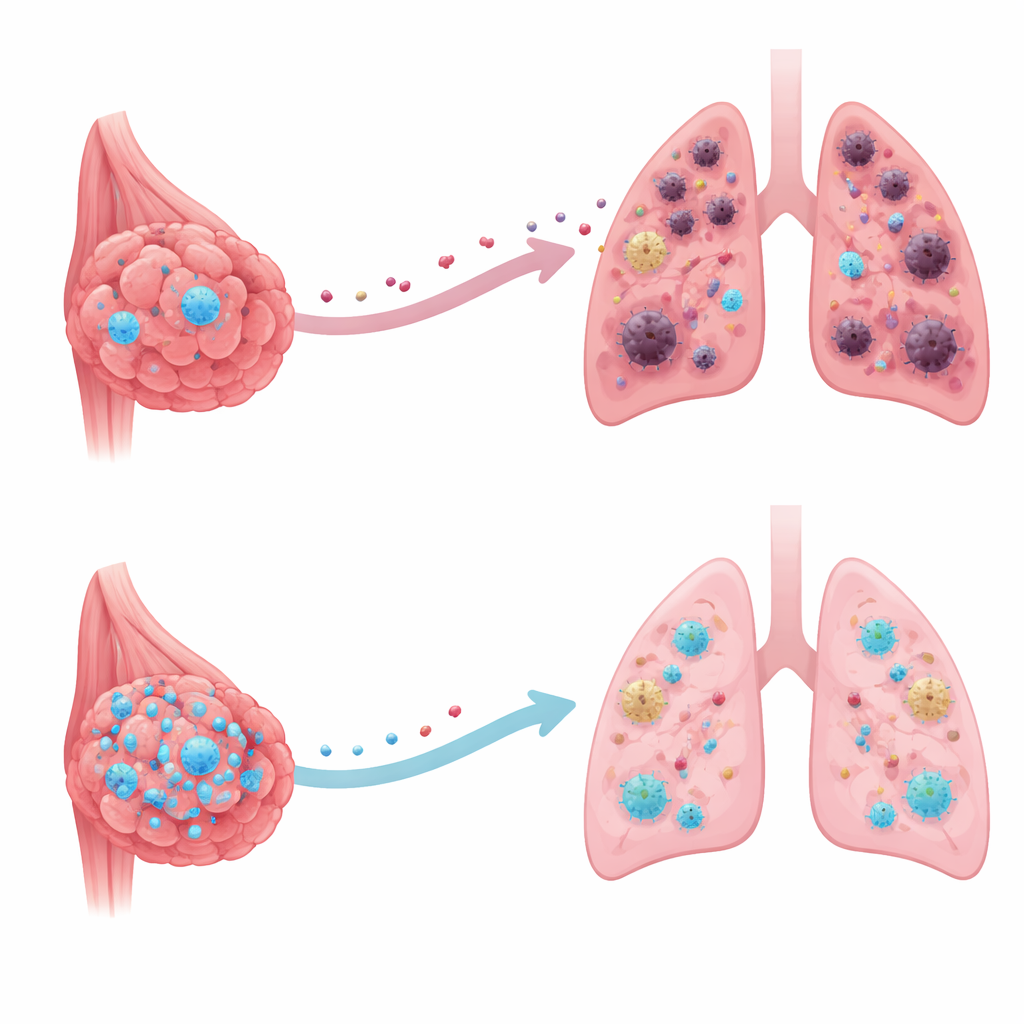
Cichy obrońca wewnątrz komórek nowotworowych
Naukowcy skupili się na białku o nazwie CRMP2, najlepiej znanym z roli we wspieraniu wzrostu i utrzymania cytoszkieletu komórek nerwowych. Analiza dużych publicznych baz danych nowotworowych oraz próbek guzów od pacjentów wykazała, że poziomy CRMP2 są nietypowo niskie w rakach piersi, szczególnie w tych, które już dały przerzuty. Pacjenci, których guzy wciąż zawierały wyższe ilości CRMP2, mieli tendencję do dłuższego przeżycia i mniejsze ryzyko powstania odległych przerzutów. Ten wzorzec sugeruje, że CRMP2 pełni w raku piersi rolę hamulca, działając jako wewnętrzny obrońca zamiast czynnik napędowy choroby.
Jak płuca są przygotowywane do inwazji
Komórki nowotworowe rzadko pojawiają się w odległym narządzie zupełnie niespodziewanie. Na długo przed ich przybyciem pierwotny guz uwalnia cząsteczki, które przekształcają ten narząd w tzw. „prekorektywną niszę przerzutową” – mikrośrodowisko sprzyjające przetrwaniu nowotworu. W dobrze ugruntowanym modelu myszy, który wiernie naśladuje ludzki rak piersi, zespół wykazał, że gdy komórki guza piersi zostały zmodyfikowane tak, by produkować dodatkowy CRMP2, guzy pierwotne rosły tak samo szybko, ale płuca stawały się znacznie mniej przyjazne. Markery zapalenia i przebudowy tkanki w płucach spadły, a mniej komórek układu odpornościowego, które normalnie tłumią obronę przeciwnowotworową, zostało zrekrutowanych. W efekcie, po usunięciu guza pierwotnego, w płucach powstawało znacznie mniej guzków przerzutowych.
Łańcuch sygnałów, który wywołuje kłopoty
Idąc głębiej, naukowcy zastanawiali się, które wydzielane przez guz sygnały odpowiadają za przygotowanie płuc. Skoncentrowali się na CXCL10, małym białku sygnałowym (chemokinie) znanym z przyciągania określonych komórek układu odpornościowego i pobudzania uśpionych komórek nowotworowych. Zarówno w hodowanych w laboratorium ludzkich, jak i mysich komórkach raka piersi zwiększenie CRMP2 wyraźnie zmniejszało ilość wytwarzanego i uwalnianego CXCL10. U myszy, płuca narażone na materiał guza bogaty w CRMP2 miały znacznie niższe poziomy CXCL10 i mniej napływających komórek odpornościowych, które zwykle osłabiają aktywność komórek T. Kiedy badacze zablokowali CXCL10 przeciwciałem, kolonizacja płuc przez komórki nowotworowe zmalała; gdy dodali dodatkowy CXCL10, zniweczyło to ochronny efekt CRMP2. To umiejscowiło CXCL10 bezpośrednio poniżej CRMP2 jako kluczowego inicjatora niszy sprzyjającej przerzutom.
Ukryty pośrednik stabilizujący szkodliwe sygnały
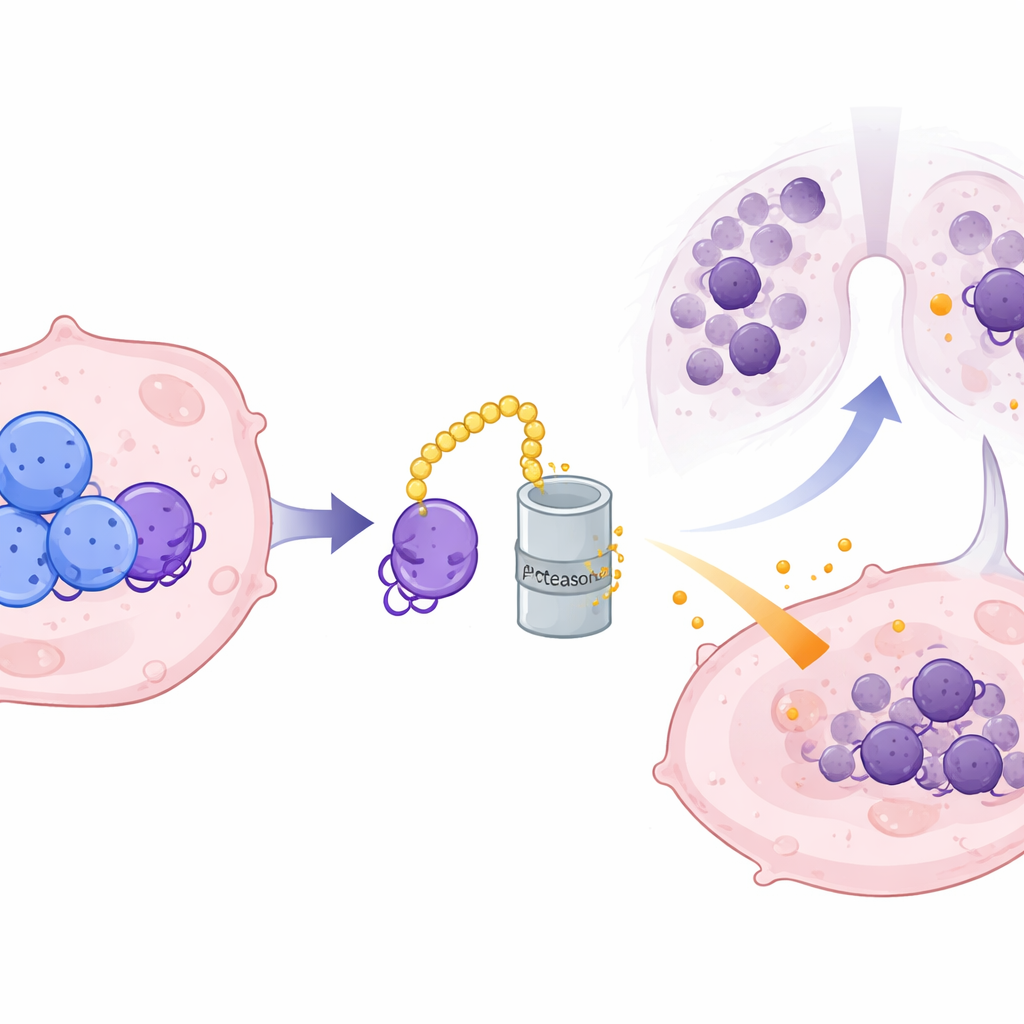
Ponieważ CRMP2 występuje wewnątrz komórek, a CXCL10 jest wydzielany, zespół podejrzewał istnienie molekularnego pośrednika. Zidentyfikowali ILF3, białko wiążące RNA, jako bezpośredniego partnera CRMP2. ILF3 przyczepia się do matrycowego RNA CXCL10 i zwykle chroni je przed rozkładem, co pozwala na produkcję większej ilości białka CXCL10. CRMP2 wiąże się z ILF3 w określonych punktach kontaktu i oznacza je do zniszczenia przez komórkowe mechanizmy recyklingu białek, skracając żywotność ILF3 i przerywając jego wpływ na RNA CXCL10. Gdy poziomy CRMP2 są wysokie, ILF3 jest szybciej degradowane, RNA CXCL10 staje się niestabilne, a mniej tej zapalnej chemokiny jest wydzielane. Przy sztucznym przywróceniu ILF3 mogło ono zneutralizować tłumienie CXCL10 przez CRMP2, potwierdzając swoją rolę jako kluczowe ogniwo w tym łańcuchu.
Przekształcanie związku roślinnego w potencjalnego sojusznika
Aby sprawdzić, czy tę ścieżkę można wykorzystać terapeutycznie, badacze przesiewali bibliotekę związków naturalnych i odkryli, że psoralen – pochodna roślinna od dawna stosowana w leczeniu skóry – wiąże się bezpośrednio z CRMP2 i zwiększa jego stabilność. W eksperymentach na komórkach psoralen podnosił poziomy CRMP2, obniżał ILF3 i CXCL10 oraz zmniejszał inwazyjne zachowanie komórek raka piersi, nie wpływając na ich ogólną przeżywalność. W wielu modelach mysich psoralen nie zmniejszał wielkości guzów pierwotnych, ale silnie ograniczał przerzuty do płuc i osłabiał tworzenie prekorektywnej niszy przerzutowej, ponownie w sposób zależny od CRMP2. Chociaż sam psoralen może powodować toksyczność wątroby i będzie wymagał udoskonalenia, te wyniki pokazują, że małe cząsteczki mogą wzmocnić ochronną rolę CRMP2.
Co to oznacza dla pacjentów
Podsumowując, praca ujawnia osłonową oś wewnątrz komórek raka piersi, w której CRMP2 destabilizuje ILF3, co z kolei obniża poziom CXCL10 i zapobiega temu, by płuca stały się podatnym gruntem dla przerzutów. Zamiast atakować komórki nowotworowe bezpośrednio, strategia ta ma na celu unieszkodliwienie odległych nisz, od których zależą przerzuty, przechylając balans na korzyść własnych mechanizmów obronnych organizmu. Choć przed zastosowaniem klinicznym pozostaje jeszcze wiele pracy, celowanie w szlak CRMP2–ILF3–CXCL10 – być może przy użyciu bezpieczniejszych związków podobnych do psoralenu – oferuje obiecujące nowe podejście do powstrzymywania rozprzestrzeniania się raka piersi.
Cytowanie: Lin, B., Luo, M., Zhou, Y. et al. CRMP2 inhibits metastasis formation by impairing ILF3-dependent stabilization of CXCL10 mRNA in breast cancer. Cell Death Dis 17, 255 (2026). https://doi.org/10.1038/s41419-026-08515-5
Słowa kluczowe: przerzuty raka piersi, prekorektywny nisza przerzutowa, sygnalizacja chemokin, białka wiążące RNA, leki pochodzenia naturalnego