Clear Sky Science · pl
Ubenimex współdziała z blokadą PD-L1 w raku żołądka przez konkurencyjne wiązanie LAP3 z UBE3A
Dlaczego to badanie ma znaczenie
Dla wielu osób z zaawansowanym rakiem żołądka nowoczesne leki immunoterapeutyczne, które „zwalniają hamulce” układu odpornościowego, przyniosły nową nadzieję — jednak nadal pomagają tylko niewielkiej części pacjentów. To badanie stawia praktyczne pytanie o realny wpływ: czy starszy lek wzmacniający odporność, Ubenimex, można ponownie zastosować, aby zwiększyć skuteczność tych leków i dlaczego miałoby to pomóc? Naukowcy odkrywają ukryty molekularny trik, którego nowotwory używają, by unikać ataku immunologicznego, i pokazują, jak Ubenimex może go odwrócić, otwierając drogę do skuteczniejszych terapii skojarzonych.
Nowy partner dla immunoterapii przeciwnowotworowej
Praca skupia się na raku żołądka, chorobie nadal częstej i śmiertelnej, zwłaszcza w Chinach. Leki blokujące PD-1 lub PD-L1 — białka tłumiące odpowiedzi immunologiczne — są dziś podstawą leczenia. Mimo to większość pacjentów nie reaguje lub w końcu doświadcza nawrotu. Autorzy zwrócili się ku Ubenimexowi, długo zatwierdzonemu lekowi stosowanemu jako dodatek do chemioterapii i radioterapii, znanemu ze stymulowania komórek odpornościowych. Zastanawiali się, czy połączenie Ubenimexu z przeciwciałami blokującymi PD-L1 mogłoby uczynić guzy bardziej podatnymi na atak cytotoksycznych limfocytów T, komórek odpornościowych, które bezpośrednio niszczą komórki nowotworowe.
Testowanie kombinacji leków
W modelu myszy z rakiem żołądka, w którym guzy były genetycznie zmodyfikowane do nadprodukcji białka LAP3, zespół leczył zwierzęta Ubenimexem, przeciw-PD-L1, oboma lekami lub bez leczenia. Każde leczenie indywidualnie zmniejszało guzy, ale kombinacja wyróżniała się: guzy całkowicie zregresowały u wszystkich leczonych myszy, a przeżywalność poprawiła się bardziej niż przy samej blokadzie PD-L1. Analizy immunologiczne wykazały, że kombinacja znacznie zwiększyła liczbę i aktywność cytotoksycznych limfocytów CD8, które wydzielały więcej toksycznych cząsteczek i zapalnych mediatorów. Co istotne, leczenie nie powodowało widocznych uszkodzeń wątroby ani utraty masy ciała, co sugeruje, że podejście to może być skuteczne bez nadmiernej toksyczności.
Ukryty przełącznik chroniący guzy
Aby zrozumieć, dlaczego Ubenimex pomagał, badacze skoncentrowali się na LAP3, enzymie, który on hamuje. Stwierdzili, że poziomy LAP3 były wyższe w ludzkich guzach żołądka niż w normalnej tkance żołądkowej, a pacjenci z wyższym LAP3 mieli zwykle gorsze przeżycie. Zarówno w próbkach pacjentów, jak i w guzach mysich wysoki poziom LAP3 wiązał się z mniejszą liczbą limfocytów CD8 w obrębie nowotworu, mimo że inne typy komórek układu odpornościowego pozostawały niezmienione. Gdy LAP3 eksperymentalnie zmniejszano w komórkach nowotworowych, guzy rosły wolniej, przyciągały więcej limfocytów CD8 i stawały się łatwiejsze do zabicia w testach in vitro. Dane razem sugerują, że LAP3 nie jest tylko biernym obserwatorem, lecz aktywnym promotorem ucieczki przed układem odpornościowym.
Jak guzy wykorzystują LAP3, by trzymać hamulec
Dokopując się głębiej, zespół odkrył mechanizm, dzięki któremu LAP3 chroni komórki nowotworowe przed atakiem immunologicznym. Odkryto, że LAP3 pomaga stabilizować PD-L1, kluczowe „hamulec” na komórkach nowotworowych, który wyłącza limfocyty T. Normalnie PD-L1 może być znakowany małymi peptydami, które kierują je do komórkowego mechanizmu utylizacji. Enzym nazwany UBE3A przyłącza te znaczniki, prowadząc do rozpadu PD-L1. LAP3 fizycznie wiąże UBE3A i przez to uniemożliwia UBE3A znakowanie PD-L1. W rezultacie PD-L1 gromadzi się na powierzchni guza, tworząc ochronną tarczę przed limfocytami CD8. Gdy poziomy LAP3 maleją lub gdy jego działanie jest blokowane, PD-L1 jest intensywniej znakowany, szybciej rozkładany, a jego poziom na powierzchni spada — pozwalając limfocytom T zbliżyć się i zaatakować.
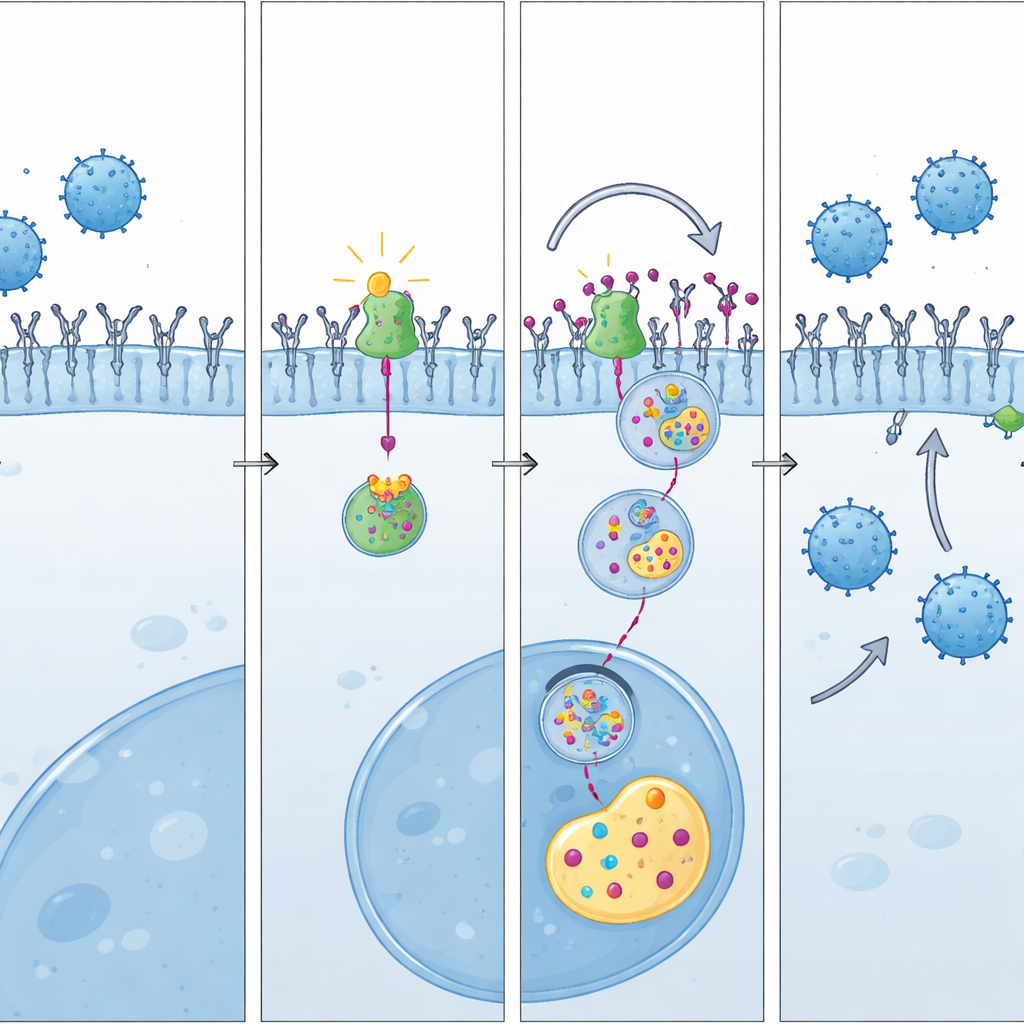
Jak Ubenimex przechyla szalę
W badaniu wykazano następnie, że Ubenimex działa przez zakłócenie partnerstwa LAP3–UBE3A. Modele komputerowe i eksperymenty biochemiczne wskazują, że Ubenimex umiejscawia się w LAP3 w tym samym rejonie, gdzie LAP3 normalnie oddziałuje z UBE3A. To konkurencyjne wiązanie odciąga UBE3A od LAP3, uwalniając je do znakowania PD-L1 kierującego go na rozkład. W doświadczeniach komórkowych Ubenimex zmniejszał PD-L1 na powierzchni komórek nowotworowych, zwiększał znakowanie PD-L1 do degradacji i odwracał efekt podwyższenia PD-L1 wywołany nadmiarem LAP3. W żywych myszach ta molekularna zmiana przełożyła się na większą aktywność limfocytów CD8 i spektakularną kontrolę guza, gdy Ubenimex był stosowany razem z blokadą PD-L1.
Co to oznacza dla pacjentów
Podsumowując, badanie przedstawia jasny obraz: wiele guzów żołądka nadprodukuje LAP3, co pomaga im utrzymywać wysokie poziomy PD-L1 i w ten sposób ukrywać się przed układem odpornościowym. Ubenimex przełamuje tę ochronę, blokując uchwyt LAP3 na UBE3A, co pozwala PD-L1 zostać usuniętym. Przy mniejszej liczbie „hamulców” na powierzchni komórek nowotworowych leki blokujące PD-L1 i cytotoksyczne limfocyty T mogą współpracować znacznie skuteczniej. Ponieważ Ubenimex jest już stosowany klinicznie, a LAP3 można mierzyć w próbkach guzów, badanie dostarcza konkretnej, testowalnej strategii poprawy immunoterapii w raku żołądka i potencjalnie w innych nowotworach z podwyższonym LAP3.
Cytowanie: Zhao, C., Li, J., Zheng, J. et al. Ubenimex synergizes with the PD-L1 blockade in gastric cancer by competitively binding LAP3 with UBE3A. Cell Death Dis 17, 241 (2026). https://doi.org/10.1038/s41419-026-08509-3
Słowa kluczowe: rak żołądka, immunoterapia, PD-L1, Ubenimex, LAP3