Clear Sky Science · pl
CCL11 sprzyja nawrotowi raka wątrobowokomórkowego po operacji, wzmacniając immunosupresyjne CCR5 + CD206 + makrofagi typu M2 i zwiększając inwazyjność guza
Dlaczego rak wątroby może powrócić po operacji
Chirurgia wątroby często stanowi najlepszą nadzieję dla pacjentów z wczesnym stadium raka wątroby, jednak wielu pacjentów doświadcza nawrotu choroby w ciągu kilku lat. Badanie stawia proste, lecz kluczowe pytanie: czy własna odpowiedź zapalna organizmu po operacji mimowolnie pomaga przetrwałym komórkom nowotworowym w wzroście i rozprzestrzenianiu się? Badacze koncentrują się na cząsteczce sygnalizacyjnej zwanej CCL11 i pokazują, że jej wzrost po zabiegu może jednocześnie osłabiać odporność przeciwnowotworową oraz czynić pozostałe komórki guza bardziej agresywnymi.
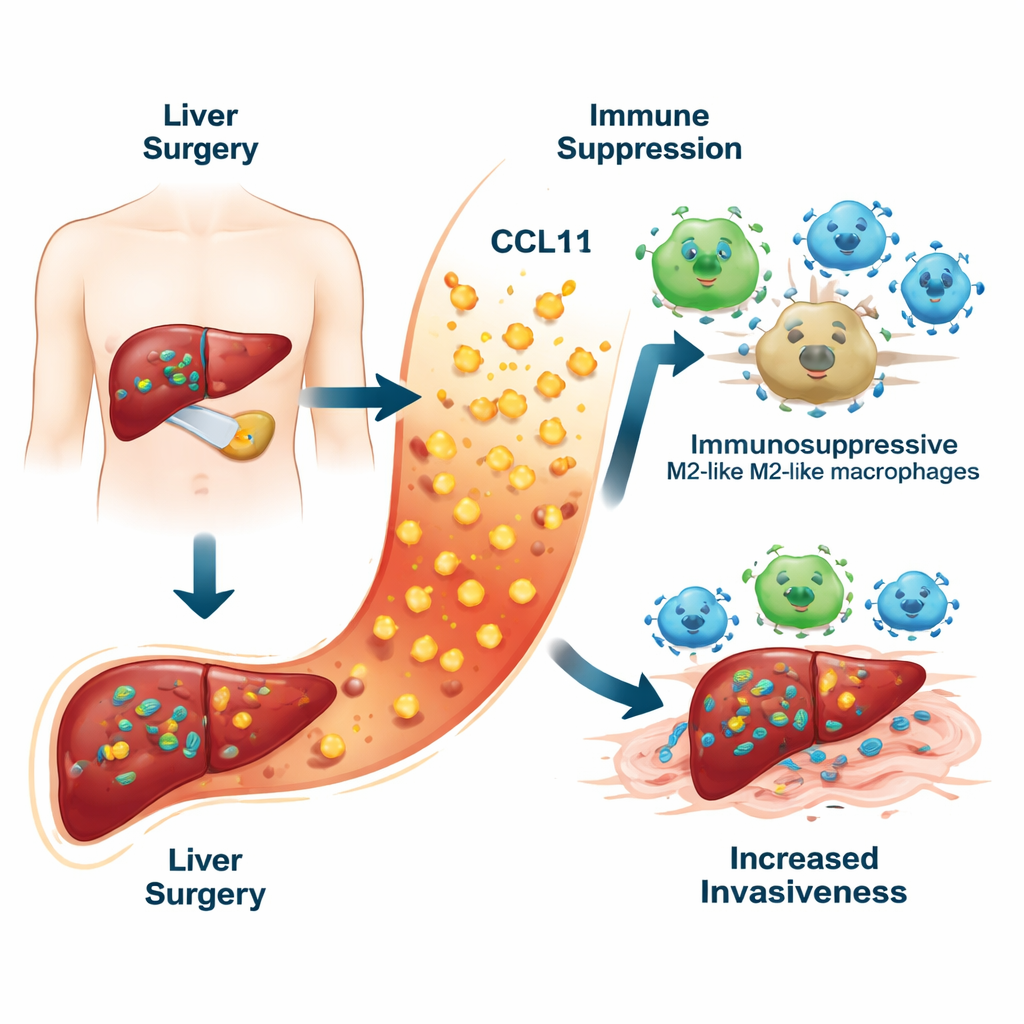
Ukryte zagrożenie w reakcji gojenia
Gdy chirurdzy usuwają guz wątroby, muszą zacisnąć naczynia krwionośne i uszkodzić otaczającą tkankę. To uszkodzenie wywołuje falę zapalenia, która wspiera gojenie wątroby. Mierząc dziesięć różnych cząsteczek zapalnych we krwi pacjentów tydzień po operacji, zespół odkrył, że jedna chemokina, CCL11, wyróżniała się. Pacjenci, u których później wystąpił nawrót raka wątroby, mieli znacząco wyższe poziomy CCL11 niż ci, którzy pozostali wolni od choroby. Wysokie stężenia CCL11 wiązały się także z gorszym przeżyciem. Kiedy badacze połączyli CCL11 z rutynowymi danymi klinicznymi, takimi jak badania krwi i cechy guza, zbudowali „kartę ryzyka”, która przewidywała nawroty w ciągu pięciu lat dokładniej niż tradycyjne modele.
Nawet tkanka wątroby wyglądająca na prawidłową ma znaczenie
Większość badań nad rakiem skupia się na samym guzie, ale to badanie pokazuje, że otaczająca „prawidłowa” tkanka wątroby może być równie ważna. W próbkach od ponad 100 pacjentów CCL11 było w rzeczywistości wyższe w tkance pozaguzowej niż w guzach nowotworowych czy wątrbach dawców zdrowych. Pacjenci, których pobliska tkanka wątroby produkowała więcej CCL11, częściej mieli zaawansowaną chorobę, przerzuty odległe i nawroty po operacji. W modelach mysich, które naśladują krótkotrwały zanik i przywrócenie przepływu krwi podczas zabiegu, uszkodzenie wątroby szybko podnosiło poziomy CCL11. W warunkach niskiego tlenu in vitro komórki wspierające wątrobę, takie jak miofibroblasty i komórki śródbłonka naczyń, również wytwarzały więcej CCL11, co sugeruje, że stres chirurgiczny przygotowuje pozostałą część wątroby do stania się środowiskiem sprzyjającym nowotworom.
Jak CCL11 zamienia obrońców immunologicznych w biernych obserwatorów
Aby sprawdzić, jak CCL11 kształtuje odporność, autorzy przyjrzeli się makrofagom — wszechstronnym białym krwinkom, które mogą albo atakować guzy, albo je chronić. Stwierdzili, że w tkance pozaguzowej wyższe poziomy CCL11 szły w parze z większą liczbą podtypu makrofagów niosących marker CCR5 i wykazujących profil tzw. M2-podobny, sprzyjający nowotworowi. U pacjentów wątroby bogate w te CCR5+ M2-podobne makrofagi wiązały się z gorszym przeżyciem. W hodowlach komórkowych dodanie CCL11 skłaniało monocyty do przemiany w ten immunosupresyjny typ makrofagów, zwiększając cząsteczki takie jak PD‑L1 i IL‑10 oraz uwalniając sygnały, które przyciągały i polaryzowały więcej komórek odpornościowych. Te „warunkowane” CCL11 makrofagi następnie sprzyjały przekształceniu naiwnych pomocniczych limfocytów T w komórki regulatorowe (Treg), populację znaną z tłumienia odpowiedzi przeciwnowotworowych. Doświadczenia mechanistyczne wykazały, że CCL11 aktywuje w makrofagach łańcuch sygnałowy kończący się szlakiem NF‑κB i produkcją PD‑L1, co pomaga osłonić komórki nowotworowe przed atakiem immunologicznym.
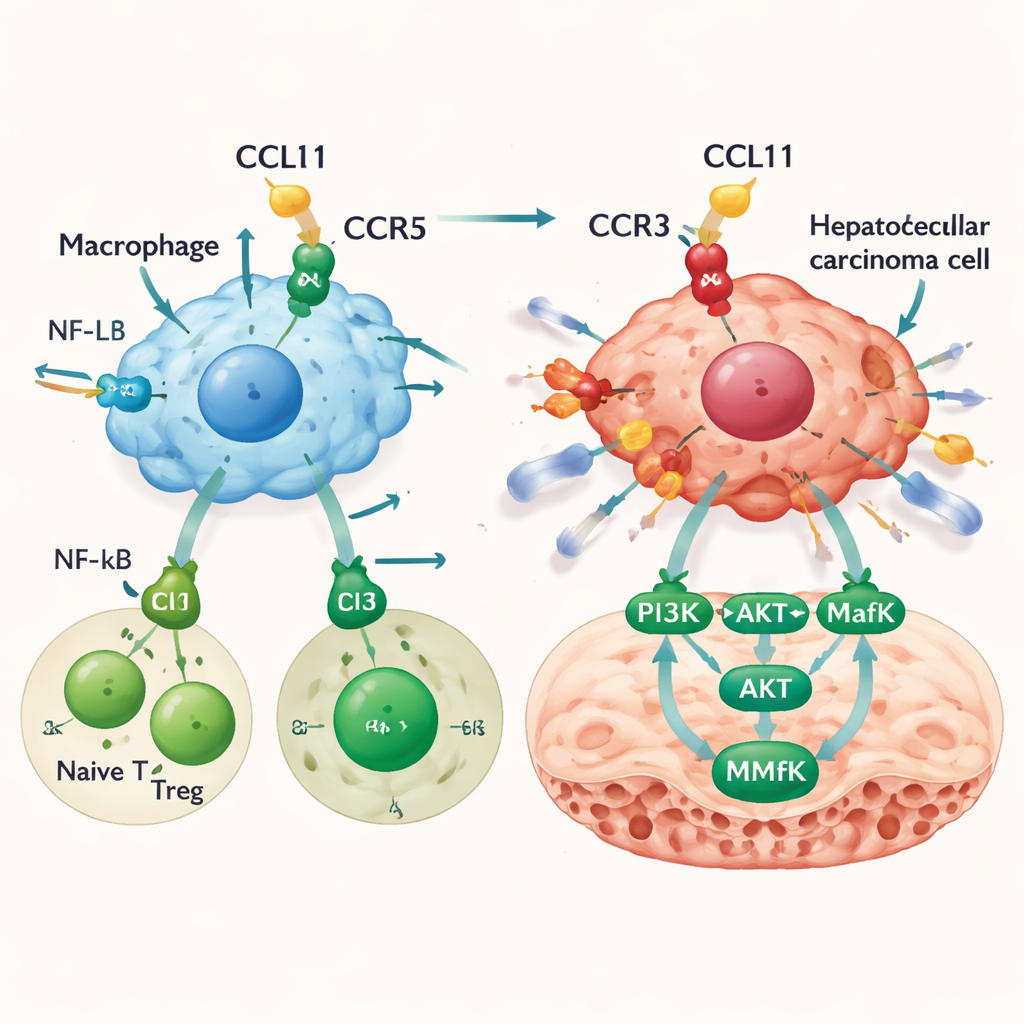
Jak CCL11 zwiększa inwazyjność pozostałych komórek nowotworowych
CCL11 nie tylko przekształca krajobraz immunologiczny; działa też bezpośrednio na komórki raka wątroby. Chociaż same komórki nowotworowe wytwarzają niewiele CCL11, posiadają jeden z jego receptorów, CCR3. W testach laboratoryjnych CCL11 nie przyspieszał wzrostu komórek raka wątroby, ale zwiększał ich migrację i zdolność do inwazji przez bariery — cechę typową dla potencjału przerzutowego. Blokowanie receptora CCR3 w dużej mierze niwelowało ten efekt. Analizy genów wskazały na szlak, w którym sygnalizacja CCL11–CCR3 uruchamia PI3K i AKT, co następnie aktywuje czynnik transkrypcyjny MafK. MafK z kolei zwiększa produkcję MMP13, enzymu rozkładającego otaczającą tkankę i otwierającego drogę do rozprzestrzeniania się nowotworu. W modelach mysich podawanie CCL11 do wątroby zwiększało obciążenie guzem i prowadziło do większej liczby przerzutów, wraz z wyższą aktywnością szlaku PI3K–AKT–MafK–MMP13 w obrębie guzów.
Przełożenie ryzykownego sygnału na szansę leczenia
Ponieważ CCL11 wydaje się jednocześnie wyciszać obronę immunologiczną i wzmacniać przetrwałe komórki nowotworowe, badacze sprawdzili, czy jego zablokowanie po operacji może zmienić wyniki. U myszy z guzami wątroby, które zostały chirurgicznie usunięte, leczenie przeciwciałem neutralizującym CCL11 znacząco zmniejszyło wskaźnik nawrotów w wątrobie i poprawiło przeżycie, bez widocznych skutków ubocznych takich jak utrata masy ciała. Zebrane razem wyniki przedstawiają CCL11 jako główny przełącznik łączący uraz chirurgiczny z immunosupresyjnym, sprzyjającym inwazji środowiskiem wątroby. Dla pacjentów praca ta sugeruje, że pomiar CCL11 po operacji mógłby pomóc zidentyfikować osoby o najwyższym ryzyku nawrotu, a leki celujące w oś CCL11–CCR5/CCR3 mogłyby w przyszłości stać się elementem strategii zapobiegających nawrotom raka wątroby.
Cytowanie: Wang, J., Yeung, O.WH., Qiu, W. et al. CCL11 promotes hepatocellular carcinoma recurrence after surgery by potentiating immunosuppressive CCR5 + CD206 + M2-like macrophages and promoting tumor invasiveness. Cell Death Dis 17, 236 (2026). https://doi.org/10.1038/s41419-026-08508-4
Słowa kluczowe: nawroty raka wątroby, chemokina CCL11, mikrośrodowisko guza, tłumienie układu odpornościowego, przerzuty nowotworowe