Clear Sky Science · pl
Fibroblasty związane z nowotworem sprzyjają oporności na osimertynib w komórkach niedrobnokomórkowego raka płuca poprzez m7G-modyfikację NET1 zależną od METTL1
Dlaczego niektóre raki płuca przestają reagować na „inteligentny” lek
Leki celowane, takie jak osimertynib, zrewolucjonizowały leczenie wielu osób z powszechnym typem raka płuca, zapewniając dłuższe życie przy mniejszych skutkach ubocznych niż tradycyjna chemioterapia. Jednak u większości pacjentów korzyści te są chwilowe: guzy w końcu znajdują sposoby, by przechytrzyć lek. Badanie stawia pozornie proste pytanie o dużych implikacjach: czy tkanka wspierająca guz — a konkretnie komórki zwane fibroblastami związanymi z nowotworem — po cichu pomagają komórkom nowotworowym uchylić się od działania osimertynibu?
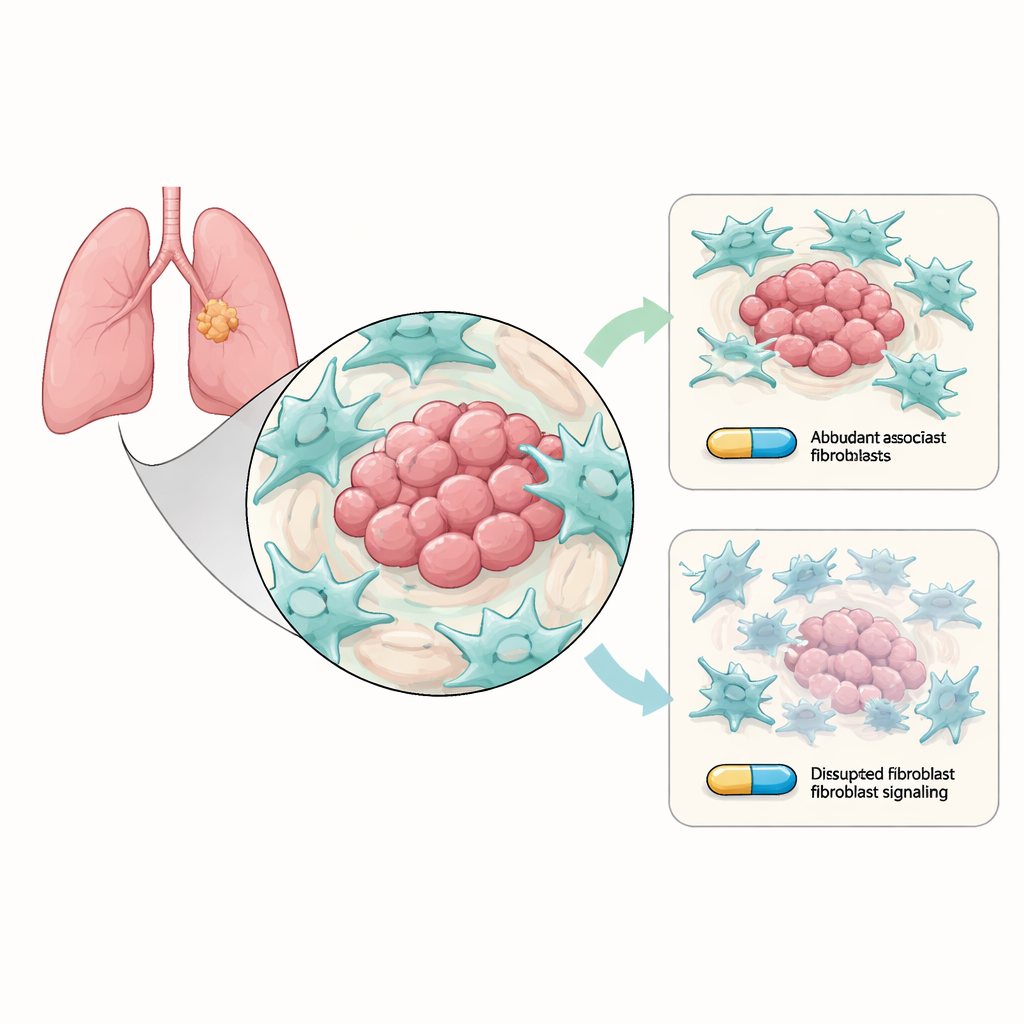
Pomocnicze komórki, które potajemnie osłaniają guz
Niedrobnokomórkowy rak płuca rozwija się w tętniącej życiem okolicy komórek niebędących nowotworowymi, zwanej mikrośrodowiskiem guza. Do najbardziej licznych mieszkańców należą fibroblasty związane z nowotworem (CAF), komórki tkanki łącznej, które przebudowują otoczenie guza. Badacze hodowali w laboratorium komórki raka płuca niosące typowe mutacje EGFR wrażliwe na osimertynib razem z CAF. Stwierdzili, że w obecności CAF komórki nowotworowe były trudniejsze do zabicia osimertynibem: tworzyły więcej kolonii, rzadziej ulegały apoptozie i wykazywały silniejsze cechy „podobne do komórek macierzystych” związane z długotrwałym przeżyciem i nawrotem. Innymi słowy, chociaż lek nadal celował w komórki nowotworowe, otaczające fibroblasty po cichu pomagały im przetrwać.
Chemiczna etykieta na RNA, która zmienia zasady gry
Zespół następnie spojrzał poza same geny na chemiczne znaczniki zdobiące RNA — robocze kopie informacji genetycznej w komórce. Jedna z takich etykiet, nazwana m7G, może wpływać na stabilność cząsteczki RNA i na to, jak efektywnie jest tłumaczona na białko. Przy użyciu testów biochemicznych i mapowania obejmującego cały genom badacze wykazali, że CAF zwiększają ogólną liczbę znakowań m7G na RNA wewnątrz komórek raka płuca. Ten wzrost był napędzany głównie przez enzym metylotransferazę o nazwie METTL1, który umieszcza znaczniki m7G na mRNA. Poziomy METTL1 były wyższe w guzach płuca niż w sąsiedniej tkance normalnej i korelowały z bardziej zaawansowaną chorobą oraz gorszym przeżyciem pacjentów, sugerując, że ten enzym robi coś więcej niż tylko drobne dostrajanie rutynowych funkcji komórkowych.
Sygnał wydzielany i podatny łańcuch molekularny
Jak CAF zwiększają poziom METTL1 w komórkach nowotworowych? Badanie wskazuje na białko o nazwie HMGB1, które CAF uwalniają do swojego otoczenia. W porównaniu z komórkami nowotworowymi CAF wydzielały znacznie większe ilości HMGB1. Gdy badacze dodali HMGB1 do komórek raka płuca, wzrosły poziomy METTL1 i znaczniki m7G; gdy zablokowali HMGB1 w medium kondycjonowanym przez CAF, efekt ten zanikał. Przybliżając dalej, zidentyfikowali jeden kluczowy cel RNA METTL1: NET1, gen wspierający wzrost i ruchliwość komórek. CAF zwiększały zarówno znakowanie m7G, jak i obfitość RNA oraz białka NET1, a METTL1 fizycznie wiązał RNA NET1, stabilizując je. Mniej METTL1 oznaczało mniej zmodyfikowanego NET1, słabsze sygnały przeżyciowe komórek nowotworowych i większą wrażliwość na osimertynib.
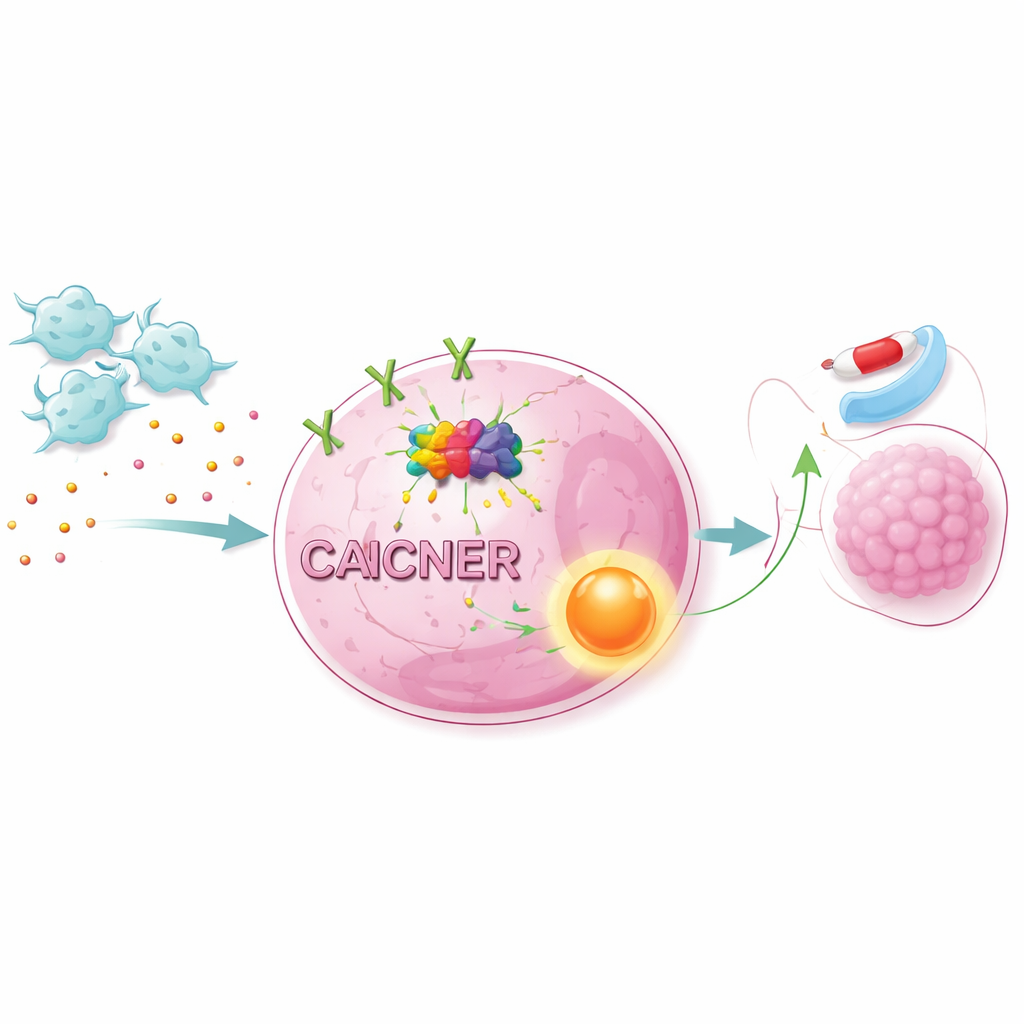
Włączanie szlaków przeżycia wewnątrz komórek nowotworowych
Wzmocniony sygnał NET1 nie działał w izolacji. Łącząc duże zestawy danych RNA z analizą szlaków, naukowcy pokazali, że CAF aktywują główną drogę wzrostu i przeżycia wewnątrz komórek znaną jako szlak AKT/NF-κB. Zablokowanie AKT lub NF-κB przy użyciu specyficznych inhibitorów uczyniło komórki raka płuca bardziej podatnymi na osimertynib, nawet w obecności CAF. Zmiany poziomów NET1 dały podobne efekty: obniżenie NET1 osłabiło ochronę ze strony CAF, podczas gdy zwiększenie NET1 wzmocniło oporność. U myszy wszczepionych ludzkimi komórkami raka płuca dodanie CAF sprawiło, że guzy rosły szybciej i były mniej wrażliwe na osimertynib. Wyciszenie METTL1 w komórkach nowotworowych zmniejszyło znaczniki m7G, obniżyło poziomy NET1 i aktywację szlaku oraz zdecydowanie ograniczyło wzrost guza napędzany przez CAF.
Co to oznacza dla przyszłego leczenia raka płuca
Dla osób z rakiem płuca z mutacją EGFR praca ta przedstawia nowe spojrzenie na to, dlaczego potężne leki, takie jak osimertynib, ostatecznie zawodzą. Zamiast przypisywać winę wyłącznie nowym mutacjom w komórkach nowotworowych, podkreśla ona łańcuch molekularny rozpoczynający się poza komórką guza — od CAF wydzielających HMGB1 — i przebiegający przez METTL1, znaczniki m7G na NET1 oraz aktywację szlaków przeżycia, które łagodzą skutki leku. Przerwanie tego łańcucha w dowolnym punkcie mogłoby w zasadzie przywrócić lub wydłużyć wrażliwość na leczenie. Choć leki bezpośrednio celujące w METTL1, HMGB1 czy specyficzne RNA oznaczone m7G są wciąż na wczesnych etapach, badanie sugeruje, że łączenie osimertynibu z terapiami wymierzonymi w komórki wspierające guz lub ich sygnały modyfikujące RNA może pomóc dłużej utrzymać tę postać raka płuca pod kontrolą.
Cytowanie: Qian, Y., Gong, Z., Jia, Y. et al. Cancer-associated fibroblasts promote osimertinib resistance in non-small cell lung cancer cells via METTL1-mediated NET1 m7G modification. Cell Death Dis 17, 248 (2026). https://doi.org/10.1038/s41419-026-08505-7
Słowa kluczowe: oporność na osimertynib, niedrobnokomórkowy rak płuca, fibroblasty związane z nowotworem, metylacja RNA, szlak METTL1 NET1