Clear Sky Science · pl
miR-424(322)~503 osłabia postęp nowotworu jelita grubego napędzanego przez deficyt PTEN
Dlaczego to badanie ma znaczenie dla raka jelita grubego
Rak jelita grubego pozostaje jednym z najczęstszych i najgroźniejszych nowotworów na świecie, a wielu pacjentów przechodzi do zaawansowanej choroby pomimo operacji, chemioterapii i leków celowanych. W badaniu zbadano niewielki zestaw genetycznych „regulatorów” zwanych microRNA, które mogą spowalniać lub przyspieszać wzrost guza. Odkrywając, jak określony klaster microRNA współdziała ze znanym genem supresorowym nowotworu PTEN, praca pomaga wyjaśnić, dlaczego niektóre raki jelita grubego stają się bardziej agresywne, i wskazuje nowe sposoby przewidywania ryzyka oraz projektowania terapii.
Maleńkie przełączniki RNA o dużym znaczeniu
MicroRNA to krótkie cząsteczki RNA, które nie kodują białek, lecz precyzyjnie regulują wykorzystanie setek genów w komórce. Klaster miR-424(322)~503, składający się z dwóch spokrewnionych microRNA, zadziwiał badaczy, ponieważ w różnych nowotworach może działać jak hamulec lub jak przyspieszacz. W raku jelita grubego jego rola była niejasna. Autorzy skupili się na nowotworach napędzanych utratą PTEN — genu, który zwykle kontroluje sygnały wzrostu i jest często zmieniony w guzach jelita grubego. Postawili proste, ale konsekwentne pytanie: co się dzieje z rozwojem raka jelita grubego, gdy brak jest zarówno PTEN, jak i tego klastra microRNA?
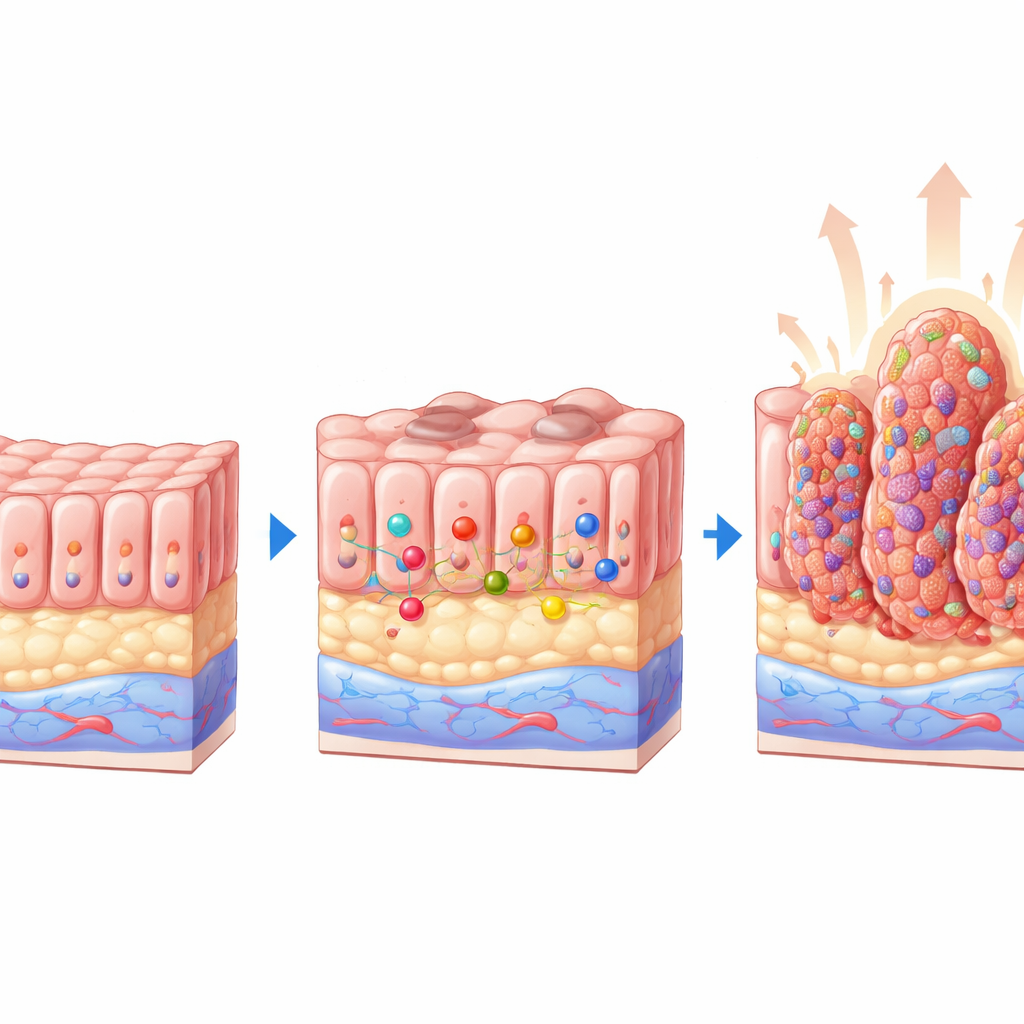
Modele myszy ujawniają rolę ochronną
Aby odpowiedzieć na to pytanie, zespół użył genetycznie zmodyfikowanych myszy, w których PTEN można wyłączyć w wyściółce jelita, i skrzyżował je z myszami pozbawionymi klastra miR-424(322)~503. Powstały cztery grupy: zwierzęta kontrolne, myszy pozbawione tylko microRNA, myszy pozbawione tylko PTEN oraz myszy podwójnie knockout pozbawione obu elementów. Po indukcji utraty PTEN dokładnie zbadano okrężnice. Zwierzęta z utratą jedynie PTEN rozwinęły wiele małych polipów, z których wiele miało wczesne zmiany nieprawidłowej tkanki. W uderzającym kontraście myszy pozbawione zarówno PTEN, jak i klastra microRNA miały znacznie więcej zmian, większe polipy i wyższy odsetek zmian zaawansowanych, w tym dysplazji wysokiego stopnia i jawnego gruczolakoraka. Sam klaster microRNA nie wywołał choroby, co pokazuje, że jego utrata jest szczególnie szkodliwa, gdy PTEN jest już brakujący.
Niezmieniony klasyczny szlak, przesunięcie ku nowym sprawcom
Rak jelita grubego często napędzany jest nadaktywacją szlaku Wnt/β-kateniny, kluczowej drogi kontrolującej komórki macierzyste w jelicie. Ponieważ ten klaster microRNA może wpływać na ten szlak w tkance piersi, autorzy sprawdzili, czy tak jest również tutaj. Ku zaskoczeniu, poziomy i lokalizacja β-kateniny oraz jej koreceptora LRP6 w okrężnicy nie zmieniły się po usunięciu klastra microRNA, nawet u myszy podwójnie knockout. Zamiast tego profilowanie ekspresji genów na dużą skalę wskazało inny kierunek: guzy pozbawione zarówno PTEN, jak i microRNA wykazywały silne sygnatury przebudowy tkanki, odpowiedzi na uraz oraz przejścia nabłonkowo-mezenchymalnego — programu związanego z naciekaniem i przerzutami. Szczególnie wzbogacone były drogi sygnałowe napędzane przez kinazy MAP (ERK1/2 i p38) oraz przez czynnik wzrostu TGFβ.
Jak sygnały wzrostu wymykają się spod kontroli
Zagłębiając się dalej, badacze zbadali białka w tkance okrężnicy. Odkryli, że podczas gdy sama utrata PTEN wzmagała szlak PI3K/AKT, dodanie utraty klastra microRNA wywołało dodatkowy wzrost aktywności MAPK: więcej aktywowanego JNK, p38, MKK4, a szczególnie ERK1/2. Te wysoce aktywne sygnały pokrywały się z wyższymi poziomami cykliny D1, kluczowego promotora podziału komórkowego. Jednocześnie komponenty szlaku TGFβ sprzyjające jego aktywności (SMAD3 i SMAD4) wzrosły, podczas gdy wewnętrzny hamulec (SMAD7) spadł, a komórki nowotworowe wykazywały silniejsze jądrowe barwienie SMAD2/3, zgodne z aktywacją szlaku. Porównując geny guzów mysich z przewidywanymi celami microRNA, zespół zidentyfikował IGF1 — silny czynnik wzrostu zasilający kaskady MAPK — jako bezpośredni cel klastra miR-424(322)~503. Gdy microRNA były nieobecne, IGF1 wymykał się represji, podbijając sygnalizację MAPK jeszcze bardziej. Analizy zestawów danych z ludzkiego raka jelita grubego odzwierciedliły te wyniki: IGF1 był wyższy w guzach z niskim poziomem miR-424 lub miR-503, a długi niekodujący RNA, który jest gospodarzem tych microRNA — MIR503HG — jak również same microRNA, były skoordynowanie zmienione w guzach pacjentów.
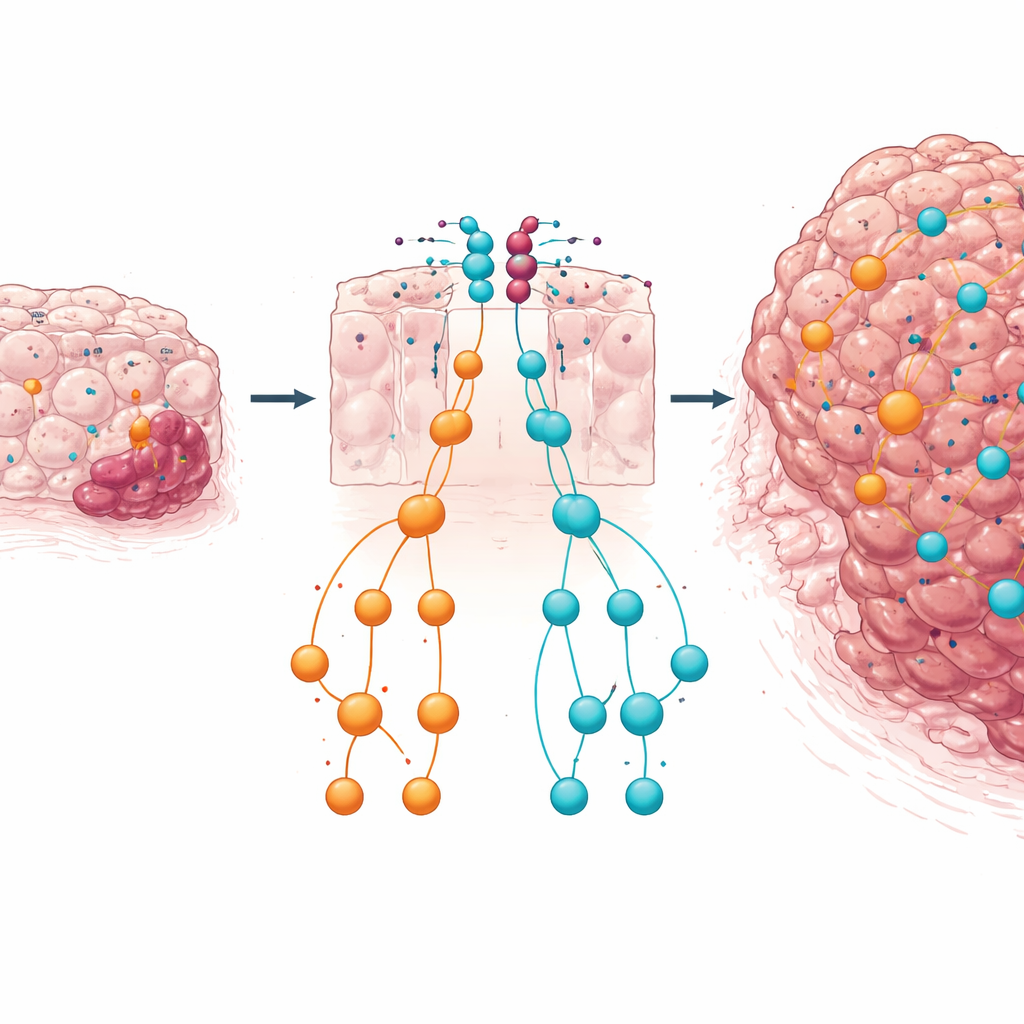
Podwójna siatka bezpieczeństwa i co to oznacza dla pacjentów
Podsumowując, wyniki sugerują, że w tkance jelita grubego pozbawionej PTEN klaster miR-424(322)~503 działa jak drugie zabezpieczenie. Gdy PTEN jest utracony, te microRNA są podwyższone, częściowo za pośrednictwem sygnałów takich jak TGFβ, i powstrzymują potężne szlaki wzrostu, takie jak IGF1–MAPK i TGFβ–SMAD. Jeśli ten mikroRNA‑owy hamulec zostanie usunięty, sygnały wzrostu i przebudowy wymykają się spod kontroli, przyspieszając przejście od łagodnych polipów do raka inwazyjnego. Dla laika kluczowe przesłanie jest takie, że nie wszystkie zmiany genetyczne w guzie działają w tym samym kierunku: niektóre są wbudowanymi mechanizmami obronnymi. Zrozumienie, jak PTEN i ten klaster microRNA współpracują, by utrzymać równowagę wzrostu komórek, może pomóc zidentyfikować pacjentów wysokiego ryzyka i zainspirować terapie kombinowane, które celują jednocześnie w osie PI3K/AKT oraz MAPK/TGFβ w raku jelita grubego.
Cytowanie: Vidal-Sabanés, M., Bonifaci, N., Navaridas, R. et al. miR-424(322)~503 impairs colon cancer progression driven by PTEN deficiency. Cell Death Dis 17, 254 (2026). https://doi.org/10.1038/s41419-026-08504-8
Słowa kluczowe: rak jelita grubego, PTEN, microRNA, szlak sygnalizacyjny MAPK, TGF-beta