Clear Sky Science · pl
Szlak ROR1-PI3K/AKT napędza adaptacyjną oporność na blokadę cyklu komórkowego w raku jajnika z mutacją TP53
Dlaczego te badania mają znaczenie dla zdrowia kobiet
Rak jajnika jest jednym z najgroźniejszych nowotworów u kobiet, w dużej mierze dlatego, że guzy często nabywają oporność na chemioterapię. W tym badaniu postawiono kluczowe pytanie: gdy silne leki mają na celu wymusić na komórkach nowotworowych śmiertelny błąd podziału, jak te komórki nadal znajdują sposoby na przeżycie i czy ta droga ucieczki może stać się sama w sobie słabością? Śledząc komórki raka jajnika przez tygodnie i miesiące terapii, badacze ujawniają centralny system kontroli wewnątrz komórek, który decyduje, czy one nadal się dzielą, czy zatrzymują i naprawiają uszkodzenia — oraz wskazują nowy sposób ataku na guzy, które już nauczyły się opierać standardowym lekom. 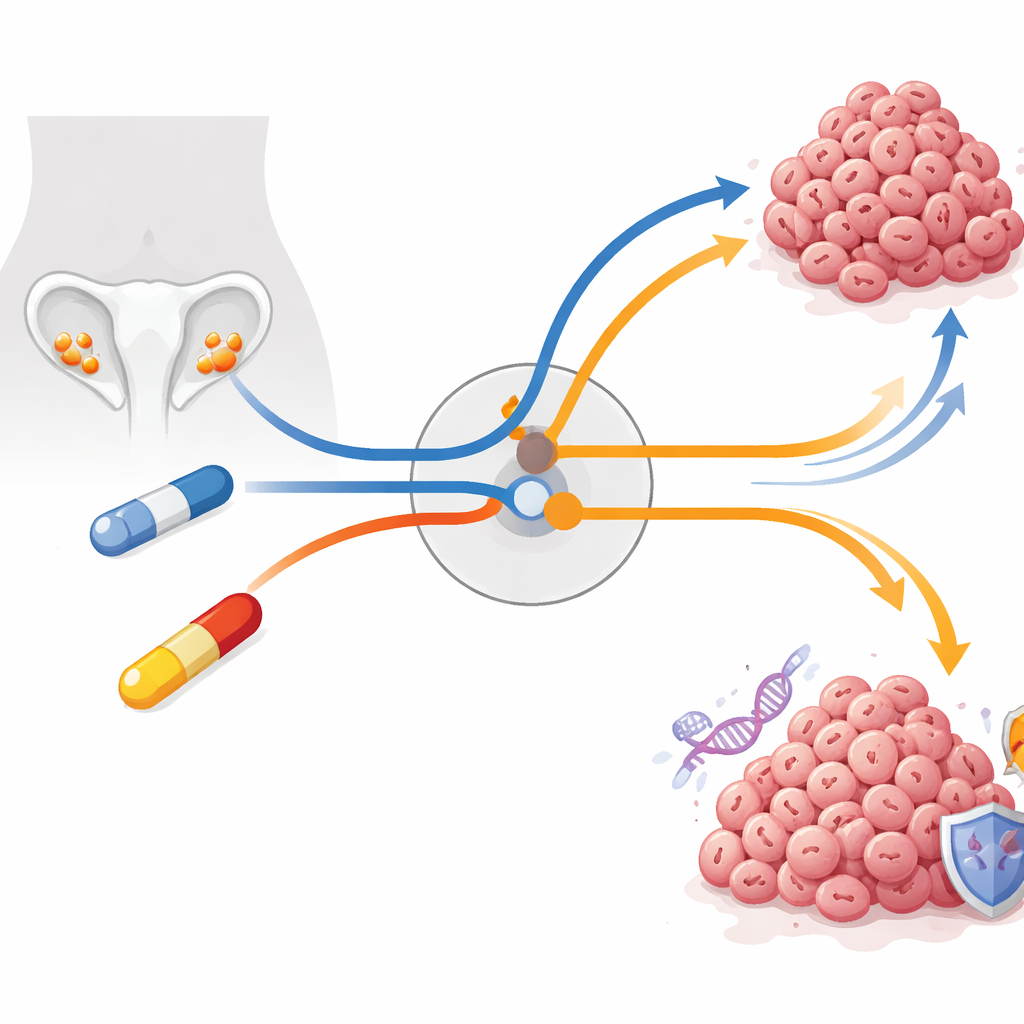
Dwa powszechne leki, jedna wspólna droga ucieczki
Zespół skupił się na raku surowiczym wysokiego stopnia złośliwości, najbardziej agresywnej i najczęstszej postaci choroby, która niemal zawsze zawiera mutacje w genie TP53, zwanym „strażnikiem genomu”. Ponieważ TP53 jest uszkodzony, te guzy szczególnie polegają na późniejszych punktach kontrolnych cyklu komórkowego. Dwa leki szeroko stosowane lub testowane w tym kontekście wykorzystują tę słabość: adawoserib, eksperymentalny inhibitor WEE1, który zmusza uszkodzone komórki do przedwczesnego wejścia w podział, oraz paklitaksel, standardowa chemioterapia, która unieruchamia wewnętrzny szkielet potrzebny do rozdzielenia chromosomów. W teorii oba powinny doprowadzić komórki nowotworowe do „katastrofy mitotycznej” — śmiertelnej porażki podziału. Jednak w klinice i laboratorium guzy często się adaptują. Badacze stworzyli modele komórek z długotrwałą opornością, stopniowo zwiększając dawki leków przez miesiące, co lepiej naśladuje to, co dzieje się u pacjentek, niż krótkie eksperymenty z wysokimi dawkami.
Jak komórki nowotworowe przebudowują się, by przetrwać
Wykorzystując zaawansowane obrazowanie i „Cell Painting” — technikę barwienia wielu struktur komórkowych jednocześnie — naukowcy zaobserwowali, że komórki odporne nie wyglądały po prostu jak ich poprzednie formy. Wiele z nich miało wiele jąder, przebudowany wewnętrzny szkielet oraz tworzyło gęściej upakowane skupiska i mniejsze, bardziej rozproszone sferoidy 3D — cechy częściowej zmiany kształtu znanej jako przejście nabłonkowo-mezenchymalne. Te zmiany morfologiczne sugerowały, że komórki przesterowały swoje zachowania ruchowe, podziałowe i interakcyjne. Równocześnie szczegółowe sekwencjonowanie RNA pojedynczych komórek ujawniło, że każdy lek i linia komórkowa wypracowały własny wzorzec zmienionych genów i chromosomów. Pomimo tej genetycznej różnorodności pojawił się spójny motyw: aktywność szlaku wzrostu i przetrwania skupionego na PI3K i AKT wzrastała w modelach opornych, często wraz z pokrewnymi trasami sygnalizacyjnymi, takimi jak MAPK i NF-κB.
Komórkowy przełącznik między „szybkim obejściem” a „wolną naprawą”
Pogłębiając analizę, badacze odkryli, że system PI3K/AKT działa jak przełącznik, który przełącza komórki nowotworowe między dwiema strategiami przetrwania. W trybie „szybkiego obejścia” wysoka aktywność PI3K/AKT unieszkodliwia białko hamujące FOXO3 i osłabia punkty kontrolne cyklu komórkowego, pozwalając komórkom dalej się dzielić i unikać śmiertelnych efektów adawoseribu lub paklitakselu. W kontrastującym trybie „wolnej naprawy” aktywność PI3K/AKT jest niższa, FOXO3 pozostaje aktywny w jądrze, a komórki zwalniają replikację, uruchamiają programy naprawy DNA i skuteczniej wypompowują leki. Co istotne, krótkotrwała ekspozycja na lek wywoływała gwałtowny wzrost aktywności PI3K/AKT we wszystkich modelach; długotrwała oporność ustalała się następnie w stanie albo szybkiego obejścia, albo wolnej naprawy, w zależności od podłoża genetycznego nowotworu i wcześniejszych sygnałów. To pokazuje, że ten sam centralny węzeł może wspierać bardzo różne drogi ucieczki. 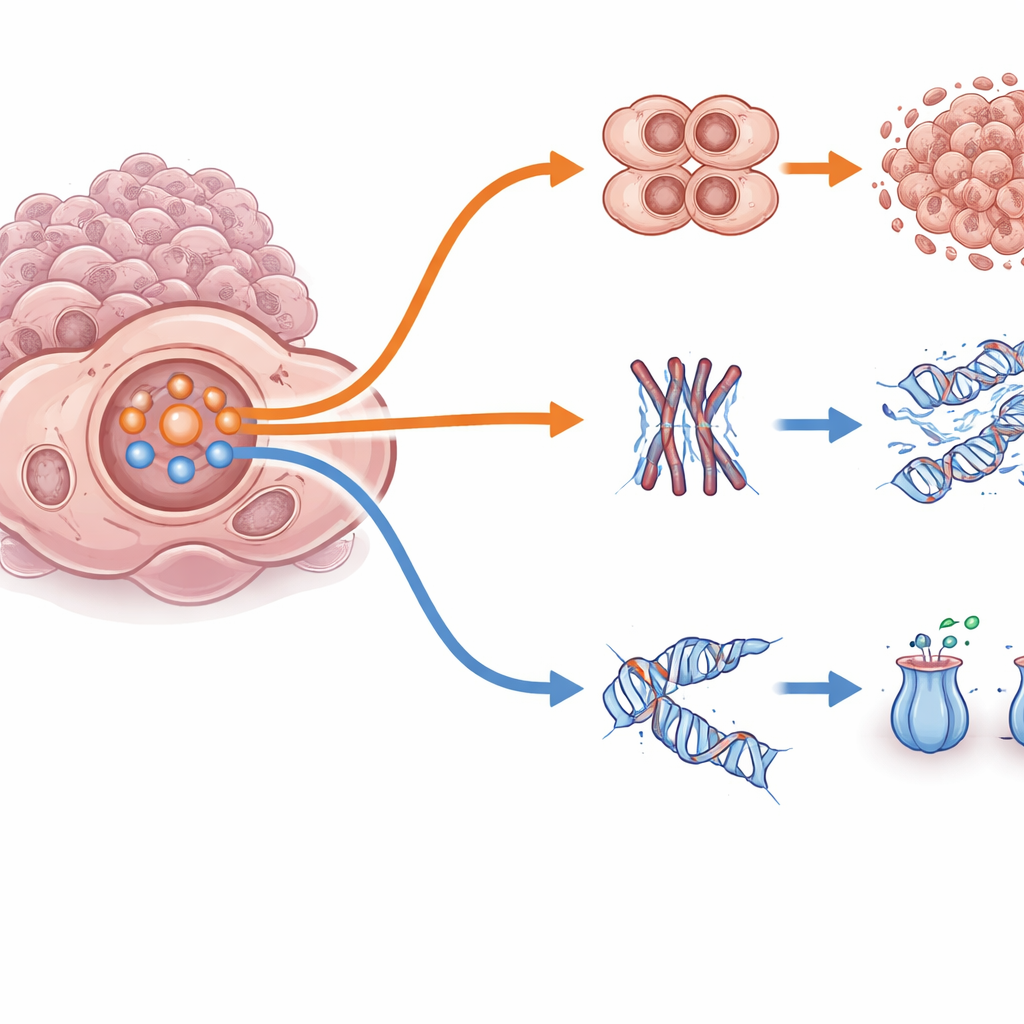
Przekształcenie sygnału oporności w cel terapeutyczny
Kluczowym górnym elementem tego węzła jest ROR1, receptor zwykle rzadki w normalnych tkankach dorosłych, ale podwyższony w kilku nowotworach. W wielu modelach opornych raka jajnika poziomy ROR1 wzrastały wraz z aktywnością PI3K/AKT. Zespół wykazał, że regulacja ROR1 w górę lub w dół może zmieniać skłonność komórek do nabywania oporności na adawoserib lub paklitaksel, w sposób zależny od kontekstu. Najważniejsze, że przetestowali zilovertamab-wedotin, sprzężoną przeciwciało–lek, która celuje w ROR1 i dostarcza toksyczny ładunek. Zarówno w liniach komórkowych, jak i w 3D organoidach pochodzących od pacjentów, guzy o wysokim poziomie ROR1 odporne na adawoserib były szczególnie wrażliwe na ten środek, a łączenie go z adawoseribem często zwiększało zabijanie komórek. Niektóre modele odporne na paklitaksel były mniej podatne, prawdopodobnie dlatego, że wzmocniły także swoją zdolność do wydalania leków.
Co to oznacza dla przyszłego leczenia raka jajnika
Ta praca przedefiniowuje oporność na leki w raku jajnika z mutacją TP53 nie jako zdarzenie przypadkowe, lecz jako skoordynowaną odpowiedź rządzoną przez centralny przełącznik sygnalizacyjny. Identyfikując oś PI3K/AKT–FOXO3 oraz ROR1 jako kluczowe węzły, badanie wskazuje praktyczne strategie: łączenie leków celujących na mitozy, takich jak adawoserib i paklitaksel, z terapiami blokującymi hub oporności lub wykorzystującymi ROR1 na komórkach opornych. Ponieważ ROR1 jest w dużej mierze nieobecny w zdrowych tkankach, takie kombinacje mogłyby selektywnie atakować nawrotowe, uodpornione guzy, oszczędzając komórki normalne. Chociaż wyniki pochodzą z modeli laboratoryjnych i hodowli pochodzących od pacjentek, a nie z zakończonych badań klinicznych, oferują jasną mapę drogową do projektowania mądrzejszych, trwalszych terapii dla kobiet z rakiem surowiczym wysokiego stopnia złośliwości.
Cytowanie: Raivola, J., Rantanen, F., Dini, A. et al. ROR1-PI3K/AKT signaling drives adaptive resistance to cell cycle blockade in TP53 mutated ovarian cancer. Cell Death Dis 17, 276 (2026). https://doi.org/10.1038/s41419-026-08501-x
Słowa kluczowe: rak jajnika, oporność na leki, szlak PI3K AKT, terapia przeciwciałem przeciw ROR1, inhibitory cyklu komórkowego