Clear Sky Science · pl
ERRα-KDM5C ogranicza aktywność wzmacniacza STING, modulując sygnalizację interferonów typu I w progresji raka piersi
Powstrzymanie komórek nowotworowych przed ukrywaniem się
Komórki nowotworowe robią więcej niż tylko niekontrolowanie się namnażają — uczą się także ukrywać przed układem odpornościowym organizmu. W tym badaniu odkryto, jak niektóre komórki raka piersi przygłuszają ważny wewnętrzny system alarmowy, zwany szlakiem STING, który normalnie pomaga zaalarmować odporność o zagrożeniu. Zrozumienie tego „wyłącznika” może umożliwić naukowcom opracowanie nowych metod sprawiających, by guzy stały się bardziej widoczne dla układu odpornościowego i poprawić skuteczność istniejących terapii, w tym chemioterapii.
Komórkowy system alarmowy pod presją
Szlak STING działa jak wbudowany system bezpieczeństwa w naszych komórkach. Gdy wykrywane są uszkodzenia DNA lub sygnały przypominające infekcję wirusową, STING pomaga uruchomić interferony typu I — silne przekaźniki immunologiczne, które przyciągają obronne komórki, takie jak cytotoksyczne limfocyty T. Wiele nowotworów znajduje sposoby na uciszenie tego alarmu, co ułatwia im niekontrolowany wzrost. Autorzy tej pracy skupili się na komórkach raka piersi i zapytali: które molekuły odpowiadają za tłumienie STING i jak ta kontrola jest wbudowana w komórkowy „panel przełączników” w postaci wzmacniaczy — krótkich regionów DNA zwiększających aktywność pobliskich genów?
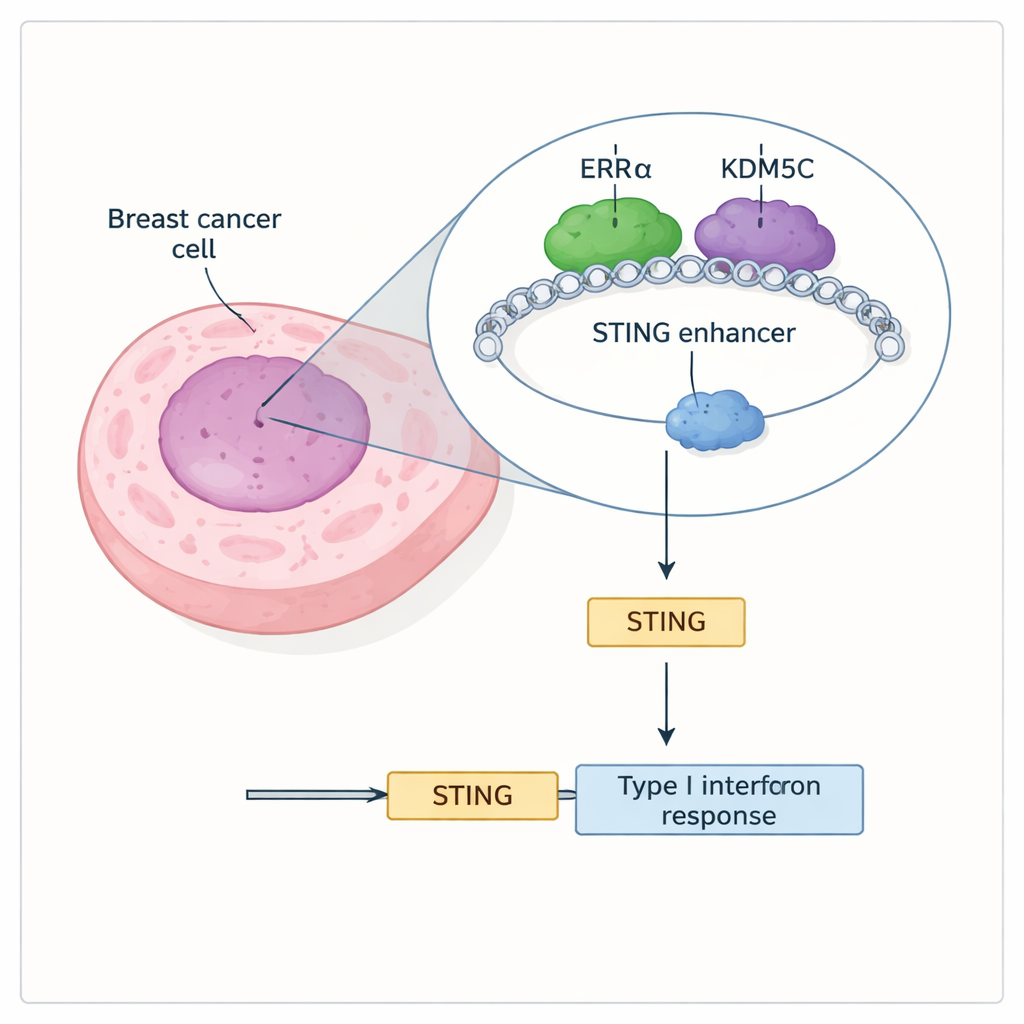
Dwie białka współpracują, by stłumić STING
Naukowcy odkryli, że receptor jądrowy o nazwie ERRα i enzym KDM5C fizycznie oddziałują ze sobą i współwystępują na wielu aktywnych regionach wzmacniaczy, w tym na wzmacniaczu kontrolującym gen STING. ERRα jest znany z tego, że pomaga komórkom nowotworowym przestawić metabolizm i opierać się apoptozie, natomiast KDM5C to „redaktor chromatyny”, który usuwa chemiczny znacznik (H3K4me3) związany z silną aktywacją genów. Na podstawie map wiązania w skali całego genomu zespół wykazał, że ERRα i KDM5C często współzajmują miejsca wzmacniaczy niosące markery wysokiej aktywności i produkujące RNA wzmacniaczy, co świadczy, że te przełączniki są włączone. W szczególności na wzmacniaczu STING obecne są oba białka, a ich obecność koreluje ze stłumioną aktywnością STING.
Uwolnienie hamulca sygnałów odpornościowych
Gdy badacze obniżyli poziomy ERRα lub KDM5C w komórkach raka piersi, wzmacniacz STING stał się nadaktywowany. Zwiększyły się chemiczne znaki związane z silną aktywacją, zmalały te związane ze stanem słabszej aktywności, a produkcja RNA wzmacniacza wzrosła. W ślad za tym nastąpił wzrost poziomu mRNA i białka STING oraz silniejsza aktywacja jego dalszego szlaku, w tym TBK1 i IRF3 — kluczowych białek przekaźnikowych napędzających produkcję interferonów typu I. W rezultacie komórki zaczęły wyrażać wyższe poziomy interferonów i genów stymulowanych interferonami, które są centralne dla obrony przeciwwirusowej i odporności przeciwnowotworowej. Innymi słowy, usunięcie ERRα lub KDM5C przemieniło stłumiony alarm w głośną syrenę wewnątrz komórek nowotworowych.
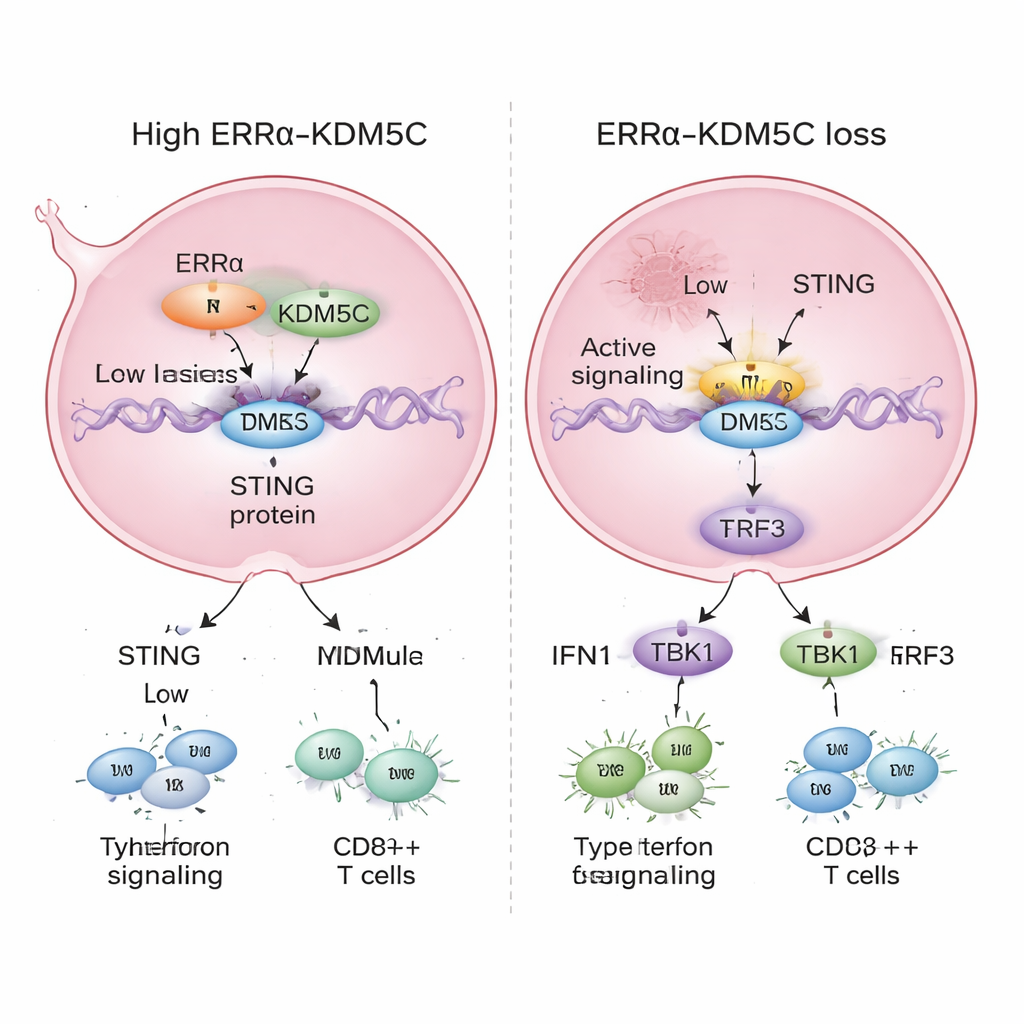
Spowolnienie wzrostu guza i zwiększenie efektywności terapii
Te molekularne zmiany miały wyraźny wpływ na zachowanie komórek nowotworowych. Komórki raka piersi z obniżonym poziomem ERRα lub KDM5C rosły wolniej i tworzyły mniej kolonii w hodowlach. W modelach mysich guzy pochodzące z komórek pozbawionych ERRα były mniejsze i lżejsze, co wskazuje na osłabiony wzrost in vivo. Co ważne, kiedy STING także został wyciszony, wiele z tych efektów hamujących wzrost zostało odwróconych, pokazując, że aktywacja STING jest kluczową częścią mechanizmu, dzięki któremu utrata ERRα i KDM5C ogranicza guzy. Zespół przetestował także lek chemioterapeutyczny etopozyd, który powoduje uszkodzenia DNA znane z aktywowania STING. Zablokowanie ERRα zwiększyło skuteczność etopozydu w zmniejszaniu guzów, sugerując, że poluzowanie tego hamulca sprawia, iż standardowe terapie działają lepiej poprzez wzmocnienie sygnałów stymulujących odporność.
Co to oznacza dla pacjentów
Analiza danych pacjentów ujawniła, że poziomy ERRα są wyższe w ludzkich nowotworach piersi niż w normalnej tkance piersiowej, a wysoka ekspresja ERRα wiąże się z gorszym przeżyciem i mniejszą liczbą przeciwnowotworowych komórek CD8+ T wewnątrz guzów. Podsumowując, praca przedstawia jasny obraz: ERRα i KDM5C tworzą moduł kontrolny, który utrzymuje alarm STING w stanie uśpienia, pomagając guzom piersiowym rosnąć i unikać ataku immunologicznego. Dla laika kluczowy przekaz jest taki, że niektóre raki piersi korzystają z tego duetu, by ukryć się przed obroną organizmu. Celowanie w ERRα, KDM5C lub ich więź z wzmacniaczem STING może pomóc „odkryć” guzy, wzmocnić odpowiedź immunologiczną i zwiększyć siłę działania istniejących terapii.
Cytowanie: Xu, ZH., Chen, J., He, Y. et al. ERRα-KDM5C restrains STING enhancer activity to modulate type I interferon signaling in breast cancer progression. Cell Death Dis 17, 228 (2026). https://doi.org/10.1038/s41419-026-08499-2
Słowa kluczowe: rak piersi, szlak STING, interferon typu I, regulacja epigenetyczna, odporność przeciwnowotworowa