Clear Sky Science · pl
tłumienie autofagii napędzane przez mTOR definiuje podatność metaboliczną w raku piersi opornym na inhibitory CDK4/6 HR+/HER2−
Dlaczego to ma znaczenie dla pacjentek z rakiem piersi
Wiele kobiet z zaawansowanym rakiem piersi żyje dziś dłużej dzięki lekom zwanym inhibitorami CDK4/6, które spowalniają tempo podziałów komórek nowotworowych. Niestety większość guzów z czasem uczy się unikać działania tych leków. To badanie stawia obiecujące pytanie: czy gdy rak piersi staje się oporny na inhibitory CDK4/6, zyskuje nową słabość, którą lekarze mogliby wykorzystać przy pomocy istniejących, stosunkowo prostych leków metabolicznych, takich jak metformina czy dichlorooctan (DCA)?
Gdy leki hamujące cykl komórkowy przestają działać
Lekarze często leczą najczęstszy typ raka piersi — nowotwór z receptorami hormonalnymi dodatnimi i ujemnym HER2 — terapią hormonalną w połączeniu z inhibitorami CDK4/6, takimi jak palbocyklib czy ribocyklib. Leki te celują w białka napędzające cykl podziałowy komórek. Z czasem jednak niektóre komórki nowotworowe adaptują się i stają się silnie oporne, nadal rosnąc nawet przy wysokich dawkach leków. Badacze odtworzyli ten problem w laboratorium, eksponując linie komórkowe raka piersi (T47D i MCF7) na stopniowo rosnące stężenia inhibitorów CDK4/6. Otrzymali dwie grupy przetrwałych komórek: komórki częściowo oporne oraz mniejszą grupę wysoce opornych klonów, które przestały dobrze reagować na leczenie.
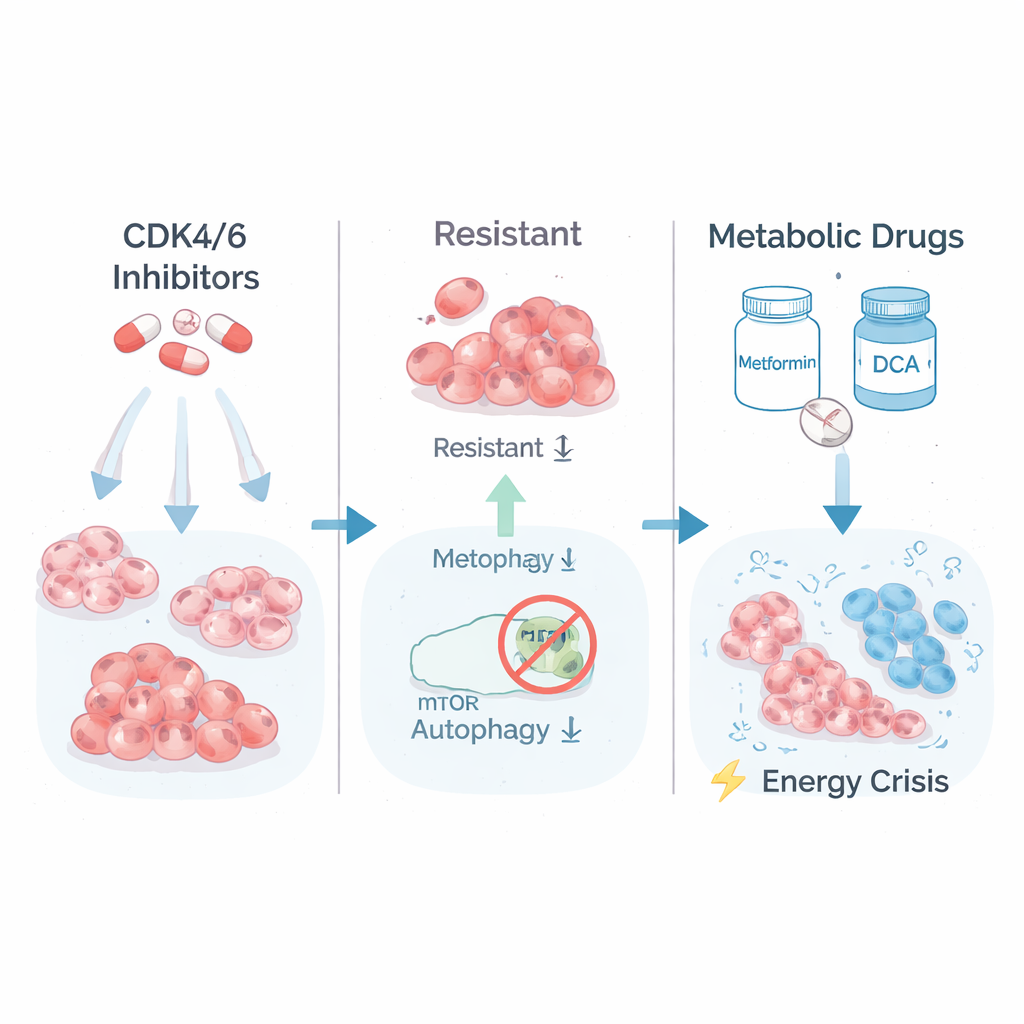
Ukryta słabość w wykorzystaniu energii przez guz
Aby zrozumieć, co wyróżniało wysoce oporne komórki, zespół przeanalizował, które geny były włączone lub wyłączone. Stwierdzili, że najbardziej oporne komórki nasilają szlaki związane z rozkładem cukrów (glikolizą) oraz sygnalizacją wzrostu kontrolowaną przez kompleks białkowy mTORC1. Innymi słowy, te komórki funkcjonowały na wysokich obrotach, spalając paliwo w szybkim tempie, by utrzymać wzrost. Naukowcy sprawdzili następnie, czy tę „wysokobiegową” gospodarkę metaboliczną można obrócić przeciwko komórkom. Leczyli komórki oporne i rodzicielskie metforminą — powszechnym lekiem przeciwcukrzycowym, który obciąża „fabryki energii” komórki — oraz DCA, który zmusza komórki do bardziej efektywnego przetwarzania paliwa. Co uderzające, najbardziej oporne klony okazały się wtedy najbardziej podatne: ich długoterminowy wzrost w hodowlach upadł pod wpływem terapii metabolicznej, podczas gdy komórki rodzicielskie i tylko częściowo oporne były znacznie mniej dotknięte.
Zablokowane samoczyszczenie i załamanie energetyczne
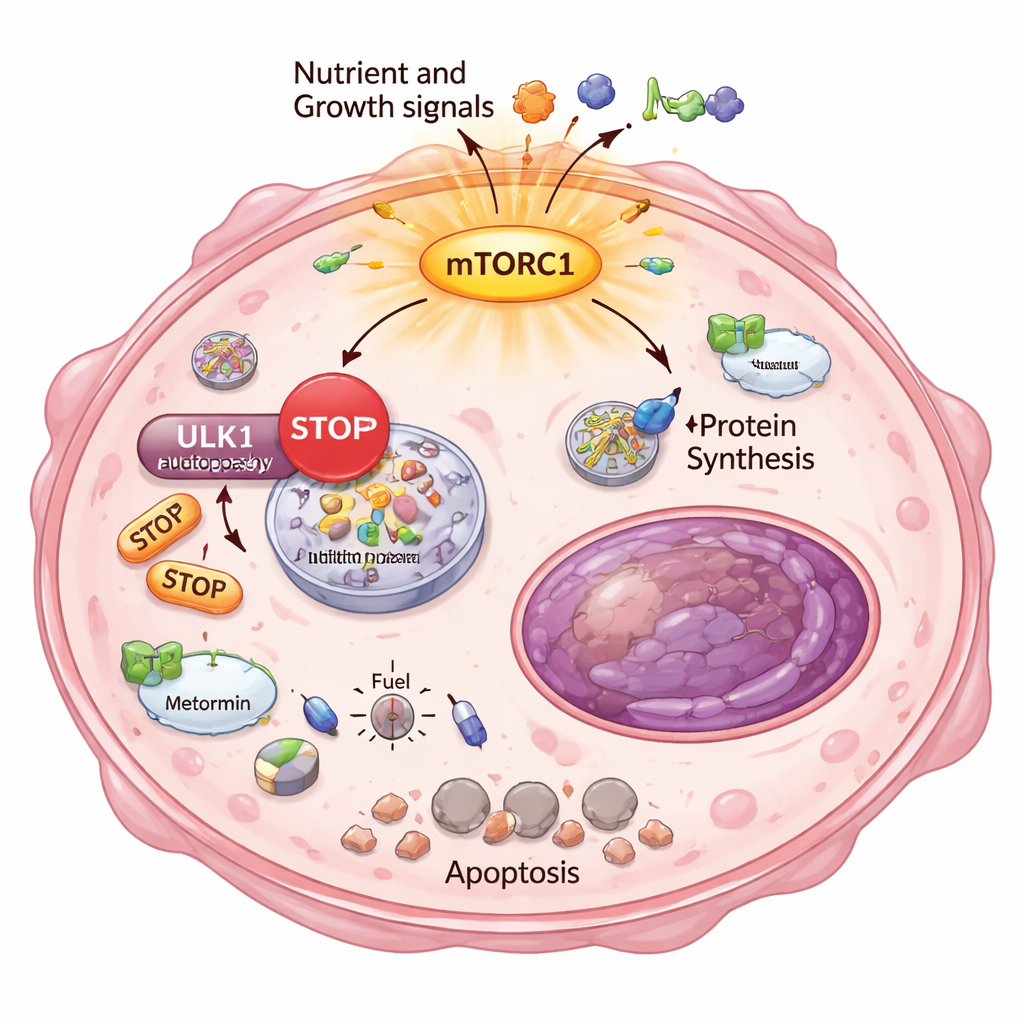
Dlaczego te uciekające komórki nowotworowe były tak wrażliwe na stres energetyczny? Odpowiedź tkwiła w innym podstawowym procesie przetrwania: autofagii, wbudowanym systemie „recyklingu i sprzątania” komórki. Normalnie, gdy energia jest niska, komórki rozkładają i ponownie wykorzystują własne komponenty, by przeżyć. Badacze wykazali, że w wysoce opornych klonach mTORC1 był nadaktywowany i nałożył chemiczny hamulec na ULK1, kluczowy inicjator autofagii. Przy użyciu czułego testu reporterowego pokazali, że te komórki nie potrafiły prawidłowo włączać ani zwiększać autofagii, nawet po pobudzeniu lekami metabolicznymi. W rezultacie metformina i DCA wywołały poważny kryzys energetyczny: aktywowały się sensory niskiej energii, zahamowana została synteza tłuszczów, a w wyraźnie opornych komórkach pojawiły się markery nieodwracalnej śmierci komórkowej.
Dane z prawdziwych guzów pacjentek
Modele laboratoryjne nie zawsze odzwierciedlają to, co dzieje się u pacjentów, więc zespół sięgnął po próbki ludzkich guzów piersi. Zabarwili ponad sto nowotworów na obecność markera aktywności mTORC1 (sfałdowanej fosforylowanej 4E-BP1) oraz p62, białka kumulującego się przy zablokowanej autofagii. Guzy wykazujące wysoką aktywność mTORC1 miały tendencję do większej zawartości p62, co wspiera hipotezę, że wzorzec „nadmiernego sygnału wzrostu i upośledzonego recyklingu” istnieje w rzeczywistych rakach piersi, a nie tylko w liniach komórkowych. To sugeruje, że u podzbioru pacjentek mogą występować guzy z tą samą metaboliczną słabością widoczną w laboratorium.
Co to może znaczyć dla przyszłych terapii
Dla osoby niebędącej specjalistą kluczowy wniosek jest taki, że gdy raki piersi ewoluują, by uciec przed silnymi inhibitorami CDK4/6, mogą także popaść w metaboliczny narożnik. Trwale włączając sygnały wzrostu i wyłączając komórkowy recykling, te guzy stają się silnie zależne od stałego dopływu energii. Badanie pokazuje, że tę konfigurację można wykorzystać za pomocą leków metabolicznych, takich jak metformina i DCA, które są już dobrze znane w innych chorobach. Co ważne, autorzy proponują, że proste testy tkankowe na aktywność mTORC1 i markery autofagii mogłyby pomóc zidentyfikować pacjentki, których oporne guzy są podatne na tego typu metaboliczny atak, otwierając drogę do bardziej spersonalizowanych terapii ratunkowych po nieskuteczności inhibitorów CDK4/6.
Cytowanie: von Wichert, L., Stroh, A., Witt, M. et al. mTOR-driven autophagy suppression defines metabolic vulnerability in CDK4/6 inhibitor-resistant HR+/HER2− breast cancer. Cell Death Dis 17, 235 (2026). https://doi.org/10.1038/s41419-026-08496-5
Słowa kluczowe: rak piersi, oporność na inhibitory CDK4/6, mTOR, autofagia, terapia metaboliczna