Clear Sky Science · pl
Zmiana splicingu onkogennego izoformy BCS1L hamuje postęp raka jajnika przez zakłócenie funkcji mitochondrialnej
Elektrownie wewnątrz komórek nowotworowych
Każda komórka w naszym ciele polega na drobnych elektrowniach zwanych mitochondriami. Komórki nowotworowe, które szybko rosną i rozsiewają się, szczególnie potrzebują energii. W tym badaniu odkryto, w jaki sposób rak jajnika przestawia jednego ze swoich kluczowych pomocników mitochondrialnych i pokazano, że delikatne przełączenie molekularnego „włącznika” na tym białku może wyzyskać guzy z energii, jednocześnie w dużej mierze oszczędzając tkanki zdrowe.
Dlaczego guzy polegają na swoich silnikach
Komórki raka jajnika, podobnie jak wiele innych nowotworów, potrafią elastycznie korzystać z różnych źródeł energii. Przeszukując obszerne bazy danych pacjentów i profile na poziomie pojedynczych komórek, badacze stwierdzili, że wiele guzów jajnika funkcjonuje z mitochondriami ustawionymi na wysokie obroty, znane jako fosforylacja oksydacyjna, czyli OXPHOS. Guzy z podwyższoną aktywnością mitochondrialną były bardziej agresywne i częstsze w zaawansowanych stadiach choroby. Spośród wielu białek budujących maszynerię energetyczną mitochondriów wyróżnił się jeden: BCS1L, chaperon pomagający w składaniu Kompleksu III, centralnego węzła w mitochondrialnym łańcuchu energetycznym. Guzy o wysokim OXPHOS i niektóre podtypy komórek nowotworowych wykazywały szczególnie silną aktywność BCS1L, co sugeruje, że komórki raka mocno polegają na tym pomocniku, by utrzymać swoje „silniki” w ruchu.
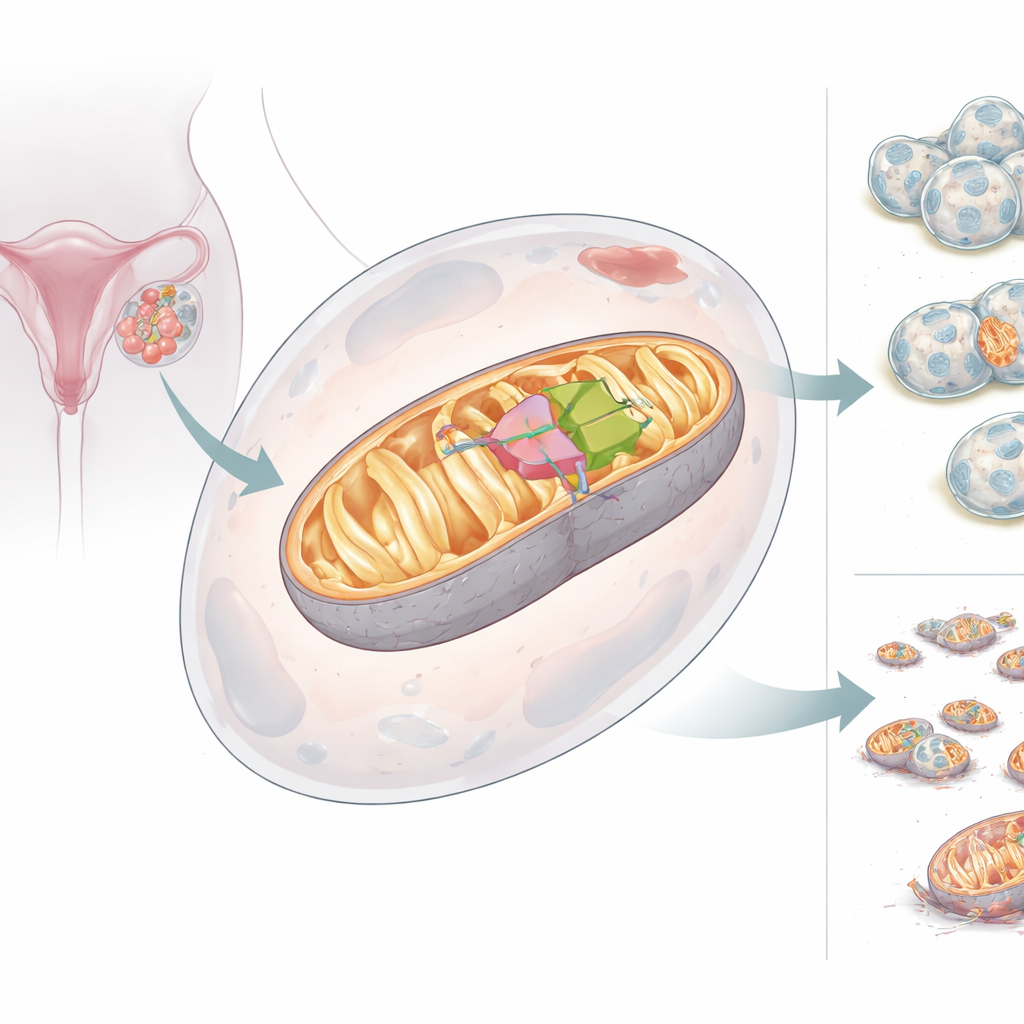
Dwie twarze mitochondrialnego pomocnika
Zespół odkrył, że gen BCS1L może produkować dwie wersje, czyli izoformy, swojego białka. Forma pełnej długości, BCS1L-L, zawiera sygnał kierujący ją do mitochondriów, gdzie wspiera prawidłowe składanie Kompleksu III i silną produkcję energii. Krótsza forma, BCS1L-S, pozbawiona kluczowego fragmentu, nie może dotrzeć do mitochondriów; zamiast tego pozostaje w cytoplazmie i jądrze komórkowym i nie wspiera produkcji energii. W tkankach zdrowych krótsza wersja jest powszechna, natomiast w raku jajnika równowaga się odwraca: dominuje długa, związana z mitochondriami forma. Gdy komórkom wymuszano produkcję większej ilości BCS1L-L, ich mitochondria wytwarzały więcej energii, utrzymywały silniejszy potencjał błonowy, produkowały mniej szkodliwych produktów ubocznych tlenu i były bardziej odporne na apoptozę. Przy zmniejszeniu poziomu BCS1L mitochondria ulegały fragmentacji, produkcja energii spadała, rosły poziomy szkodliwych form tlenu, a komórki nowotworowe częściej ginęły.
Jak nowotwór przepina komunikat
Produkcja wersji długiej lub krótkiej BCS1L zależy od tego, jak komórka edytuje swój komunikat w postaci RNA, procesu zwanego splicingiem. Badacze poszukiwali białek wiążących RNA BCS1L i wpływających na ten wybór. Skoncentrowali się na USP39, czynniku splicingowym już powiązanym z kilkoma nowotworami. W komórkach raka jajnika USP39 wiąże się w pobliżu odcinka RNA, który stanie się eksonem 2 BCS1L i sprzyja jego włączeniu, preferując w ten sposób długą, kierowaną do mitochondriów wersję. Gdy wyciszano USP39, komórki częściej pomijały ten fragment, przesuwając równowagę w stronę krótszej formy BCS1L-S. Ta zmiana osłabiała Kompleks III, redukowała oddychanie mitochondrialne i produkcję ATP, zwiększała stres oksydacyjny i indukowała śmierć komórek nowotworowych. Przywrócenie BCS1L-L w tych komórkach uratowało dużą część funkcji mitochondrialnych i przeżycia, co pokazuje, że USP39 napędza krytyczny mitochondrialny włącznik w dużej mierze przez wpływ na BCS1L.
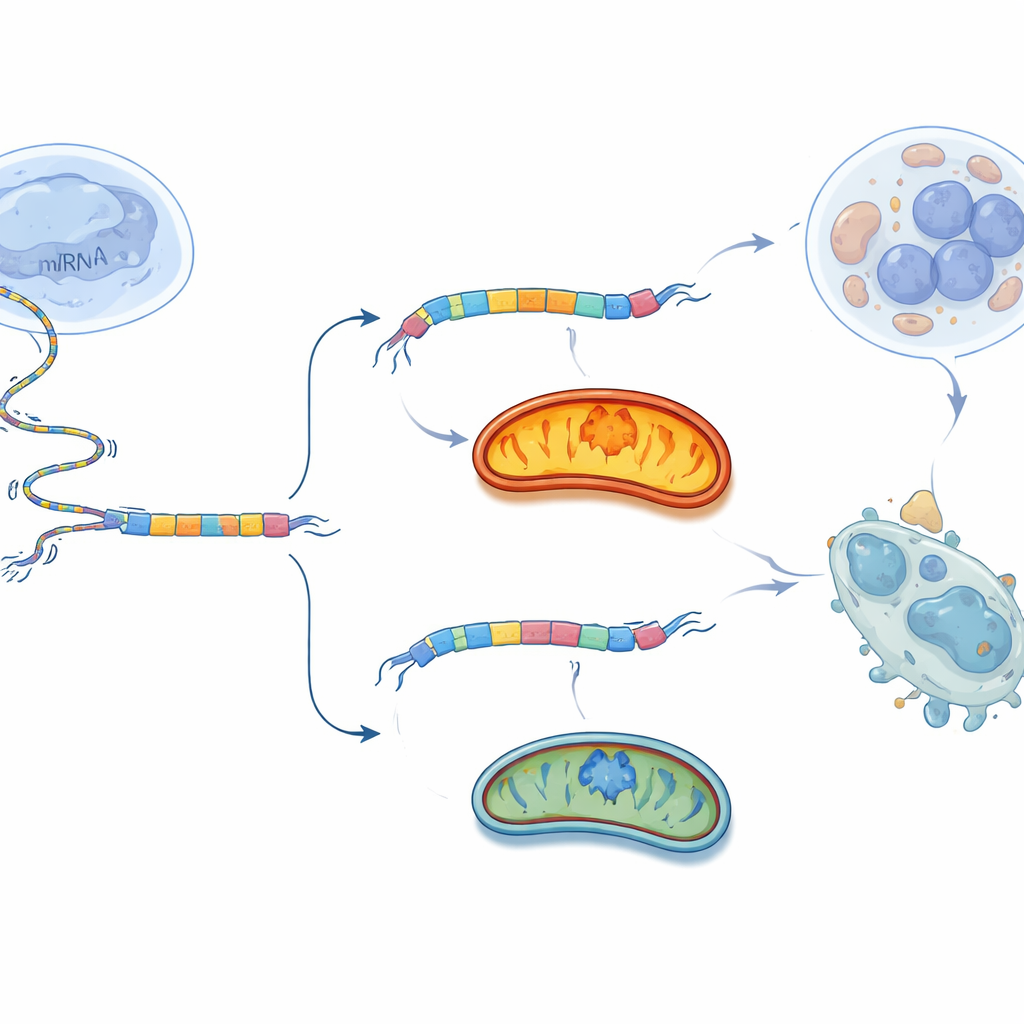
Wykorzystanie przełącznika przeciwko guzowi
Zamiast szeroko blokować mitochondria, co mogłoby zaszkodzić wielu tkankom, zespół zastosował bardziej chirurgiczne podejście: manipulację wyborem splicingu samego BCS1L. Zaprojektowali krótkie fragmenty materiału genetycznego zwane oligonukleotydami antysensownymi (ASO), które wiążą się tuż wokół eksonu 2 RNA BCS1L. Te ASO działają jak maleńkie klamerki, zmieniając sposób, w jaki maszyneria splicingowa odczytuje komunikat i zachęcając komórkę do pominięcia eksonu 2. W hodowlach komórek raka jajnika najlepszy ASO silnie zmniejszał formę długą BCS1L-L i zwiększał formę krótką BCS1L-S. W efekcie oddychanie mitochondrialne i produkcja ATP spadły, wzrosły poziomy szkodliwych form tlenu, a znacznie więcej komórek przeszło zaprogramowaną śmierć. Gdy ten sam ASO wstrzyknięto do guzów raka jajnika u myszy, wzrost nowotworu spowolnił, a guzy ważyły mniej, przy czym efekt był znacznie silniejszy w komórkach nowotworowych niż w normalnych fibroblastach.
Co to może oznaczać dla pacjentów
W prostych słowach, praca ta pokazuje, że wiele raków jajnika polega na „turbo” wersji pomocniczego białka mitochondrialnego, by napędzać swój wzrost. Czynnik splicingowy USP39 przechyla maszynerię edycji RNA komórki tak, by powstawało więcej tej turbo-wersji, utrzymując mitochondria guza w doskonałej kondycji. Poprzez zastosowanie precyzyjnie zaprojektowanych ASO, które przełączają wybór splicingu z powrotem na słabszą wersję, badacze mogą selektywnie osłabić mitochondria komórek nowotworowych, wywołując ich śmierć przy relatywnie mniejszym wpływie na większość komórek normalnych. Chociaż dostarczanie takich leków ASO do guzów pozostaje poważnym wyzwaniem, badanie to wskazuje na przełącznik splicingu BCS1L jako obiecujący i wysoce specyficzny cel terapeutyczny w leczeniu raka jajnika.
Cytowanie: Xu, M., Wang, Z., Yang, S. et al. Splice-switching of the oncogenic BCS1L isoform suppresses ovarian cancer progression by disrupting mitochondrial function. Cell Death Dis 17, 293 (2026). https://doi.org/10.1038/s41419-026-08495-6
Słowa kluczowe: rak jajnika, mitochondria, splicing RNA, BCS1L, oligonukleotydy antysensowne