Clear Sky Science · pl
NSD2 hamuje ekspresję PD-L1 poprzez fosforylację oksydacyjną, kontrolując nadzór immunologiczny w raku wątrobowokomórkowym
Dlaczego ta historia o raku wątroby ma znaczenie
Rak wątrobowokomórkowy, najczęstsza postać nowotworu wątroby, bywa rozpoznawany późno i jest oporny na wiele terapii. Leki immunoterapeutyczne blokujące „pelerynę niewidzialności” PD-L1 na komórkach nowotworowych pomagają niektórym pacjentom, lecz większości nie. W tym badaniu odkryto nietypowego uczestnika, białko nazwane NSD2, które łączy sposób, w jaki komórki raka wątroby wytwarzają energię, z ich rozpoznawalnością przez układ odpornościowy. Zrozumienie tego powiązania może wskazać nowe sposoby wzmocnienia istniejących terapii i pomóc identyfikować pacjentów, którzy najprawdopodobniej skorzystają.
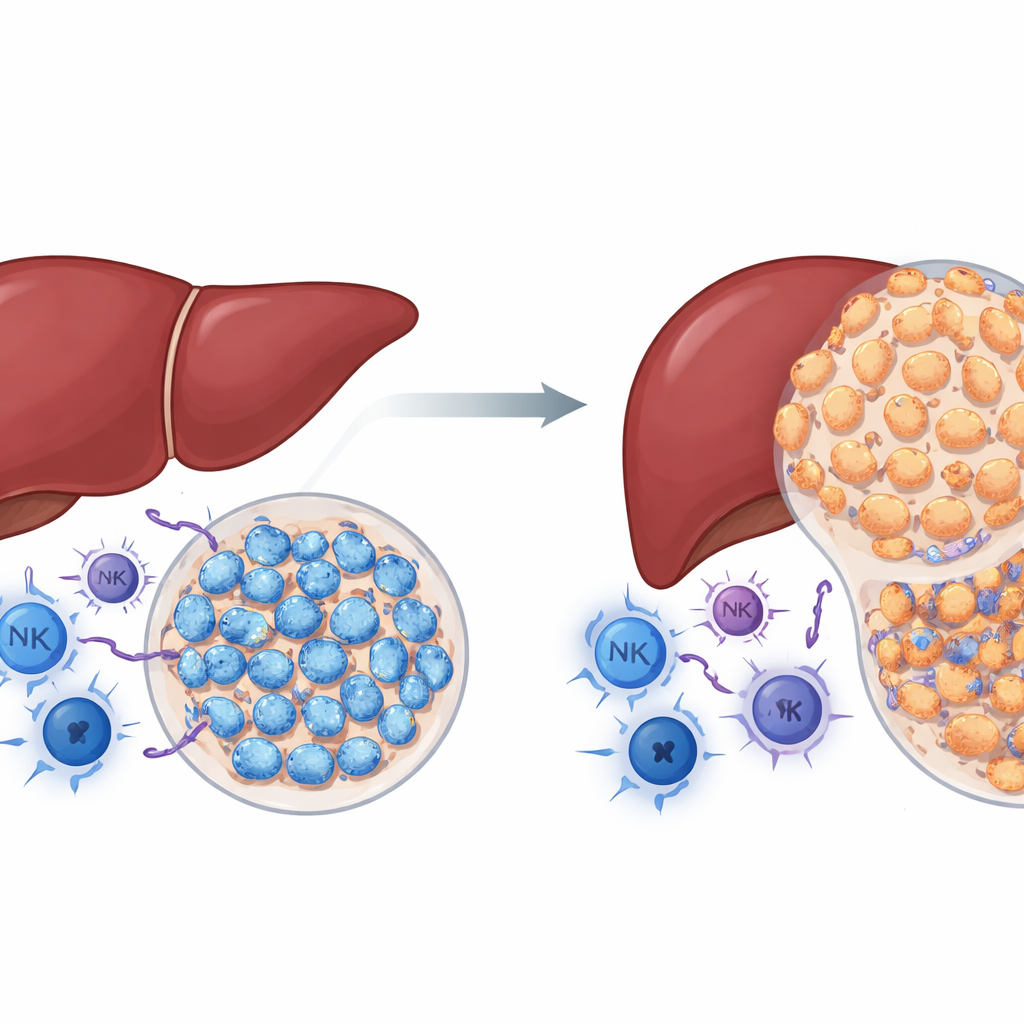
Zaskakująca rola znanego białka nowotworowego
NSD2 jest enzymem modyfikującym histony, białka, wokół których owinięte jest DNA. W wielu nowotworach NSD2 bywa postrzegane jako czynnik napędzający wzrost guza. Autorzy postawili pytanie, czy tak jest również w raku wątroby. Używając genetycznie zmodyfikowanych myszy, w których NSD2 jest aktywowany specyficznie w komórkach wątroby, poddali zwierzęta działaniu chemicznego czynnika wywołującego guzy wątroby. Wbrew oczekiwaniom myszy z nadekspresją NSD2 rozwijały znacznie mniej i mniejsze guzy niż myszy kontrolne, a ich wątroby wykazywały mniejsze uszkodzenie, bliznowacenie i proliferację komórek. Jednocześnie guzy z wątroby z nadekspresją NSD2 zawierały więcej komórek odpornościowych walczących z rakiem, w tym limfocytów T pomocniczych i zabójczych oraz komórek NK. Wyniki te sugerują, że w obecności sprawnego układu odpornościowego NSD2 zachowuje się mniej jak przyspieszacz, a bardziej jak hamulec rozwoju raka wątroby.
Fabryki energii i wykorzystanie paliwa w komórkach guzowych
Aby zrozumieć, jak NSD2 ogranicza guzy, zespół przeanalizował aktywność genów w tkance wątroby. Stwierdzili, że nadekspresja NSD2 silnie tłumi geny zaangażowane w fosforylację oksydacyjną — proces, w którym mitochondria, „elektrownie” komórki, wytwarzają energię z użyciem tlenu. Dalsze eksperymenty na liniach komórkowych raka wątroby myszy i człowieka pokazały, że zwiększenie poziomu NSD2 obniża ekspresję wielu genów fosforylacji oksydacyjnej, redukuje zużycie tlenu i produkcję ATP oraz obniża potencjał błony mitochondrialnej, co świadczy o osłabieniu aktywności mitochondriów. Jednocześnie komórki te zużywały mniej glukozy, ale nie przestawiały się na zwiększoną glikolizę, co wskazuje na łączny spadek wydajności energetycznej. Utrata NSD2 dawała efekty odwrotne, wzmacniając moc mitochondriów i wykorzystanie paliwa.
Jak NSD2 przebudowuje energetykę i widoczność immunologiczną
Zagłębiając się dalej, badacze połączyli genomowe mapowanie chromatyny z danymi ekspresji genów i zidentyfikowali zestaw genów bezpośrednio aktywowanych w obecności NSD2. Dwa z nich, Camk2d i Prkce, są znane jako hamujące aktywność mitochondrialną. NSD2 zwiększał obecność specyficznej modyfikacji histonu (H3K36me2) na ich promoterach, podnosząc ich ekspresję. Przywrócenie ekspresji tych genów w komórkach raka wątroby pozbawionych NSD2 zmniejszyło zużycie tlenu przez mitochondria i produkcję ATP, potwierdzając, że działają one jako dźwignie hamujące fosforylację oksydacyjną w szlaku NSD2. Co istotne, wcześniejsze badania sugerowały, że wysoce aktywne mitochondria sprzyjają wysokiej ekspresji PD-L1 na komórkach nowotworowych. Zgodnie z tymi obserwacjami autorzy stwierdzili, że nadekspresja NSD2 obniża poziomy PD-L1, podczas gdy utrata NSD2 podnosi PD-L1 na komórkach raka wątroby i w tkance guza.
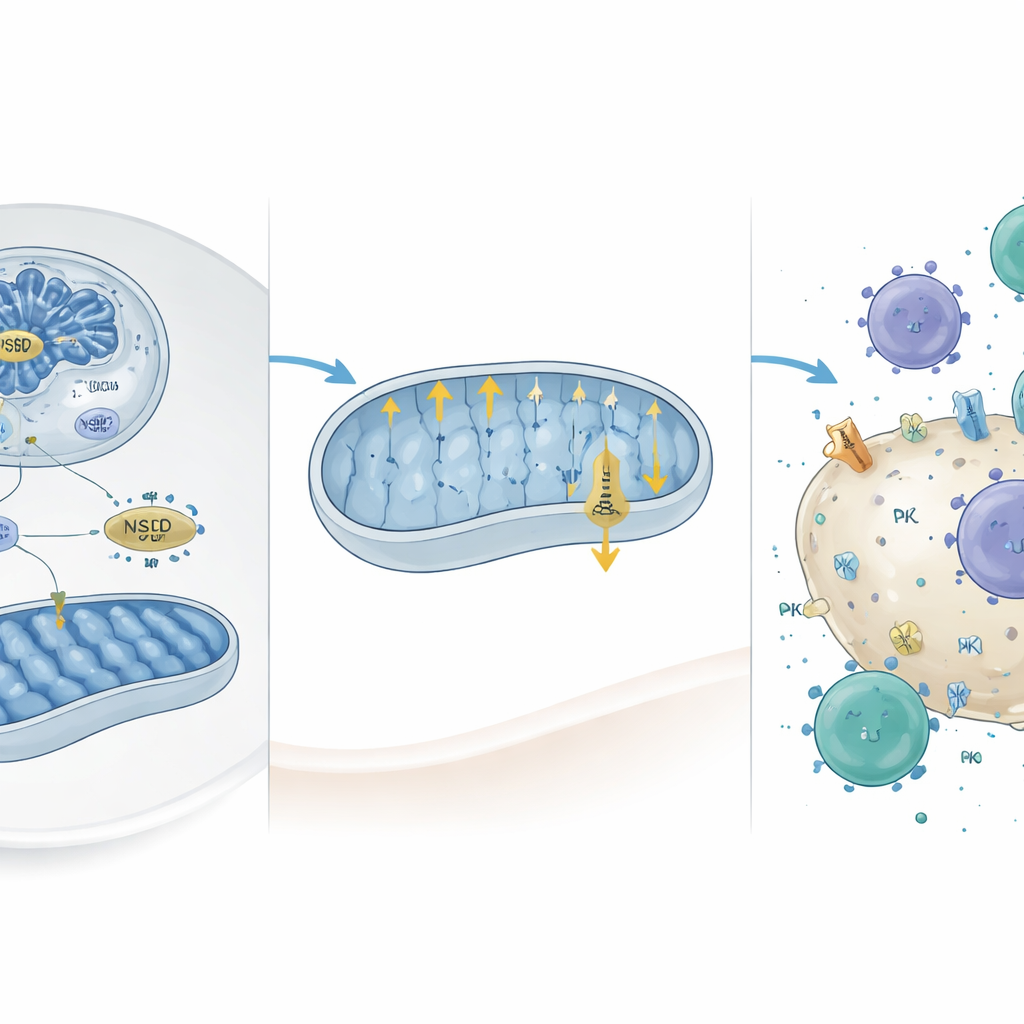
Ściszenie tarczy i pobudzenie ataku immunologicznego
Funkcjonalny wpływ tych molekularnych zmian testowano u myszy otrzymujących wstrzyknięcia do wątroby komórek nowotworowych zaprojektowanych tak, by zyskiwać lub tracić NSD2. Komórki pozbawione NSD2 szybko tworzyły większe guzy, wykazywały wyższą ekspresję PD-L1 i były mniej nacieczone przez limfocyty T i komórki NK, zwłaszcza aktywowane limfocyty T zabójcze. Gdy badacze chemicznie zablokowali kompleks V mitochondrium, kluczowy komponent fosforylacji oksydacyjnej, poziomy PD-L1 w komórkach pozbawionych NSD2 spadły w stronę normy, a komórki odpornościowe lepiej indukowały śmierć komórek nowotworowych. Podobnie, nadekspresja Camk2d lub Prkce w komórkach bez NSD2, albo leczenie guzów przeciwciałem blokującym PD-L1, zmniejszały rozmiar guza i przywracały nacieki komórek odpornościowych. W analizach zbiorów danych od pacjentów niska ekspresja NSD2 wiązała się z gorszym przeżyciem, ale, co ciekawe, z lepszą odpowiedzią na terapię celującą PD-L1, sugerując, że status NSD2 mógłby pomóc przewidywać, kto skorzysta z takich leków.
Co to oznacza dla przyszłej opieki nad rakiem wątroby
Dla czytelnika ogólnego najważniejsze jest to, że badanie przedefiniowuje NSD2 jako czynnik hamujący rozwój guza w raku wątroby, przynajmniej w obecności działającego układu odpornościowego. Poprzez ograniczenie tlenowej produkcji energii komórkowej NSD2 pośrednio obniża PD-L1 na komórkach nowotworowych, usuwając część ich „peleryny niewidzialności” i umożliwiając komórkom odpornościowym ich rozpoznanie i atak. Opisany łańcuch NSD2–energia–PD-L1 sugeruje dwie praktyczne koncepcje: po pierwsze, pacjenci, których guzy nie wykazują NSD2, mogą być szczególnie dobrymi kandydatami do leków blokujących PD-L1; po drugie, łączenie leków hamujących mitochondrialną produkcję energii z immunoterapią może stanowić skuteczne połączenie przeciw rakowi wątroby.
Cytowanie: Zhang, W., Feng, W., Ma, C. et al. NSD2 inhibits the expression of PD-L1 via oxidative phosphorylation to control immune surveillance in hepatocellular carcinoma. Cell Death Dis 17, 284 (2026). https://doi.org/10.1038/s41419-026-08490-x
Słowa kluczowe: rak wątrobowokomórkowy, NSD2, fosforylacja oksydacyjna, PD-L1, immunoterapia nowotworowa