Clear Sky Science · pl
Regulacja splicingu DDX39B zależna od SNRPD2 sprzyja progresji raka endometrium przez hamowanie aktywacji kryptycznych egzonic CTSC
Dlaczego ukryte komunikaty w genach nowotworowych mają znaczenie
Rak endometrium, powszechny nowotwór trzonu macicy, odnotowuje globalny wzrost zachorowań, a u wielu pacjentek z zaawansowaną chorobą wciąż brakuje skutecznych opcji leczenia. W badaniu tym ujawniono, jak subtelny proces wewnątrz komórek — sposób, w jaki wycinane i składane są informacje genetyczne — może napędzać wzrost i rozsiewanie się guzów endometrium. Odkrycie kruchego „schematu połączeń”, od którego zależą komórki nowotworowe, wskazuje nowe możliwości ich wyłączania przy użyciu precyzyjnych leków genetycznych.
Rosnący nowotwór potrzebujący nowych odpowiedzi
Rak endometrium jest obecnie najczęstszym nowotworem ginekologicznym w wielu krajach zachodnich, a liczba zachorowań i zgonów systematycznie rośnie zarówno na Zachodzie, jak i w Chinach. Stosuje się zabieg operacyjny, radioterapię, chemioterapię, leczenie hormonalne i immunoterapię, ale żadne z tych podejść nie jest doskonałe. Usunięcie macicy pozbawia płodności, terapie hormonalne często zawodzą, a agresywne guzy mają skłonność do nawrotów. Te wyzwania skłoniły badaczy do głębszego przyjrzenia się wnętrzu komórek nowotworowych w poszukiwaniu molekularnych słabych punktów, które można by zaatakować bardziej precyzyjnymi terapiami.
Maszyneria splicingu jako słabe ogniwo
Aby działać, nasze geny najpierw są przepisywane na długie cząsteczki RNA, które muszą zostać przycięte i zszyte w procesie zwanym splicingiem. Specjalistyczne kompleksy białkowe zwane spliceosomami decydują, które fragmenty są zachowywane, a które usuwane — w praktyce edytując scenariusz, z którego komórki syntetyzują białka. Zespół skupił się na komponencie spliceosomu o nazwie SNRPD2, należącym do rodziny białek „Sm”, które pomagają składać maszynerię splicującą. Analizując duże bazy danych genów i białek związanych z rakiem oraz próbki od pacjentek, badacze stwierdzili, że poziomy SNRPD2 są wyraźnie podwyższone w guzach endometrium w porównaniu z prawidłową błoną śluzową macicy, a pacjentki z wyższym SNRPD2 w guzach mają gorsze rokowanie.
Wyłączenie głównego redaktora spowalnia guzy
Aby sprawdzić, czy SNRPD2 jest jedynie obserwatorem, czy aktywnym sprawcą, badacze wyciszyli jego ekspresję w hodowlach komórek raka endometrium. Po wyhamowaniu SNRPD2 komórki dzieliły się wolniej, tworzyły mniej kolonii i miały mniejszą zdolność do migracji oraz inwazji przez membrany — cech związanych z przerzutowaniem. Gdy zmodyfikowane komórki wszczepiono myszom, powstałe guzy były znacznie mniejsze i zawierały mniej komórek będących w aktywnej fazie podziału. Co istotne, zespół zaprojektował oligonukleotydy antysensowne — krótkie, przypominające leki fragmenty syntetycznego DNA — które specyficznie celują w RNA SNRPD2. W modelu xenograftu pochodzącym od pacjentki, w którym fragmenty ludzkiego guza rosną w myszach z osłabionym układem odpornościowym, te leki antysensowne znacząco obniżyły poziom SNRPD2 i rozmiar guza, sugerując, że SNRPD2 może być terapeutycznie ukierunkowany w sposób mający znaczenie kliniczne.
Trzystopniowy łańcuch od błędu splicingu do wzrostu nowotworu
Badając dane genetyczne, naukowcy pytali, jak utrata SNRPD2 przebudowuje komunikaty RNA w całym genomie. Odkryli, że przy obniżonym SNRPD2 kluczowy enzym przetwarzania RNA, DDX39B, zaczyna działać wadliwie. Normalnie DDX39B pomaga usuwać określony intron — fragment RNA, który powinien zostać wycięty — z własnego przekazu. Przy niedoborze SNRPD2 ten intron pozostaje, tworząc wadliwą wersję RNA DDX39B, którą komórka szybko degraduje. Niższy poziom DDX39B wywołuje efekt domina na kolejny gen, CTSC, który koduje enzym proteolityczny znany z podtrzymywania wzrostu i rozprzestrzeniania się guza. W warunkach prawidłowych ukryty „kryptyczny” ekson w RNA CTSC jest pomijany, co pozwala komórkom wytwarzać pełnej długości, aktywne białko CTSC. Przy zmniejszonym DDX39B ten kryptyczny ekson jest omyłkowo włączany, wprowadzając przedwczesne sygnały stopu do RNA. Zniekształcony przekaz CTSC jest degradowany, zanim zdąży wytworzyć istotne ilości białka, a komórki nowotworowe tracą część swojej agresywności.
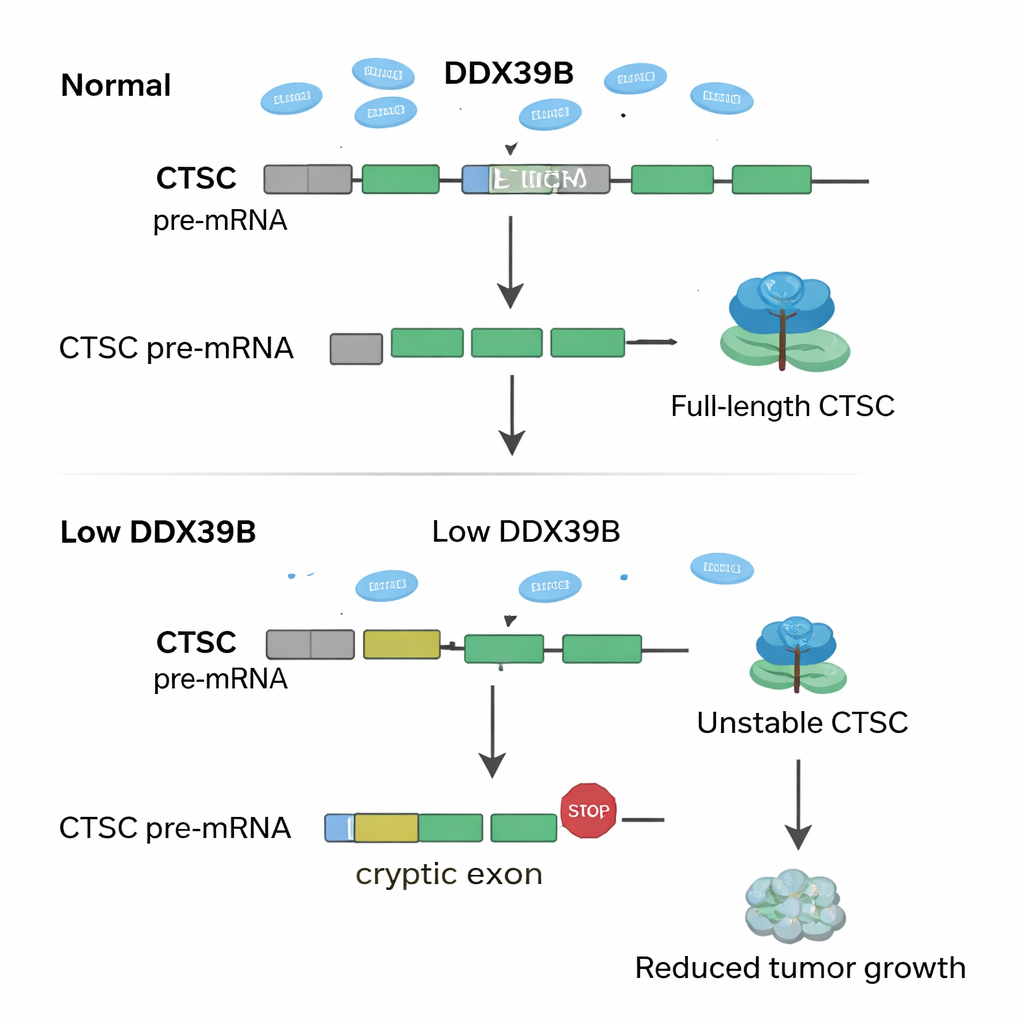
Co to oznacza dla przyszłych terapii
Mówiąc najprościej, autorzy odsłaniają system przekaźnikowy — SNRPD2 → DDX39B → CTSC — którego komórki raka endometrium używają, by przetrwać i rozwijać się. Wysokie SNRPD2 utrzymuje obfitość DDX39B; DDX39B z kolei zapobiega użyciu szkodliwych kryptycznych eksonów w CTSC, zachowując pełną funkcję białka CTSC, które wspiera wzrost i rozprzestrzenianie się guzów. Gdy SNRPD2 zostaje zablokowany, ten łańcuch się załamuje, poziomy CTSC spadają, a guzy słabną. Dla osób niezajmujących się tematem kluczowa idea jest taka, że komórki nowotworowe zależą od bardzo precyzyjnej edycji RNA i nawet drobne wymuszone „błędy” mogą selektywnie zatruć ich wzrost. Ukierunkowanie SNRPD2 za pomocą leków antysensownych albo bezpośrednie wymuszenie użycia kryptycznego eksonu w CTSC może dostarczyć nowych, bardziej dopasowanych terapii dla pacjentek z rakiem endometrium.
Cytowanie: Li, Y., Chen, Z., Liu, Y. et al. SNRPD2-mediated regulation of DDX39B splicing promotes endometrial cancer progression by suppressing the activation of CTSC cryptic exons. Cell Death Dis 17, 239 (2026). https://doi.org/10.1038/s41419-026-08489-4
Słowa kluczowe: rak endometrium, splicing RNA, SNRPD2, DDX39B, CTSC