Clear Sky Science · pl
DNMT2 hamuje rozwój anaplastycznego raka tarczycy poprzez obniżenie produkcji 5’tiRNAGly-GCC
Dlaczego ta ukryta chemia RNA ma znaczenie
Anaplastyczny rak tarczycy należy do najgroźniejszych nowotworów u ludzi, często zabijając pacjentów w ciągu kilku miesięcy pomimo zabiegów chirurgicznych, radioterapii i chemioterapii. Badanie to ujawnia zaskakującego sprawcę głęboko w komórkach nowotworowych: malutkie chemiczne modyfikacje na transferowym RNA, cząsteczkach pomagających w budowie białek. Autorzy wykazują, że gdy określony enzym, DNMT2, jest utracony lub zredukowany, guzy tarczycy rosną szybciej, łatwiej się rozprzestrzeniają i stają się odporne na powszechny lek chemioterapeutyczny doksorubicynę. Co jeszcze bardziej intrygujące, identyfikują mały fragment RNA, który pojawia się przy niskim poziomie DNMT2, i pokazują, że blokowanie tego fragmentu może stać się nową strategią terapeutyczną.
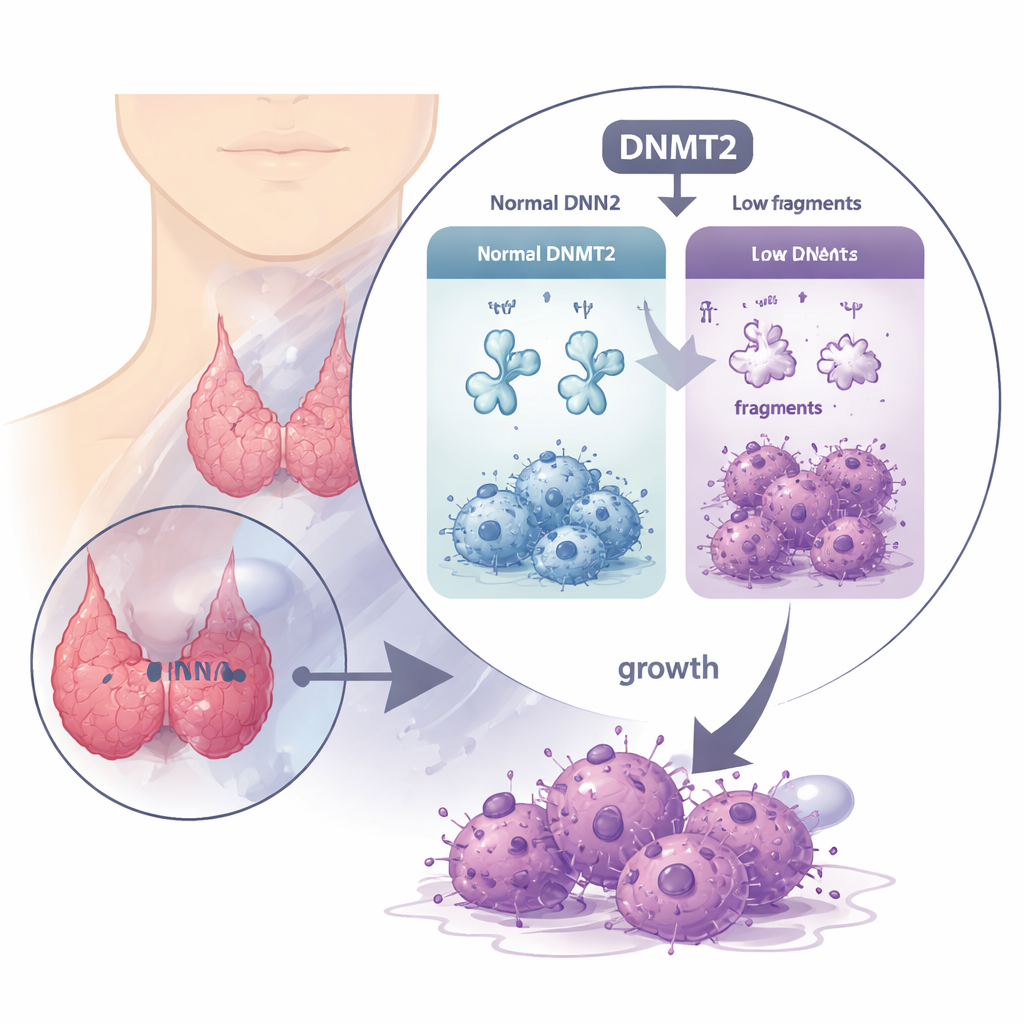
Ochronny enzym, który znika
tRNA zwykle przenoszą aminokwasy do komórkowego aparatu syntezy białek, a ich stabilność zależy od delikatnych chemicznych ozdób. DNMT2 to enzym, który dodaje jedną z takich modyfikacji — grupę metylową — w określonych miejscach tRNA. W wielu nowotworach poziom DNMT2 jest podwyższony i uważa się, że wspiera guzy, ale tutaj historia jest odwrotna. Analiza dużych baz danych pacjentów i próbek guzów wykazała, że poziomy DNMT2 są istotnie niższe w tkance anaplastycznego raka tarczycy niż w normalnej tarczycy. Pacjenci, których guzy miały wyższe stężenie DNMT2, zwykle żyli dłużej bez postępu choroby, co sugeruje, że DNMT2 działa raczej jak hamulec niż przyspieszacz w tej chorobie.
Jak niski poziom DNMT2 napędza agresywne zachowanie
Aby sprawdzić, co DNMT2 faktycznie robi w komórkach nowotworowych, zespół manipulował jego poziomami w liniach komórkowych anaplastycznego raka tarczycy hodowanych w naczyniach i w modelach mysich. Gdy DNMT2 był obniżony, komórki mnożyły się szybciej, łatwiej inwazowały przez membrany i tworzyły więcej kolonii — wszystkie cechy agresywnego guza. Komórki te stały się również mniej wrażliwe na doksorubicynę, standardowy lek stosowany w tym nowotworze. U myszy guzy z obniżonym DNMT2 rosły większe i częściej dały przerzuty do płuc, podczas gdy zwiększenie ekspresji DNMT2 miało odwrotny efekt. Badacze częściowo powiązali te zmiany z aktywacją programu komórkowego zwanego przejściem nabłonkowo-mezenchymalnym (EMT), które czyni komórki nowotworowe bardziej ruchliwymi i inwazyjnymi.
Z uszkodzonego tRNA do szkodliwych małych fragmentów
Głębsza analiza pokazuje, że DNMT2 umieszcza znak metylowy w określonej pozycji (zwanej C38) na zaledwie trzech typach tRNA. Bez tej ochrony tRNA stają się bardziej podatne na cięcie przez inny enzym — angiogeninę. To cięcie produkuje krótki fragment RNA pochodzący z tRNA-Gly-GCC, nazwany 5’tiRNAGly-GCC. Dzięki sekwencjonowaniu i testom biochemicznym autorzy odkryli, że przy niskim DNMT2 ten fragment się kumuluje, zwłaszcza pochodzący z tRNA transportującego glicynę. W eksperymentach in vitro dodanie grupy metylowej mocno chroniło tRNA przed rozcięciem, potwierdzając, że DNMT2 normalnie zabezpiecza te cząsteczki przed rozdrabnianiem na mniejsze, potencjalnie szkodliwe kawałki.
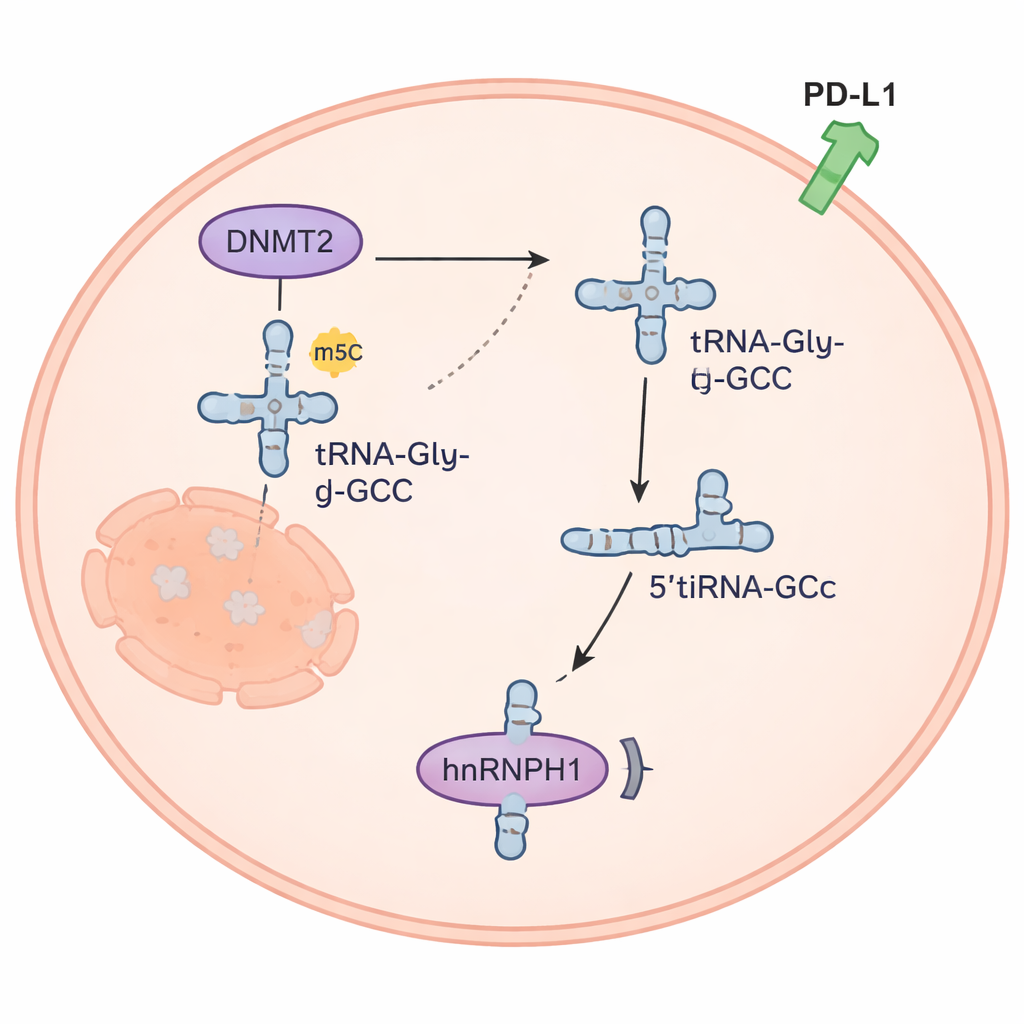
Maleńki fragment RNA przebudowuje sygnalizację nowotworu
Fragment 5’tiRNAGly-GCC okazał się czymś więcej niż odpadkiem molekularnym. Był obficie obecny w komórkach anaplastycznego raka tarczycy, ale rzadki w komórkach normalnej tarczycy. Gdy badacze sztucznie podnosili jego poziom, komórki nowotworowe proliferowały szybciej, inwazja narastała, a oporność na doksorubicynę wzrastała; obniżenie poziomu fragmentu dawało efekt przeciwny. U myszy chemicznie zaprojektowany inhibitor 5’tiRNAGly-GCC spowolnił wzrost guza, a łączenie tego inhibitora z doksorubicyną działało lepiej niż każde leczenie osobno. Zespół odkrył, że 5’tiRNAGly-GCC wiąże się z białkiem hnRNPH1, zmniejszając jego ilość w komórkach. Ponieważ hnRNPH1 normalnie pomaga utrzymywać na niskim poziomie białko związane z układem odpornościowym PD-L1, utrata hnRNPH1 pozwala PD-L1 wzrosnąć — zmiana, która może pomóc guzom uniknąć ataku immunologicznego i wiąże się z nagromadzeniem regulatorowych komórek T wokół guzów.
Co to oznacza dla przyszłych terapii
Mówiąc prosto, badanie ujawnia reakcję łańcuchową: gdy DNMT2 jest niski, niektóre tRNA tracą ochronny znak, zostają pocięte na małe fragmenty, a jeden z tych fragmentów (5’tiRNAGly-GCC) unieszkodliwia białko, które hamuje PD-L1. W rezultacie powstaje bardziej agresywny, odporny na leki i uchylający się przed układem odpornościowym nowotwór. Zamiast próbować bezpośrednio zwiększać DNMT2 — co mogłoby być ryzykowne w innych tkankach — autorzy sugerują celowanie w szkodliwy fragment RNA. Eksperymenty mysie z inhibitorem 5’tiRNAGly-GCC, szczególnie w połączeniu z doksorubicyną, dostarczają wstępnego dowodu, że przerwanie tej mikroskopijnej sieci RNA może pomóc okiełznać jedną z najbardziej śmiertelnych postaci raka tarczycy.
Cytowanie: Zhou, R., Li, B., Cao, M. et al. DNMT2 inhibits anaplastic thyroid cancer progression by downregulating 5’tiRNAGly-GCC production. Cell Death Dis 17, 240 (2026). https://doi.org/10.1038/s41419-026-08488-5
Słowa kluczowe: anaplastyczny rak tarczycy, DNMT2, fragmenty tRNA, oporność na chemioterapię, PD-L1