Clear Sky Science · pl
Ujawnienie ZNF124 jako nowego czynnika w neurodegeneracji: orkiestracja homeostazy fotoreceptorów poprzez transkrypcyjną regulację MSX2
Dlaczego to odkrycie ma znaczenie dla wzroku
Retinitis pigmentosa jest jedną z głównych przyczyn dziedzicznej ślepoty, a mimo to u niemal 40 procent pacjentów lekarze wciąż nie potrafią wskazać wadliwego genu. W badaniu tym odkryto nowego genetycznego gracza, nazwanego ZNF124, który pomaga utrzymać przy życiu komórki światłoczułe oka. Pokazując, jak mutacja w tym genie zaburza łańcuch molekularnych „przełączników” w siatkówce, badacze otwierają nowe drogi do diagnozy, a potencjalnie również do ukierunkowanych terapii dla osób tracących wzrok.
Ukryta przyczyna dziedzicznej utraty wzroku
Badacze przeanalizowali dużą rodzinę, w której u kilkorga dzieci pojawiły się klasyczne objawy retinitis pigmentosa: ślepota zmierzchowa we wczesnym wieku, kurczenie pola bocznego widzenia oraz stopniowa utrata wzroku centralnego. Szczegółowe badania okulistyczne ujawniły przerzedzenie siatkówki i osłabione elektryczne odpowiedzi na światło, oba typowe dla uszkodzenia pręcików i czopków. Żaden z ponad 80 znanych genów związanych z retinitis pigmentosa nie wykazywał oczywistych defektów u tych pacjentów, co sugerowało, że za chorobą może stać nieodkryty dotąd gen.
Wykrycie wadliwego genetycznego przełącznika
Wykorzystując sekwencjonowanie eksomu, które odczytuje białkodajne części DNA, zespół zidentyfikował rzadką, wcześniej nieopisanej mutację w genie ZNF124. Mutacja ta zmienia sposób składania RNA genu, usuwając kilka zasad w krytycznym złączu. W rezultacie białko ZNF124 zostaje skrócone i traci region palca cynkowego — strukturę zwykle służącą do rozpoznawania i wiązania konkretnych sekwencji DNA. Ponieważ białka zawierające palce cynkowe często działają jako główne przełączniki włączające lub wyłączające wiele innych genów, uszkodzony ZNF124 może wywołać dalekosiężne efekty w komórkach siatkówki.
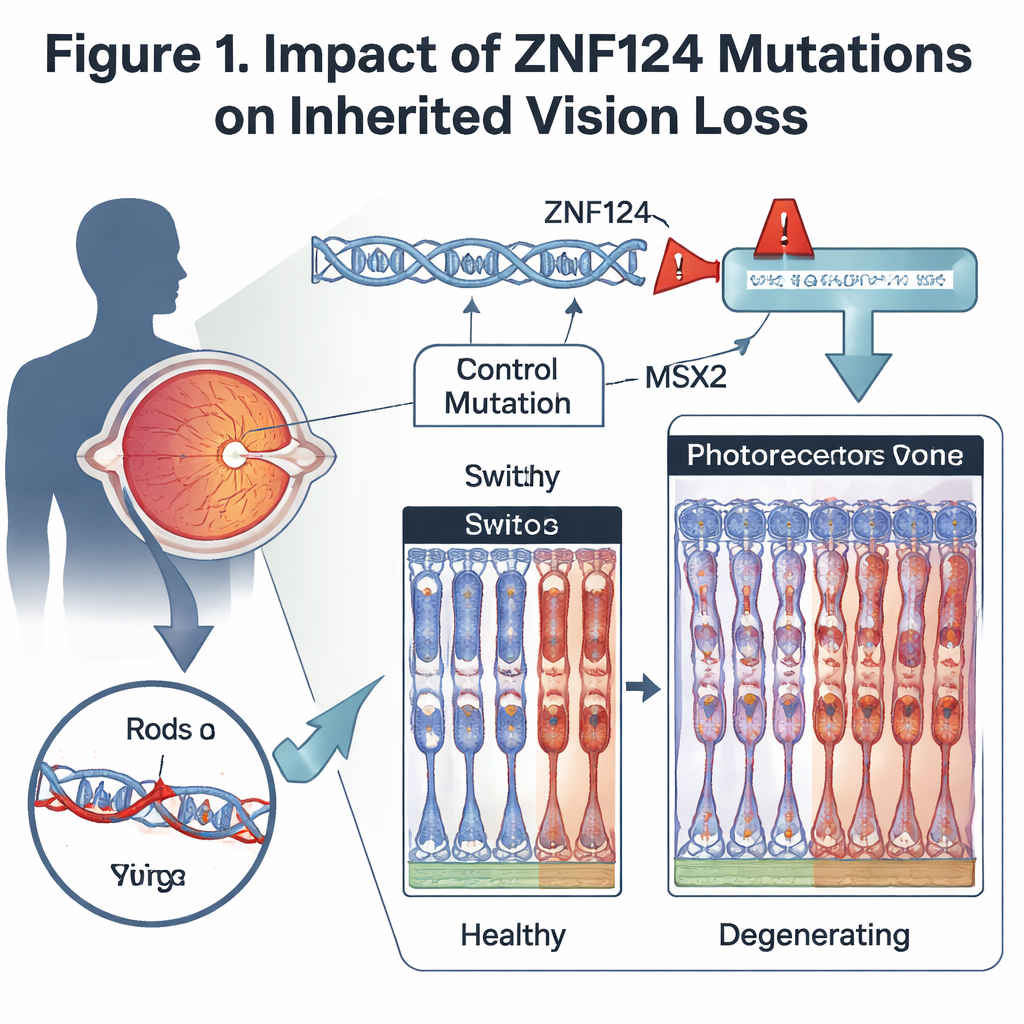
Testowanie genu w modelach zwierzęcych
Aby sprawdzić, jak utrata tego przełącznika wpływa na oko, naukowcy stworzyli myszy pozbawione Gm20541, najbliższego odpowiednika ZNF124 u myszy, specyficznie w siatkówce. Zwierzęta te rozwijały postępujące z wiekiem problemy z widzeniem: ich elektryczne odpowiedzi na słabe i silne światło osłabły, a mikroskopowe badania wykazały postępujące przerzedzenie warstwy siatkówki zawierającej fotoreceptory. Zarówno pręciki, które odpowiadają za widzenie nocne, jak i czopki, odpowiedzialne za widzenie barwne i dzienne, miały skrócone segmenty zewnętrzne i utratę kluczowych białek wzrokowych. Inne komórki siatkówki, takie jak niektóre komórki dwubiegunowe, również uległy redukcji, a komórki podporowe zostały aktywowane — co jest częstą reakcją na przewlekłe uszkodzenie siatkówki.
Odkrycie szlaku kontrolnego ZNF124–MSX2
Następnym pytaniem było, które geny ZNF124 normalnie kontroluje. Stosując metody biochemiczne mapujące miejsca wiązania białek na DNA, w połączeniu z globalnymi pomiarami RNA z siatkówek myszy, zespół wykazał, że ZNF124 wiąże się z i aktywuje inny gen zwany MSX2. W zdrowych komórkach ZNF124 przyłącza się do specyficznej krótkiej sekwencji w regionie „włącznika” MSX2 i zwiększa jego aktywność. U myszy pozbawionych Gm20541 poziomy MSX2 spadły o ponad połowę. Gdy badacze usunęli MSX2 specyficznie w komórkach pręcikowych, u tych zwierząt również wystąpiło przerzedzenie warstwy fotoreceptorów i skrócenie segmentów zewnętrznych, odzwierciedlając defekty zaobserwowane u myszy z wyłączeniem ZNF124-podobnego genu. To umieściło MSX2 bezpośrednio poniżej ZNF124 w szlaku niezbędnym do przetrwania fotoreceptorów.
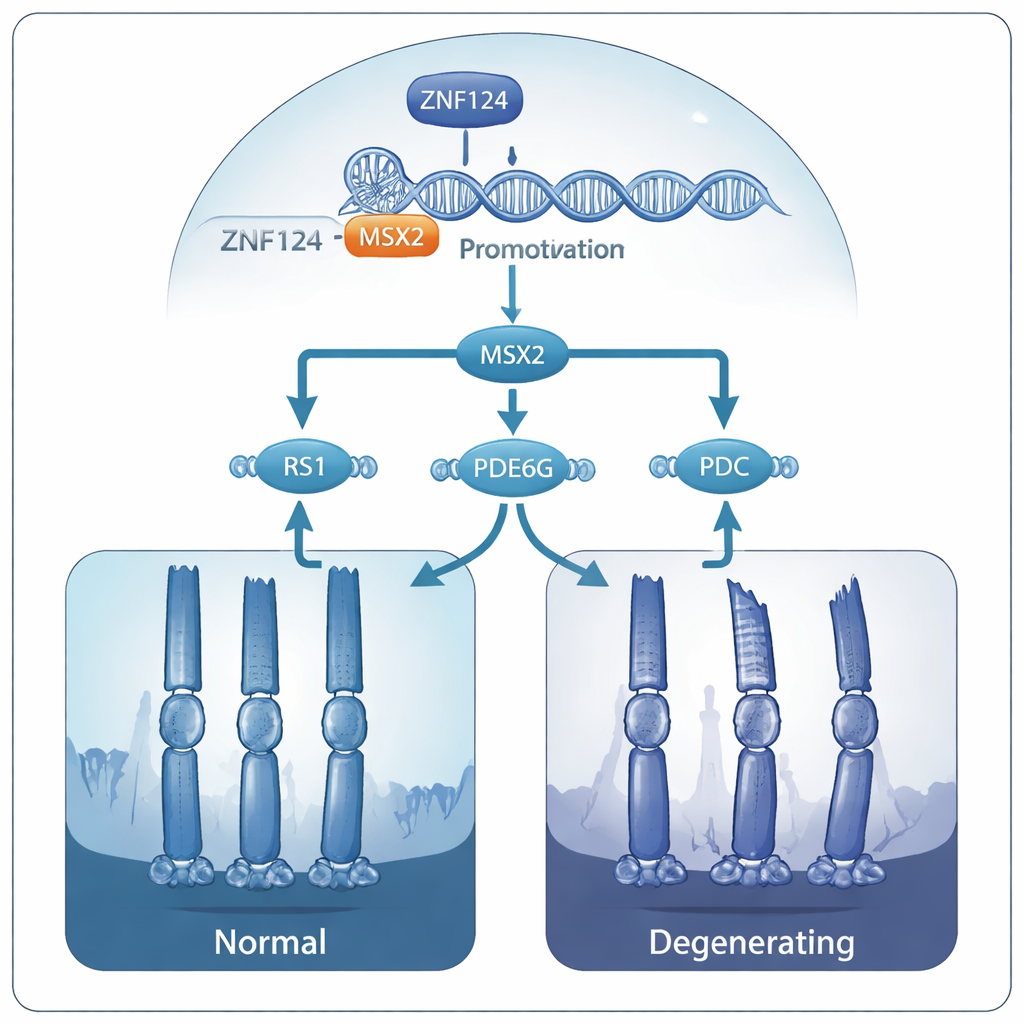
Od genetycznych przełączników do wrażliwych fotoreceptorów
Dalsze analizy wykazały, że MSX2 z kolei pomaga utrzymać aktywność kilku innych genów już powiązanych z dziedzicznymi chorobami siatkówki: RS1, PDE6G i PDC. Geny te wspierają strukturę siatkówki oraz chemię sygnalizacji wzrokowej. Gdy poziom MSX2 spadł, wszystkie trzy geny stały się mniej aktywne, a ich produkty białkowe zmniejszyły się. Autorzy proponują, że u osób z uszkadzającymi mutacjami ZNF124 cały ten kaskadowy mechanizm ulega osłabieniu: ZNF124 nie jest w stanie w pełni aktywować MSX2, MSX2 nie utrzymuje RS1, PDE6G i PDC, a z czasem fotoreceptory tracą integralność strukturalną i obumierają, prowadząc do postępującej utraty wzroku.
Co to oznacza dla pacjentów i terapii
Dla osoby nietechnicznej zasadniczym przesłaniem jest to, że siatkówka zależy od precyzyjnie wyregulowanej hierarchii genetycznych przełączników. Praca ta identyfikuje ZNF124 jako nowy przełącznik najwyższego poziomu, którego uszkodzenie może powodować dziedziczną ślepotę przez konkretny partnera położonego dalej w szlaku — MSX2 — oraz jego geny docelowe. Klinicznie ZNF124 można teraz dodać do paneli testów genetycznych, co pomoże większej liczbie rodzin uzyskać precyzyjne diagnozy. W dłuższej perspektywie terapie przywracające aktywność ZNF124, MSX2 lub dotkniętych genów docelowych mogą pomóc ustabilizować lub uratować komórki światłoczułe, dając nadzieję osobom z dotąd niewyjaśnionymi postaciami retinitis pigmentosa.
Cytowanie: Yang, Y., Jiang, X., Li, S. et al. Unveiling ZNF124 as a novel determinant in neurodegeneration: orchestration of photoreceptor homeostasis through MSX2 transcriptional regulation. Cell Death Dis 17, 234 (2026). https://doi.org/10.1038/s41419-026-08487-6
Słowa kluczowe: retinitis pigmentosa, fotoreceptory, ZNF124, MSX2, dziedziczna choroba siatkówki