Clear Sky Science · pl
HIF2α-indukowana oksydaza lizylowa chroni przebieg ciąży przez przebudowę kolagenów na granicy płodowo-matczynej
Dlaczego macica musi się przygotować na nowego lokatora
Zanim ciąża może się utrwalić, wczesny zarodek musi dokonać czegoś niezwykłego: wniknąć w ścianę macicy i zbudować system podtrzymujący życie — łożysko. Artykuł bada, jak tkanka matczyna subtelnie przebudowuje się, by przyjąć zarodek, ze szczególnym uwzględnieniem roli niskiego poziomu tlenu i mało znanego enzymu w przygotowaniu wyściółki macicy. Zrozumienie tego precyzyjnego tańca może wyjaśnić, dlaczego niektóre ciąże kończą się niepowodzeniem bardzo wcześnie, i zasugerować nowe sposoby zapobiegania niepłodności i powikłaniom ciąży.
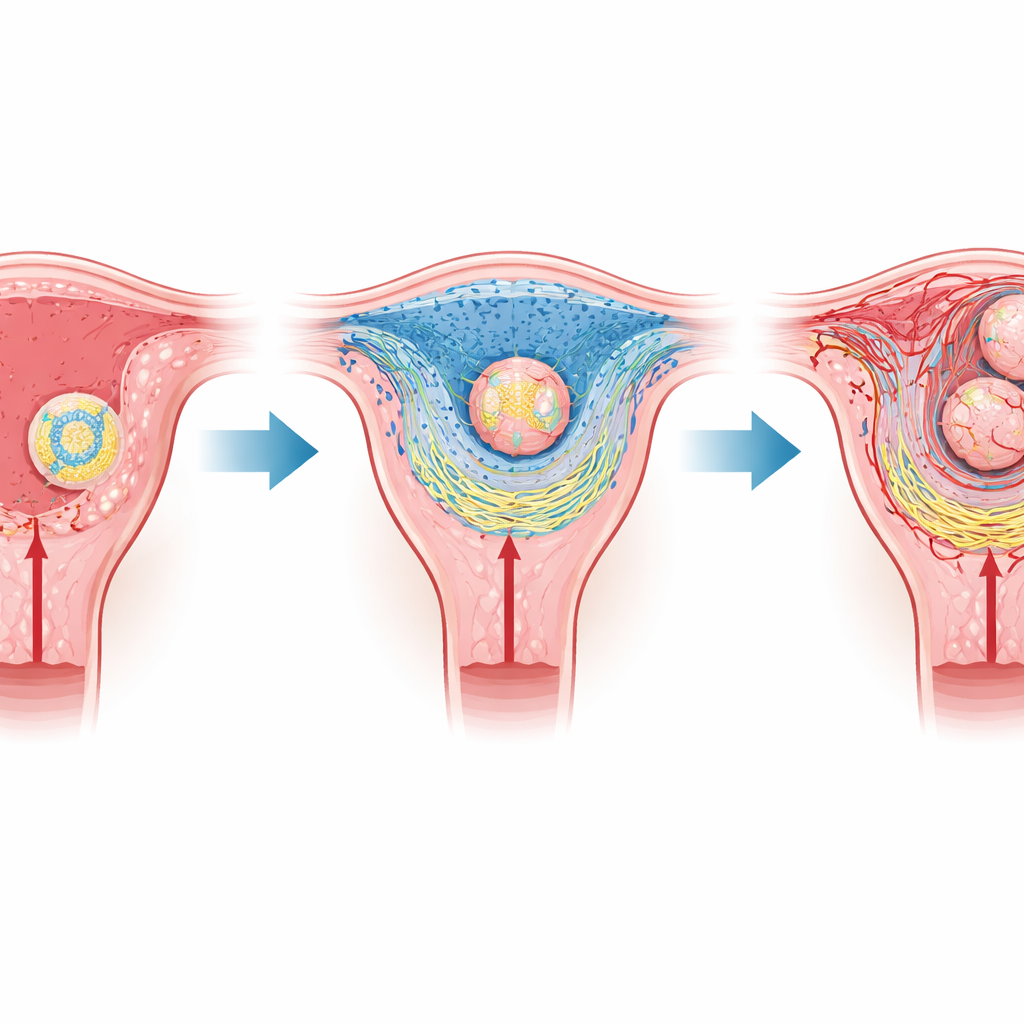
Delikatne spotkanie matki i zarodka
U ssaków, takich jak myszy i ludzie, najwcześniejszy etap ciąży zależy od implantacji, gdy zarodek przyczepia się do wyściółki macicy, a następnie w nią wnika. Zarodek otoczony jest warstwą wyspecjalizowanych komórek, które później utworzą łożysko, podczas gdy tkanka matczyna przekształca się w poduszkowatą warstwę zwaną dociduum. Najbliżej zarodka leży cienki obszar zwany pierwotną strefą docidialną, który nie zawiera naczyń krwionośnych i dlatego ma niski poziom tlenu. Wcześniejsze badania wykazały, że ta naturalnie słabo utlenowana przestrzeń pomaga uruchomić implantację, ale w jaki sposób tak prosta fizyczna właściwość może zorganizować całe tkanki, nie było dobrze poznane.
Niski tlen jako ukryty przełącznik
Autorzy użyli potężnej techniki zwanej transkryptomiką przestrzenną, która mapuje aktywność genów bezpośrednio na plasterkach tkanki, aby badać macice myszy w dniach, gdy zarodki przyczepiają się i wnikają. Skoncentrowali się na białku zwanym HIF2α, które aktywuje się w warunkach niskiego tlenu i działa jak przełącznik genetyczny. U normalnych myszy komórki w pierwotnej strefie docidialnej wykazywały silną aktywność genów związanych z hipoksją i z budową otaczającej rusztowania tkanki, w tym kolagenów tworzących macierz zewnątrzkomórkową. Gdy HIF2α został usunięty tylko z macicy, ogólny układ typów komórek wyglądał zaskakująco normalnie. Jednak w wysokiej rozdzielczości sieć kolagenowa była zdezorganizowana, powierzchnia nabłonkowa nie otwierała się prawidłowo, a komórki zarodkowe miały trudności z przenikaniem przez tkankę matczyną.
Enzym, który sieciuje rusztowanie
Pogłębiając badania, zespół zidentyfikował kluczowego gracza działającego poniżej HIF2α: oksydazę lizylową, czyli Lox, enzym chemicznie sieciujący włókna kolagenowe, który pomaga usztywnić i ustabilizować tkankę. W normalnych ciążach poziom Lox gwałtownie wzrastał wokół zarodków dokładnie w momencie, gdy zaczynały one wnikać. W macicach pozbawionych HIF2α ekspresja Lox spadła, a włókna kolagenowe wyglądały na pofragmentowane zamiast tworzyć gęstą sieć. Aby bezpośrednio przetestować znaczenie Lox, badacze stworzyli myszy, w których Lox został usunięty tylko w macicy. Samice te zaszły w ciążę rzadziej, nosiły mniej zarodków i często wykazywały objawy utraty zarodków oraz krwawienia w późniejszym okresie ciąży, mimo że najwcześniejsze etapy przyczepiania i pogrubienia tkanki początkowo wyglądały normalnie.
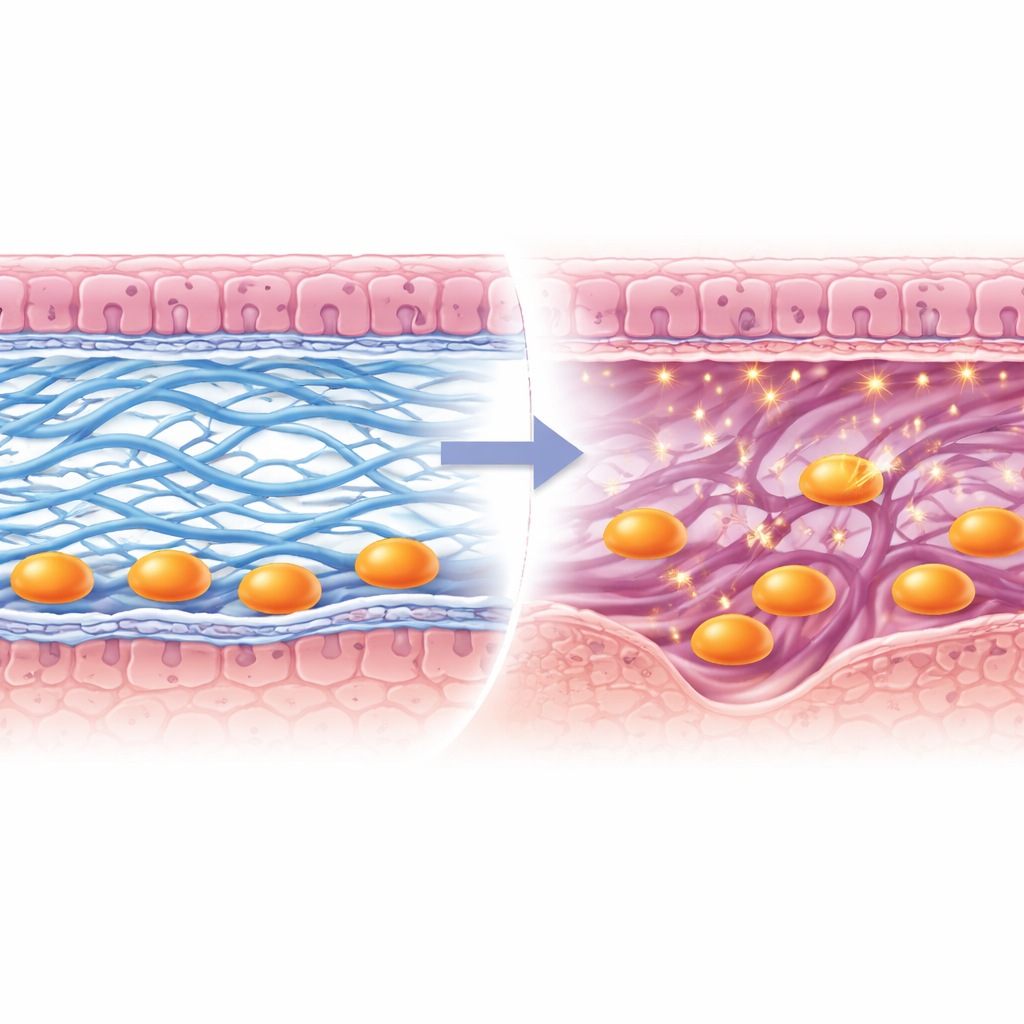
Otwarcie drogi dla łożyska
Dokładne obrazowanie ujawniło, co poszło nie tak przy braku Lox. Cienka, bogata w białka warstwa zwana błoną podstawną, która normalnie ulega rozkładowi, aby umożliwić przejście komórek zarodkowych, pozostała w dużej mierze nienaruszona. Włókna kolagenu typu I w podłożu zrębu nie utworzyły mocnych, ciągłych pęczków, podczas gdy kolagen typu IV w błonie podstawnej nie został właściwie usunięty w pobliżu komórek inwazyjnych. W efekcie komórki trofoblastu — pochodzące z zarodka pionierskie komórki budujące łożysko — utknęły na powierzchni zamiast tunelować w warstwę matczyną. Zespół stwierdził również, że enzym tnący kolagen, Mmp9, nie został uruchomiony w tych trofoblastach, co dodatkowo utrudniało ich postęp. Z upływem czasu struktury łożyska rozwijały się wadliwie, zarodki rosły nieprawidłowo, a powodzenie ciąży malało.
Co to oznacza dla zdrowia ciąży
Łącząc wyniki, ustalono łańcuch zdarzeń, w którym niski poziom tlenu w wczesnej strefie implantacyjnej aktywuje HIF2α, co z kolei zwiększa poziom Lox. Lox następnie przebudowuje i sieciuje włókna kolagenowe oraz pomaga w rozkładzie błony podstawnej, a także umożliwia aktywację enzymów takich jak Mmp9, które oczyszczają drogę. Ta przebudowa zapewnia zarówno strukturalne rusztowanie, jak i otwarte przejście dla komórek trofoblastu, aby mogły wnikać i budować łożysko. Dla czytelnika niebędącego specjalistą przekaz jest taki, że powodzenie ciąży zależy nie tylko od zdrowych zarodków i hormonów, lecz także od cichej reorganizacji architektury tkanki matczynej. Zakłócenia w tej ścieżce hipoksja–HIF2α–Lox mogą leżeć u podstaw niektórych przypadków niewyjaśnionej niepłodności, poronień i zaburzeń związanych ze słabą inwazją łożyska, co sugeruje nowe markery diagnostyczne i cele terapeutyczne wspierające wczesną ciążę.
Cytowanie: Aikawa, S., Shimizu-Hirota, R., Sakashita, A. et al. HIF2α-induced lysyl oxidase safeguards successful pregnancy by remodelling collagens at the feto-maternal interface. Cell Death Dis 17, 250 (2026). https://doi.org/10.1038/s41419-026-08485-8
Słowa kluczowe: implantacja zarodka, maciczne zewnątrzkomórkowe matrix, oksydaza lizylowa, inwazja trofoblastu, rozwój łożyska