Clear Sky Science · pl
Ubikwitynacja mH2A1 zależna od UBE3A aktywuje transkrypcję TERT, promując oporność na senescencję w raku trzustki
Dlaczego te badania mają znaczenie dla pacjentów
Rak trzustki należy do najgroźniejszych nowotworów, częściowo dlatego, że komórki nowotworowe są wyjątkowo skuteczne w omijaniu wbudowanych hamulców starzenia organizmu. W tym badaniu odkryto ukryty molekularny „obwód sabotażowy”, który pomaga komórkom raka trzustki pozostawać młodymi, nadal się dzielić i opierać terapiom. Zrozumienie tego obwodu wskazuje nowe podejście: wymusić starzenie tych komórek, a następnie selektywnie je usunąć, co otwiera drogę do inteligentniejszych terapii łączonych.
Starzenie jako naturalny hamulec nowotworowy organizmu
Wszystkie komórki mają wewnętrzny zegar, który ostatecznie sprawia, że przestają się dzielić — proces znany jako senescencja. W wczesnych zmianach przednowotworowych ten zegar może spowolnić rozwój guza, kierując komórki przedrakowe na stałą „emeryturę”. Wiele terapii przeciwnowotworowych działa częściowo przez wymuszanie takiego stanu. Jednak jeśli senescentne komórki nie zostaną usunięte, mogą napędzać stan zapalny i sprzyjać nawrotowi choroby. To doprowadziło do nowej strategii terapeutycznej: najpierw wymusić senescencję w komórkach nowotworowych, a następnie wyeliminować te zestarzałe komórki lekami senolitycznymi, które są w nich szczególnie toksyczne.
Enzym sprzyjający rakowi w świetle reflektorów
Aby znaleźć geny, które pomagają komórkom raka trzustki przeciwstawiać się senescencji, zespół przeanalizował obszerne bazy danych pacjentów, a następnie potwierdził odkrycia w próbkach guzów i liniach komórkowych. Skoncentrowali się na białku UBE3A, enzymie znakującym inne białka do degradacji. Poziomy UBE3A były znacznie wyższe w guzach trzustki niż w pobliskiej tkance normalnej, a pacjenci z większą ekspresją UBE3A mieli tendencję do większych, bardziej zaawansowanych nowotworów i gorszego przeżycia. W hodowlach komórkowych zwiększenie UBE3A przyspieszało wzrost, zmniejszało klasyczne markery starzenia komórkowego i redukowało zapalne wydzieliny charakterystyczne dla komórek senescentnych. Wyciszenie UBE3A dawało efekt odwrotny, a w modelach mysich ostro zmniejszało wzrost guza i przerzuty do wątroby. 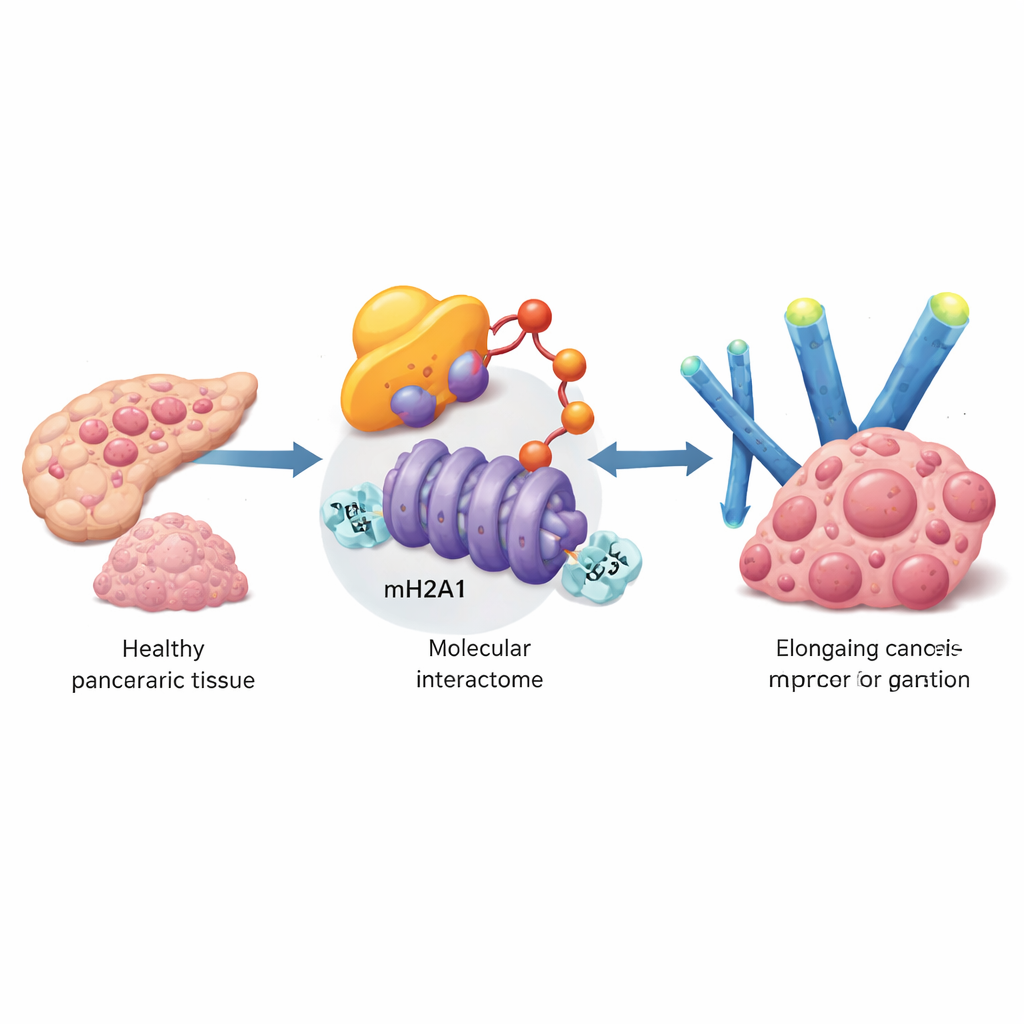
Jak komórki nowotworowe usuwają chromatinowy hamulec
Zagłębiając się dalej, badacze sprawdzili, na jakie molekuły działa UBE3A. Przy użyciu zaawansowanych przesiewów w spektrometrii mas odkryli, że UBE3A wiąże się z wariantem histonu zwanym macroH2A1 (mH2A1) i chemicznie go znakują, a ten wariant pomaga upakować DNA i zwykle działa jako hamulec aktywności genów. UBE3A przyłącza łańcuch „znaków do zniszczenia” do mH2A1 w określonym miejscu, powodując jego rozkład przez komórkowe mechanizmy degradowania białek. W guzach trzustki poziomy mH2A1 były niższe tam, gdzie UBE3A było wysokie, a przywrócenie mH2A1 przeciwdziałało zdolności UBE3A do blokowania senescencji i napędzania wzrostu guza. To ujawnia kluczowy krok: komórki raka trzustki usuwają ochronny znak chromatynowy, wykorzystując UBE3A do eliminacji mH2A1.
Odblokowanie telomerazy, by utrzymać młodość komórek
Następne pytanie brzmiało, które geny zostają uwolnione po usunięciu mH2A1. Łącząc sekwencjonowanie RNA i mapy wiązania DNA, zespół zidentyfikował gen telomerazy TERT jako centralny cel. Telomeraza utrzymuje ochronne czapeczki na końcach chromosomów, pozwalając komórkom na dalsze dzielenie się zamiast wejścia w senescencję. Badanie pokazuje, że mH2A1 zwykle znajduje się w regionie wzmacniającym (enhancer) w obrębie genu TERT, gdzie rekrutuje inny enzym, EZH2, do nałożenia represyjnego markera na pobliskie histony. Ta kombinacja tłumi TERT i pozwala telomerom się skracać. Gdy UBE3A niszczy mH2A1, kompleks represyjny się rozpada, enhancer staje się aktywny, TERT zostaje włączony, telomery są utrzymane, a komórki raka trzustki zyskują odporność na starzenie. Mutanty UBE3A pozbawione zdolności znakowania białek albo mutantne mH2A1, których nie da się znakować, przerywają ten obwód i przywracają hamulec senescencji.
Łączenie indukcji senescencji z senolitycznym sprzątaniem
Na koniec badacze sprawdzili, czy tę ścieżkę da się wykorzystać terapeutycznie. Wyłączenie UBE3A skierowało komórki raka trzustki w stronę senescencji i zwiększyło ich zależność od białek antyapoptotycznych rodziny BCL‑2 — znanej wrażliwości komórek senescentnych. Zespół połączył następnie hamowanie UBE3A z ABT‑263, lekiem senolitycznym celującym w te białka przetrwania. W hodowlach komórkowych kombinacja wywołała znacznie więcej zaprogramowanej śmierci komórek nowotworowych niż każde z leczeń osobno. W modelach mysich guzy z obniżonym UBE3A kurczyły się jeszcze bardziej po podaniu ABT‑263, a markery proliferacji w obrębie guzów spadły gwałtownie. 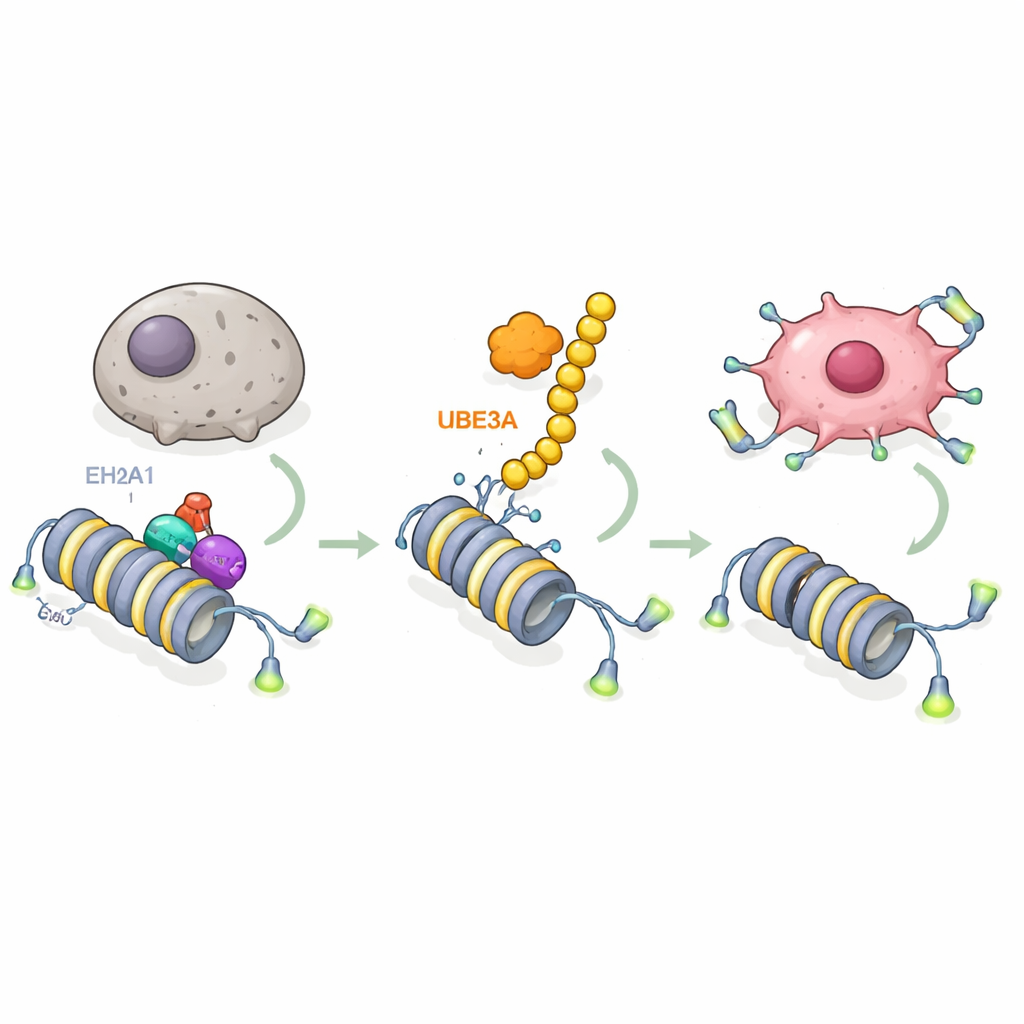
Co to oznacza dla przyszłego leczenia
Praca ta ujawnia szczegółowy łańcuch zdarzeń, dzięki któremu komórki raka trzustki unikają starzenia: UBE3A niszczy chromatynowy hamulec mH2A1, co z kolei znosi represję genu telomerazy TERT i pomaga utrzymać telomery, pozwalając komórkom na dalsze dzielenie się. Celując w UBE3A, lekarze mogą ponownie uruchomić naturalny program starzenia komórkowego, a następnie zastosować leki senolityczne, takie jak ABT‑263, by selektywnie usunąć te podatne, zestarzałe komórki nowotworowe. Chociaż potrzebne są dalsze badania, aby przekształcić ten mechanizm w terapie dla pacjentów, oś UBE3A–mH2A1–TERT oferuje obiecujący nowy punkt zaczepienia w jednym z najbardziej opornych na leczenie nowotworów.
Cytowanie: Ren, L., Lu, R., Fei, X. et al. UBE3A-mediated mH2A1 Ubiquitination activates TERT transcription to promote senescence resistance in pancreatic cancer. Cell Death Dis 17, 274 (2026). https://doi.org/10.1038/s41419-026-08480-z
Słowa kluczowe: rak trzustki, senescencja komórkowa, telomeraza, ligaza ubikwityny, terapia senolityczna