Clear Sky Science · pl
Mała cząsteczka hamująca białko ARF GTPazy 1 ogranicza wzrost i przerzuty komórek raka wątroby i jelita grubego
Dlaczego to badanie ma znaczenie
Raki wątroby i jelita grubego należą do najgroźniejszych nowotworów, a obecne terapie często zmniejszają guzy kosztem silnych działań niepożądanych. W tym badaniu analizowano nowy rodzaj leku, który nie polega na zatruwaniu szybko dzielących się komórek, lecz wnika do komórek nowotworowych i rozbija białkowe „centrum sterujące”, od którego zależą ich wzrost i rozprzestrzenianie się. Celując w to centrum, eksperymentalny związek ma na celu spowolnienie wzrostu guza przy jednoczesnym oszczędzaniu zdrowych tkanek.
Wrażliwe centrum sterujące wewnątrz komórek nowotworowych
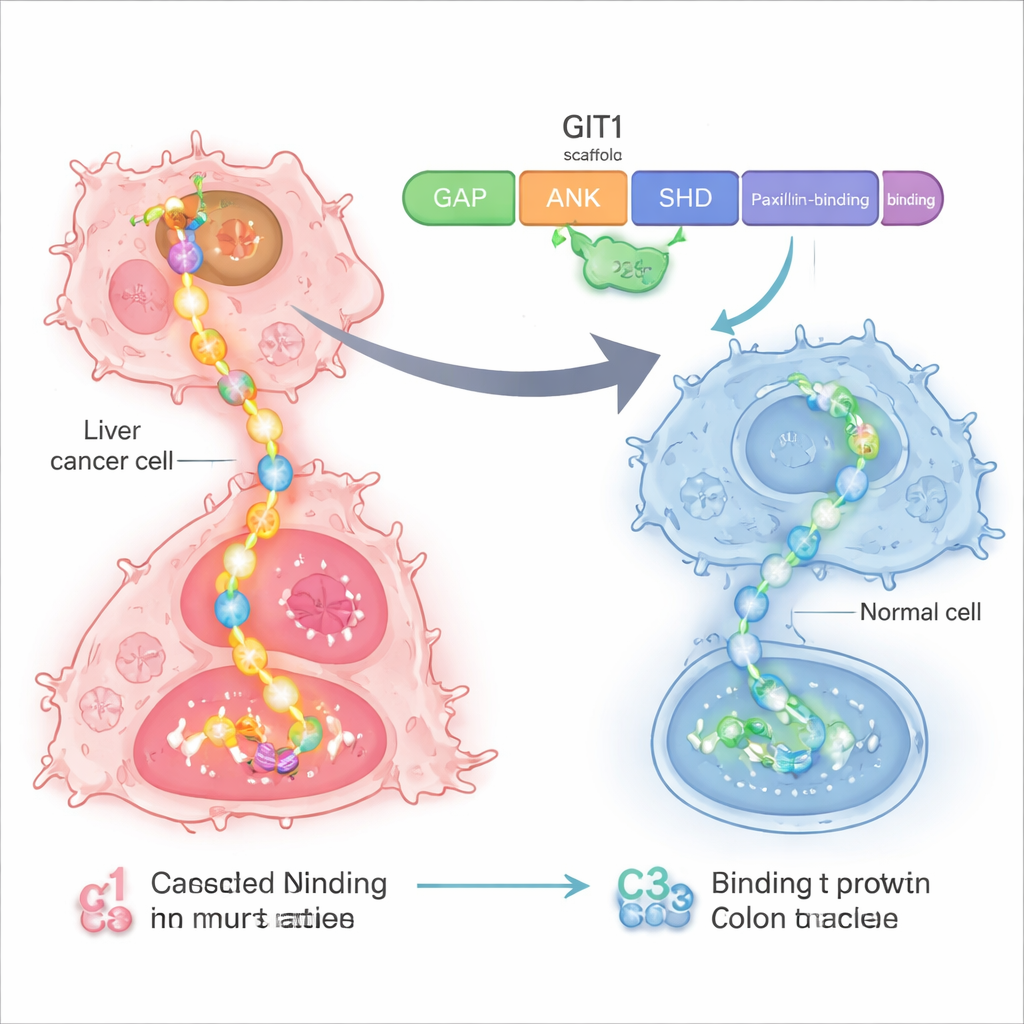
Naukowcy skupili się na białku o nazwie GIT1, które działa jak rusztowanie lub listwa zasilająca wewnątrz komórek. W raku wątroby i jelita grubego GIT1 oraz jego partner MAT2B są nadmiernie produkowane. Wspólnie gromadzą elementy kluczowej ścieżki wzrostu znanej jako RAS–RAF–MEK–ERK — łańcucha sygnałów nakazujących komórkom dzielenie i migrację. Wcześniejsze prace wykazały, że gdy GIT1 i MAT2B występują w nadmiarze, guzy wątroby i jelita grubego rosną szybciej i łatwiej się rozsiewają, a ich zmniejszenie spowalnia rozwój nowotworu. To sprawiło, że rusztowanie GIT1–MAT2B stało się atrakcyjnym celem dla bardziej precyzyjnej terapii.
Projektowanie małej cząsteczki bez mapy strukturalnej
Kluczowym wyzwaniem było to, że trójwymiarowa struktura krystaliczna GIT1 nie jest znana, więc zespół nie mógł po prostu „spojrzeć” na kształt białka. Zamiast tego użyto modeli komputerowych do przewidzenia struktury jednego regionu GIT1 złożonego z powtórzeń ankrynowych, położonego w pobliżu miejsc, gdzie przyłączają się MAT2B i inne białka sygnałowe. Następnie w sposób wirtualny przeskanowano dużą bibliotekę małych cząsteczek wobec tego modelu, aby sprawdzić, które mogą wiązać się z tym obszarem. Spośród dziewięciu kandydatów testowanych w komórkach wyróżniła się jedna cząsteczka — nazwana związek 3 (C3). C3 wiązała się specyficznie z GIT1, ale nie z jego bliskim krewnym GIT2, i obniżała aktywność sygnału wzrostu ERK w wielu liniach komórkowych nowotworów.
Powstrzymywanie komórek nowotworowych przed dzieleniem i rozprzestrzenianiem
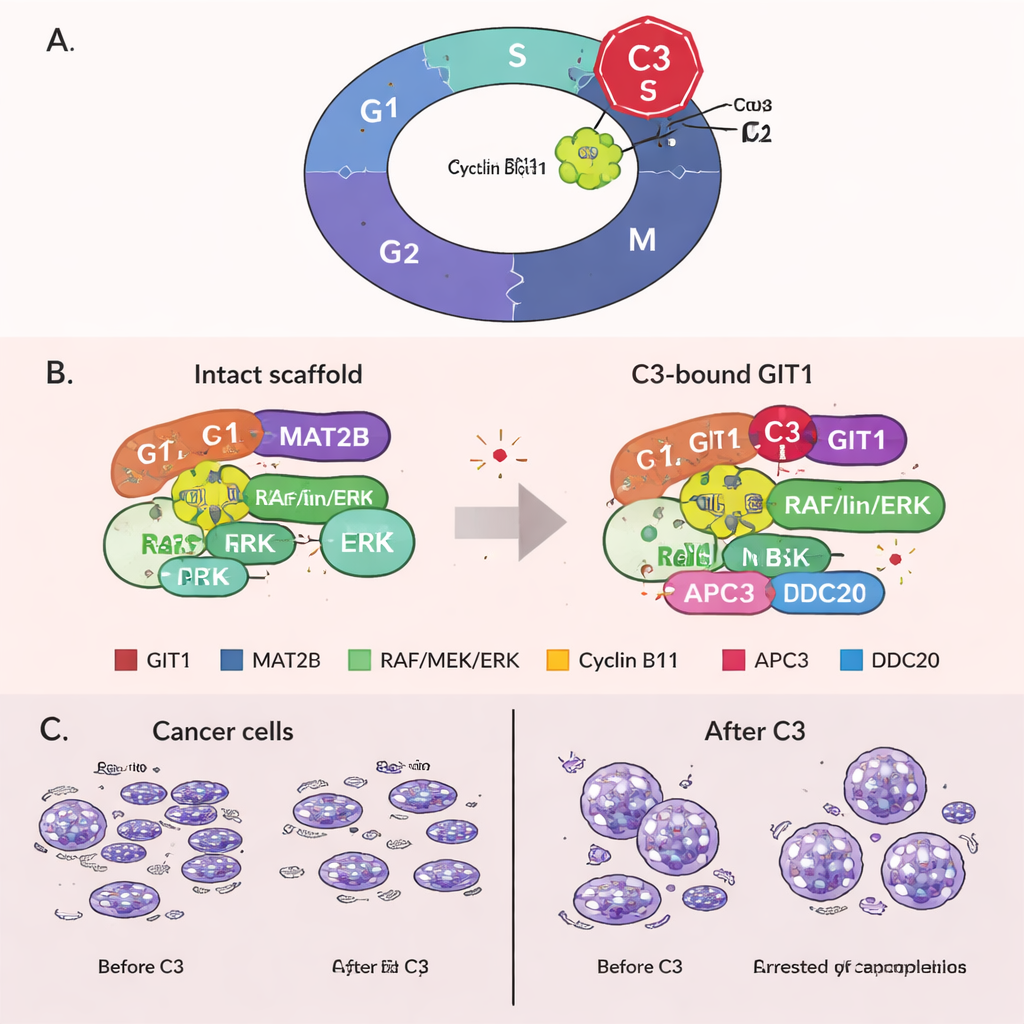
Po leczeniu komórek raka wątroby i jelita grubego C3 ich wzrost spowolnił, a przy wyższych dawkach wiele komórek obumierało, podczas gdy niezmienione komórki wątrobowe i nerkowe pozostawały w dużej mierze nienaruszone. C3 powodował zatrzymanie komórek na granicy faz G2 i M cyklu komórkowego — punkcie kontrolnym tuż przed i podczas mitozy, gdy komórka dzieli się na dwie. Związek znacząco zmniejszył też zdolność komórek nowotworowych do tworzenia kolonii i przemieszczania się po płytce — dwa laboratoryjne wskaźniki związane z nawrotem guza i przerzutami. Na poziomie molekularnym C3 osłabił interakcje między GIT1, MAT2B a białkami sygnalizacji RAF–MEK–ERK, prowadząc do niższej aktywności MEK i ERK oraz mniejszej ilości cykliny D1, która napędza cykl komórkowy.
Zatrzymywanie komórek w mitozie dzięki nowo odkrytej roli GIT1
Niespodziewanie zespół odkrył nową funkcję GIT1 w końcowych etapach podziału komórki. Stwierdzili, że GIT1 wiąże się z cykliną B1, białkiem pomagającym w wejściu w mitozę, oraz z częściami kompleksu promującego anafazę (APC/C), który normalnie znakuję cyklinę B1 do zniszczenia, żeby komórki mogły wyjść z mitozy. Leczenie C3 wzmocniło powiązanie między GIT1 a cykliną B1, ale osłabiło połączenia między GIT1, cykliną B1 i składnikami APC/C. W rezultacie cyklina B1 nie była skutecznie rozkładana, jej poziom pozostał wysoki, a komórki utknęły w mitozie. To przedłużone zatrzymanie jest znane z wywoływania śmierci komórki, co daje drugą drogę, którą C3 może zabijać komórki nowotworowe. Co ważne, gdy GIT1 zostało eksperymentalnie zmniejszone, C3 straciło dużą część swojej zdolności do podnoszenia poziomu cykliny B1, blokowania cyklu komórkowego i tłumienia wzrostu, pokazując, że jego efekty są rzeczywiście zależne od GIT1.
Zachęcające wyniki w modelach zwierzęcych
Następnie badacze przeszli do modeli mysich, aby sprawdzić, czy C3 zadziała w organizmach żywych. U myszy z prawidłowym układem odpornościowym z wszczepionymi guzami jelita grubego, wstrzyknięcia C3 bezpośrednio do guzów wyraźnie spowolniły ich wzrost bez oczywistej toksyczności dla głównych narządów. W dwóch dodatkowych modelach — ludzkie komórki raka jelita grubego rosnące w wątrbach myszy bez układu odporności oraz mysi komórki raka jelita grubego, które rozsiały się do wątroby u myszy z funkcjonującym układem odporności — podawanie C3 dootrzewnowo zmniejszyło obciążenie guzem i objawy rozsiewu. Badania krwi i analizy tkanek sugerowały, że leczenia były dobrze tolerowane, a badania farmakokinetyczne wykazały, że stężenia leku we krwi utrzymywały się wystarczająco wysoko przez kilka godzin po dawce.
Co to może znaczyć dla przyszłych terapii nowotworowych
Dla czytelnika niezwiązanego ze specjalnością kluczowy wniosek jest taki, że badacze znaleźli sposób ataku na raka nie przez celowanie w pojedynczą zmutowaną enzymę, lecz przez zakłócenie wielobiałkowego zespołu, od którego komórki nowotworowe zależą zarówno w kwestii sygnałów wzrostu, jak i poprawnego podziału komórek. Ich mała cząsteczka, C3, wiąże się specyficznie z GIT1, przebudowuje sieć jego partnerów, tłumi główną ścieżkę wzrostu i wprawia komórki nowotworowe w śmiertelny korek podczas mitozy. Chociaż C3 jest wciąż narzędziem eksperymentalnym, a nie lekiem dla pacjentów, praca ta pokazuje, że celowanie w białka-szablony takie jak GIT1 może otworzyć nową drogę leczenia raków wątroby i jelita grubego z większą precyzją i potencjalnie mniejszymi skutkami ubocznymi.
Cytowanie: Peng, H., Chhimwal, J., Fan, W. et al. A small molecule inhibitor of ARF GTPase protein 1 limits liver and colon cancer cell growth and metastasis. Cell Death Dis 17, 238 (2026). https://doi.org/10.1038/s41419-026-08477-8
Słowa kluczowe: rak wątroby, rak jelita grubego, terapia celowana, zatrzymanie cyklu komórkowego, białko-szablon