Clear Sky Science · pl
Przeprogramowanie losu komórek czerniaka: modulatory TRPM8 wywołują apoptozę i wzmacniają cytotoksyczność komórek NK
Dlaczego wykorzystanie „czujnika zimna” przeciwko rakowi skóry ma znaczenie
Czerniak to groźna postać raka skóry, która często uczy się unikać zarówno leków, jak i odpowiedzi immunologicznej. W tym badaniu zidentyfikowano nieoczekiwaną słabość komórek czerniaka: białko TRPM8, najbardziej znane jako receptor umożliwiający neuronoms odczuwanie zimna lub mentolu. Naukowcy pokazują, że starannie zaprojektowane związki blokujące TRPM8 mogą zmusić komórki czerniaka do samobójczej śmierci, jednocześnie ułatwiając ich rozpoznanie i zniszczenie przez komórki natural killers (NK). Ten podwójny efekt sugeruje nową drogę terapii opornego, zaawansowanego czerniaka.
Ukryty przełącznik na komórkach czerniaka
Poprzez analizę dużych baz danych onkologicznych i badania komórek czerniaka pochodzących od pacjentów w warunkach laboratoryjnych zespół stwierdził, że TRPM8 występuje w znacznie większym nasileniu w czerniaku przerzutowym niż w normalnej skórze, w tym w zdrowych melanocytach i fibroblastach skóry. Za pomocą obrazowania wykazano, że TRPM8 lokalizuje się zarówno na powierzchni komórki, jak i na błonach wewnętrznych, co umieszcza go w strategicznych miejscach wpływających na zachowanie komórki. Po zastosowaniu panelu nowych związków ukierunkowanych na TRPM8 dwie pochodne (oznaczone jako 4 i 9) konsekwentnie się wyróżniały: znacząco obniżały przeżywalność komórek czerniaka w czasie, pozostawiając przy tym komórki zdrowej skóry w dużej mierze nietknięte. Testy genetyczne potwierdziły, że po usunięciu TRPM8 działanie tych leków traciło moc zabijającą, a przy zwiększeniu ekspresji TRPM8 komórki czerniaka stawały się jeszcze bardziej wrażliwe, co dowodzi, że efekt zależy od tego konkretnego kanału. 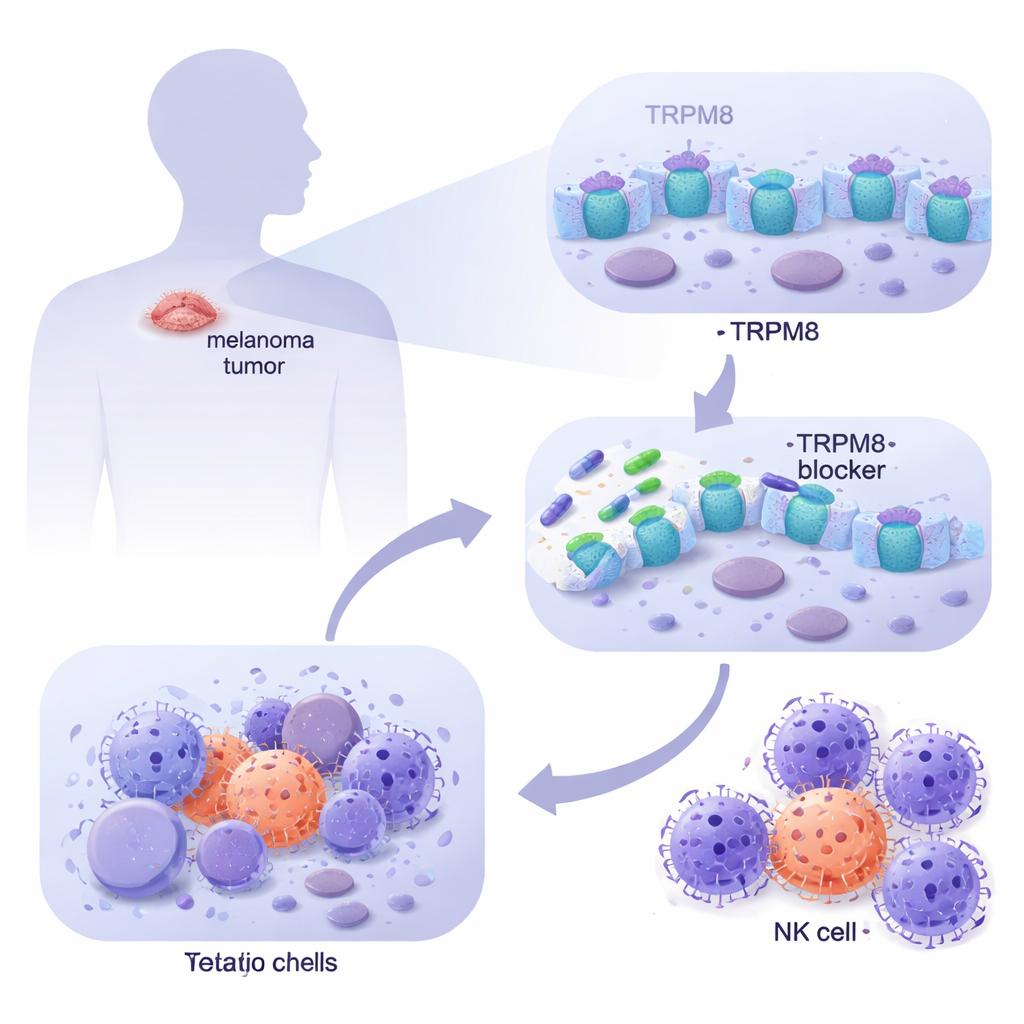
Wpychanie komórek nowotworowych w kryzys energetyczny
W odróżnieniu od klasycznych aktywatorów TRPM8, takich jak mentol, które wywołują napływ wapnia do komórek, nowe inhibitory nie powodowały zmian poziomu wapnia. Zamiast tego wywoływały falę stresu oksydacyjnego wewnątrz komórek czerniaka. Związki te szybko zwiększały liczbę reaktywnych form tlenu, szczególnie w mitochondriach — komórkowych fabrykach energii. Ten wybuch utleniania doprowadził do utraty potencjału elektrycznego mitochondriów, ich fragmentacji oraz uwolnienia cytochromu c, co stanowi kluczowy krok uruchamiający wewnętrzny program „samobójczy” komórki. Przeciwutleniacze neutralizujące te reaktywne cząsteczki w dużym stopniu ratowały komórki, pokazując, że zaburzenie równowagi redoks nie jest efektem ubocznym, lecz istotnym mechanizmem śmierci. W następstwie pojawiły się klasyczne markery śmierci, takie jak aktywacja kaspazy-3 i pęknięcie PARP, potwierdzające, że komórki przechodzą zaprogramowaną apoptozę, a nie przypadkowe uszkodzenie.
Unieszkodliwienie sygnałów przeżycia i pobudzenie strażnika
Uderzenie oksydacyjne wywołało szerszą odpowiedź stresową. Leki aktywowały ATM — sensor uszkodzeń DNA — i prowadziły do nagromadzenia oraz aktywacji p53, znanego białka supresorowego nowotworów, które decyduje, czy uszkodzona komórka ma się naprawić, czy zginąć. Równocześnie związki osłabiły jedną z głównych dróg przeżycia czerniaka: szlak PI3K–AKT. Normalnie TRPM8 wchodzi w fizyczne interakcje ze składnikami PI3K, co pomaga utrzymać AKT w aktywnej, promującej wzrost formie. Po leczeniu ta współpraca się rozpadła, a aktywność AKT spadła, jeszcze bardziej przesuwając bilans w stronę śmierci komórki. Co ważne, zmiany te były wyraźne w komórkach czerniaka, ale nie w komórkach niekancerogennych, co sugeruje okno terapeutyczne, w którym guz jest silnie atakowany, a tkanka zdrowa oszczędzana.
Uczynienie guzów bardziej widocznymi dla „oddziałów uderzeniowych” układu odpornościowego
Groźba czerniaka wynika też z jego umiejętności unikania nadzoru immunologicznego. Naukowcy zapytali więc, co dzieje się z komórkami nowotworowymi, które przetrwają niskie dawki inhibitorów TRPM8 przez dłuższy czas. Odkryli, że te pozostające komórki zaczęły wystawiać więcej markera powierzchniowego zwanego ULBP1, który działa jak sygnał alarmowy rozpoznawany przez receptory NKG2D na komórkach NK. Inne powiązane markery nie uległy zmianie, co wskazuje na efekt selektywny. W trójwymiarowych sferoidach czerniaka, które lepiej naśladują prawdziwe guzy, przedleczenie inhibitorami TRPM8 nie tylko zmniejszało rozmiary struktur i zwiększało śmiertelność komórek, lecz także czyniło je znacznie bardziej podatnymi na atak komórek NK. Gdy ULBP1 lub NKG2D były blokowane przeciwciałami, dodatkowe zabijanie w dużej mierze znikało, co pokazuje, że poprawione usuwanie przez układ odpornościowy przebiega poprzez tę specyficzną interakcję między guzem a komórkami NK. 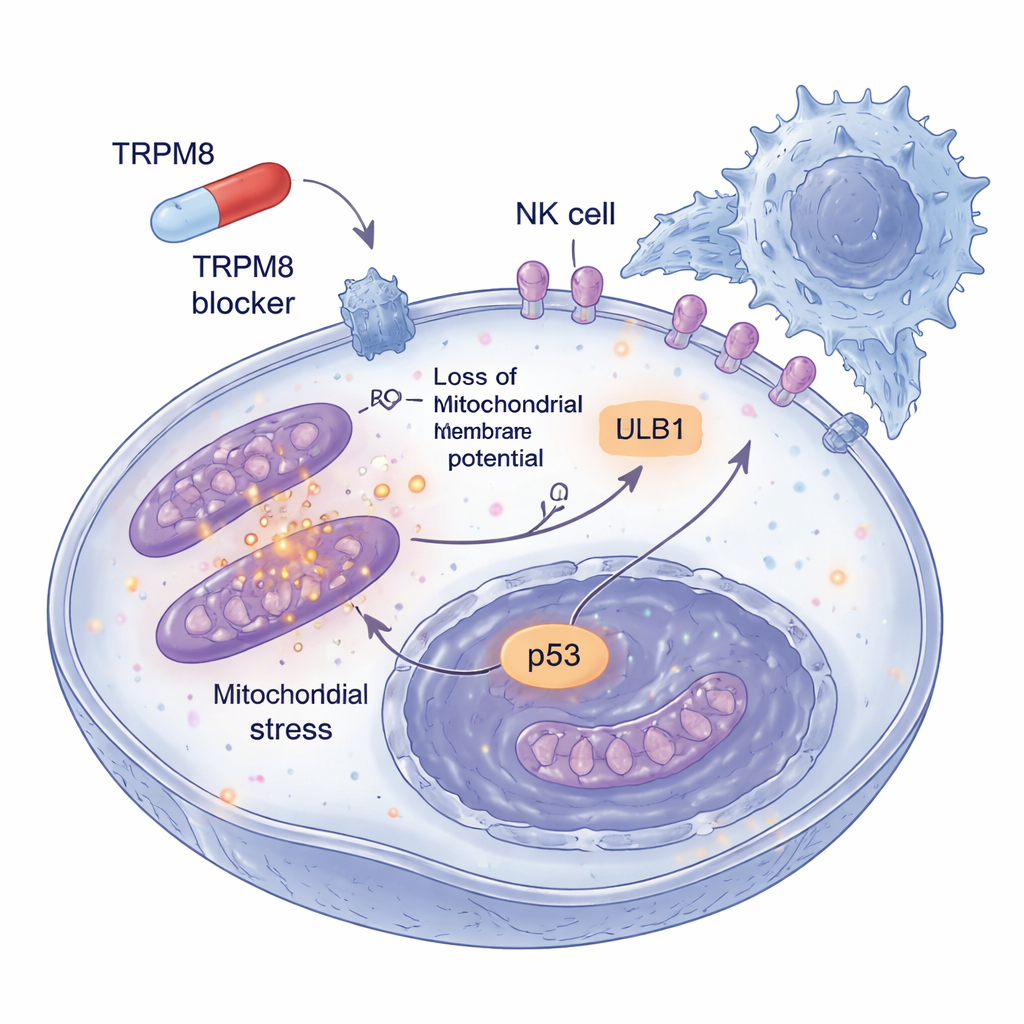
Co to może oznaczać dla przyszłej opieki nad czerniakiem
Mówiąc prosto: zablokowanie „czujnika zimna” TRPM8 zmienia go w dźwignię terapeutyczną — prowadzi komórki czerniaka do śmiertelnego kryzysu mitochondrialnego i uszkodzeń DNA, a jednocześnie oznacza je do zniszczenia przez komórki NK. Ponieważ leki oszczędzają zdrowe komórki skóry i nie szkodzą samym komórkom NK, stanowią obiecującą podstawę do nowych terapii. Autorzy sugerują, że inhibitory TRPM8 mogłyby być łączone z istniejącymi immunoterapiami, aby atakować zaawansowanego, opornego na leki czerniaka na dwóch frontach: bezpośrednio zabijając komórki nowotworowe i ułatwiając układowi odpornościowemu znalezienie i zniszczenie ocalałych komórek.
Cytowanie: Sorrentino, C., Lauretta, C., D’Angiolo, R. et al. Rewiring melanoma cell fate: TRPM8 modulators trigger apoptosis and boost NK cell cytotoxicity. Cell Death Dis 17, 223 (2026). https://doi.org/10.1038/s41419-026-08469-8
Słowa kluczowe: czerniak, TRPM8, mitochondria, stres oksydacyjny, komórki natural killers