Clear Sky Science · pl
Laktylacja napędzająca TRIM29 wywołuje inwazyjne zachowanie i przerzutowanie do węzłów chłonnych w raku żołądka za pośrednictwem szlaku Wnt/β-katenina zależnego od hnRNPA1
Dlaczego to badanie ma znaczenie
Rak żołądka jest jednym z najgroźniejszych nowotworów na świecie w dużej mierze dlatego, że wcześnie rozprzestrzenia się do pobliskich węzłów chłonnych, co utrudnia wyleczenie chirurgiczne. W tym badaniu wyjaśniono, jak chemiczna modyfikacja powiązana z metabolizmem guza aktywuje białko TRIM29, pomagając komórkom nowotworowym naciekać otaczającą tkankę, tworzyć nowe naczynia limfatyczne i opierać się chemioterapii. Zrozumienie tego łańcucha zdarzeń wskazuje nowe sposoby na spowolnienie lub nawet zablokowanie rozprzestrzeniania się raka żołądka.
Niebezpieczne partnerstwo w guzach żołądka
Naukowcy zaczęli od porównania próbek raka żołądka z przylegającą zdrową tkanką od 100 pacjentów oraz analizy dużych publicznych baz danych genowych. Stwierdzili, że TRIM29, białko wcześniej powiązane z regulacją układu odpornościowego i innymi nowotworami, jest konsekwentnie bardziej obecne w komórkach nowotworowych. Pacjenci, których guzy miały wyższy poziom TRIM29, częściej wykazywali zajęcie węzłów chłonnych i naczyń krwionośnych oraz mieli gorsze przeżycie ogólne. Wzorce te sugerowały, że TRIM29 nie tylko występuje, lecz aktywnie przyczynia się do bardziej agresywnego zachowania raka żołądka.
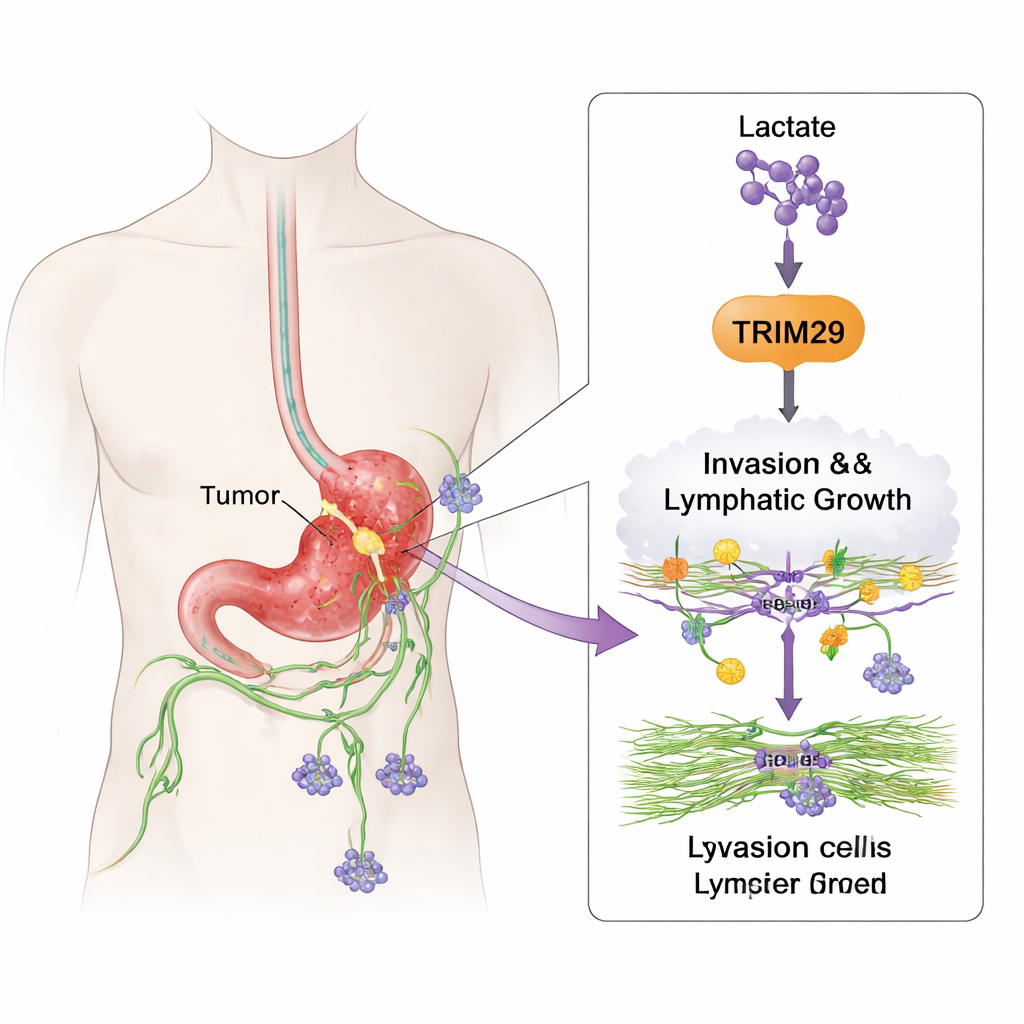
Jak komórki nowotworowe uczą się podróżować
Aby sprawdzić, co TRIM29 faktycznie robi, zespół zmieniał jego poziomy w liniach komórkowych raka żołądka. Gdy obniżono TRIM29, komórki stały się wyraźnie mniej ruchome i mniej zdolne do przeciskania się przez trójwymiarowe żele imitujące tkankę. Zwiększenie TRIM29 działało odwrotnie, czyniąc komórki bardziej inwazyjnymi. Badano także komórki śródbłonka limfatycznego, które wyścielają naczynia limfatyczne. Komórki nowotworowe bogate w TRIM29 stymulowały te komórki naczyniowe do rozgałęziania się i tworzenia struktur przypominających kanaliki, co jest oznaką powstawania nowych naczyń limfatycznych (limfangiogenezy). W modelach mysiich guzy z wysokim poziomem TRIM29 dawały więcej przerzutów do wątroby i węzłów chłonnych, podczas gdy guzy z obniżonym TRIM29 rozprzestrzeniały się mniej i tworzyły mniej naczyń limfatycznych.
Przekaźnik molekularny: ochrona kluczowego regulatora
Zagłębiając się w mechanizmy, naukowcy odkryli, że TRIM29 fizycznie wiąże się z innym białkiem, hnRNPA1, które wpływa na przetwarzanie genów i jest powiązane z rozprzestrzenianiem się nowotworów. Zwykle hnRNPA1 może zostać oznaczony do degradacji przez kolejne białko — enzym ZFP91 — w ramach systemu komórkowego usuwania odpadów. TRIM29 zakłóca ten proces, konkurując z ZFP91 o wiązanie do hnRNPA1. Gdy TRIM29 jest obfity, chroni hnRNPA1 przed znakowaniem i rozpadem. W rezultacie hnRNPA1 staje się bardziej stabilny i gromadzi się w komórkach nowotworowych, uruchamiając kaskadę sygnałową, która kończy się aktywacją szlaku Wnt/β-katenina — dobrze znanego czynnika napędzającego wzrost i migrację guza. To z kolei zwiększa produkcję VEGF‑C, cząsteczki stymulującej powstawanie nowych naczyń limfatycznych, dając komórkom nowotworowym więcej „dróg” ucieczki.
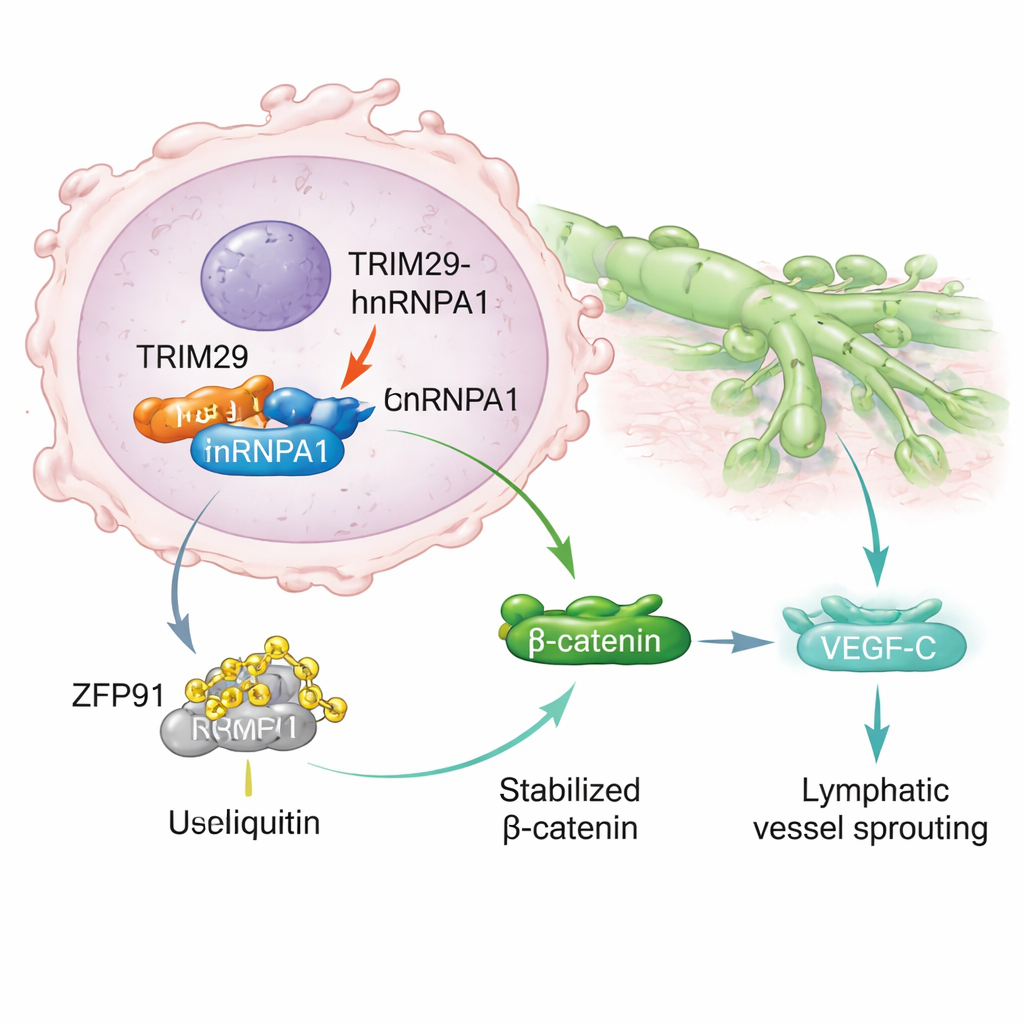
Napędzanie raka przez mleczan
Badanie łączy także to inwazyjne zachowanie z tym, jak guzy przetwarzają cukier. Szybko rosnące nowotwory często polegają na metabolizmie produkującym duże ilości mleczanu — produktu ubocznego niegdyś uznawanego za bezużyteczny odpad. Autorzy pokazują, że mleczan może chemicznie modyfikować białka histonowe, które porządkują DNA, konkretnie w miejscu zwanym H3K9. Ta „laktylacja” działa jak włącznik dla genu TRIM29, zwiększając jego aktywność. Gdy za pomocą leków metabolicznych obniżano produkcję mleczanu, poziomy TRIM29 spadały; gdy podnoszono mleczan, TRIM29 rosło. Tkanki raka żołądka od pacjentów wykazywały wyższe poziomy tej laktylacji H3K9, co korelowało z wyższym TRIM29, większym zajęciem węzłów chłonnych i gorszym przeżyciem. W istocie zmieniony metabolizm guza pomaga zaprogramować bardziej agresywny profil genetyczny.
Nowe sposoby wzmocnienia chemioterapii
Naczynia limfatyczne robią więcej niż tylko przewożą komórki nowotworowe; mogą także odprowadzać leki chemioterapeutyczne z guzów. Używając przerzutów pobranych od pacjentów i hodowanych w myszach, badacze sprawdzili, czy blokowanie TRIM29 i wzrostu naczyń limfatycznych może poprawić działanie 5‑fluorouracylu (5‑FU), standardowego leku w raku żołądka. Hamowanie TRIM29 lub blokowanie limfangiogenezy z osobna zwiększało efektywność 5‑FU w zmniejszaniu guzów i ograniczaniu podziałów komórek. Połączenie obu strategii dało najsilniejszą odpowiedź, sugerując potencjalny sposób przezwyciężenia niektórych form oporności na leki w zaawansowanej chorobie.
Co to znaczy dla pacjentów
Ta praca przedstawia krok po kroku obraz: guzy żołądka produkują nadmiar mleczanu, który włącza TRIM29; TRIM29 następnie chroni hnRNPA1, stabilizuje szlak wzrostu i zwiększa tworzenie naczyń limfatycznych oraz rozprzestrzenianie się do węzłów chłonnych. Klinicznie wysoki poziom TRIM29 i powiązane znaki laktylacji identyfikują pacjentów o wyższym ryzyku agresywnej choroby. W przyszłości leki zmniejszające sygnalizację mleczanu, blokujące TRIM29 lub zapobiegające tworzeniu naczyń limfatycznych mogłyby być łączone z istniejącą chemioterapią, aby powstrzymać rozprzestrzenianie się raka żołądka i poprawić skuteczność leczenia.
Cytowanie: Hua, R., Yu, J., Niu, Y. et al. Lactylation-drived TRIM29 induces invasive behavior and lymph node metastasis in gastric cancer via hnRNPA1-mediated Wnt/β-catenin pathway. Cell Death Dis 17, 222 (2026). https://doi.org/10.1038/s41419-026-08468-9
Słowa kluczowe: przerzuty raka żołądka, TRIM29, mleczan i laktylacja, limfangiogeneza, szlak Wnt beta-katenina