Clear Sky Science · pl
KIF20A hamuje ubikwitynację DHX9 zależną od TRIM21, zwiększając stabilność SOX2, co wzmacnia cechy macierzyste OSCC i odporność na ferroptozę
Dlaczego to badanie ma znaczenie dla pacjentów z rakiem jamy ustnej
Płaskonabłonkowy rak jamy ustnej, częsta postać raka w ustach, często nawraca i wykazuje oporność na leczenie. Wiele niepowodzeń chirurgii, chemioterapii i radioterapii można przypisać małej, uporczywej populacji „komórek macierzystych nowotworu”, które potrafią na nowo odtworzyć guz i opierać się śmierci komórkowej. To badanie odsłania kluczowy układ molekularny, który pomaga tym komórkom przetrwać i opierać się nowemu typowi śmierci komórkowej zwanemu ferroptozą, oraz wskazuje strategię lekową, która mogłaby poprawić skuteczność standardowej chemioterapii.
Ukryty czynnik napędowy w guzach jamy ustnej
Naukowcy zaczęli od porównania próbek nowotworowych pacjentów z rakiem jamy ustnej z przylegającą zdrową tkanką. Stwierdzili, że białko o nazwie KIF20A było konsekwentnie znacznie wyższe w komórkach nowotworowych. Analiza większych zbiorów danych pacjentów wykazała, że osoby, których guzy miały wyższe poziomy KIF20A, miały skłonność do krótszego przeżycia, co sugeruje związek tego białka z bardziej agresywną chorobą. 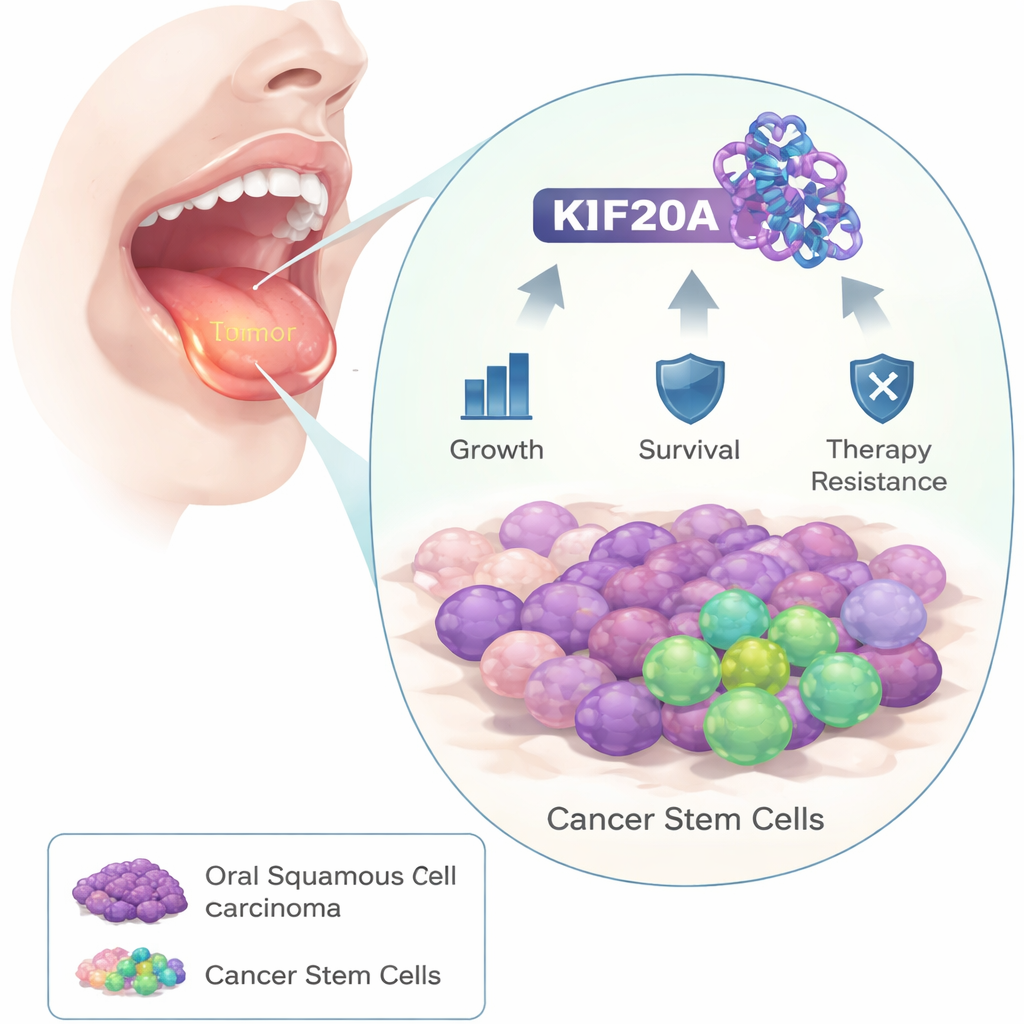
Jak KIF20A chroni kluczowego pomocnika RNA
Aby zrozumieć, co KIF20A właściwie robi, zespół zastosował metody mapowania białek, by znaleźć jego partnerów wewnątrz komórek nowotworowych. Centralnym partnerem okazał się DHX9, białko pomagające w zarządzaniu cząsteczkami RNA i wpływające na czas trwania niektórych komunikatów w komórce. Naukowcy odkryli, że KIF20A wiąże się z DHX9 i zapobiega jego oznaczaniu do zniszczenia przez inne białko — ligazę E3 TRIM21, która zwykle znaczuje DHX9 łańcuchami ubikwityny kierującymi go do komórkowego „niszczarki” białek. Blokując to znakowanie, KIF20A spowalnia rozkład DHX9 i zwiększa jego poziomy, szczególnie w cytoplazmie, gdzie może działać na określone cele RNA.
Od stabilności RNA do komórek macierzystych nowotworu i odporności na ferroptozę
Dzięki stabilniejszemu DHX9 pojawia się kolejny kluczowy gracz: SOX2, gen-mistrz, który pomaga komórkom zachować stan podobny do macierzystego i opierać się leczeniu. Badanie wykazuje, że DHX9 chroni komunikat RNA SOX2 przed rozpadem, co pozwala na wytwarzanie większej ilości białka SOX2. W komórkach raka jamy ustnej nadmiar KIF20A prowadził do wyższych poziomów DHX9 i SOX2, większego formowania kulistych struktur nowotworowych w hodowli oraz wyższego odsetka komórek wyrażających markery komórek macierzystych — objawów silniejszej „macierzystości nowotworowej”. KIF20A zmniejszał też wrażliwość komórek na ferroptozę, rodzaj śmierci komórkowej napędzanej żelazem i związanej z lipidami, który jest badany jako sposób zabijania opornych komórek nowotworowych. Po wyłączeniu KIF20A guzy u myszy szybciej się zmniejszały, a markery ferroptozy wzrastały, wskazując, że guzy utraciły tę ochronną tarczę.
Obwód molekularny z podatnym na leki słabym ogniwem
Łącząc te elementy, autorzy proponują oś KIF20A–DHX9–SOX2: KIF20A stabilizuje DHX9, DHX9 stabilizuje RNA SOX2, a SOX2 z kolei utrzymuje komórki macierzyste nowotworu i blokuje ferroptozę. Ten obwód wpływa także na szlak PI3K–AKT, główną drogę wzrostu i przeżycia w wielu nowotworach. 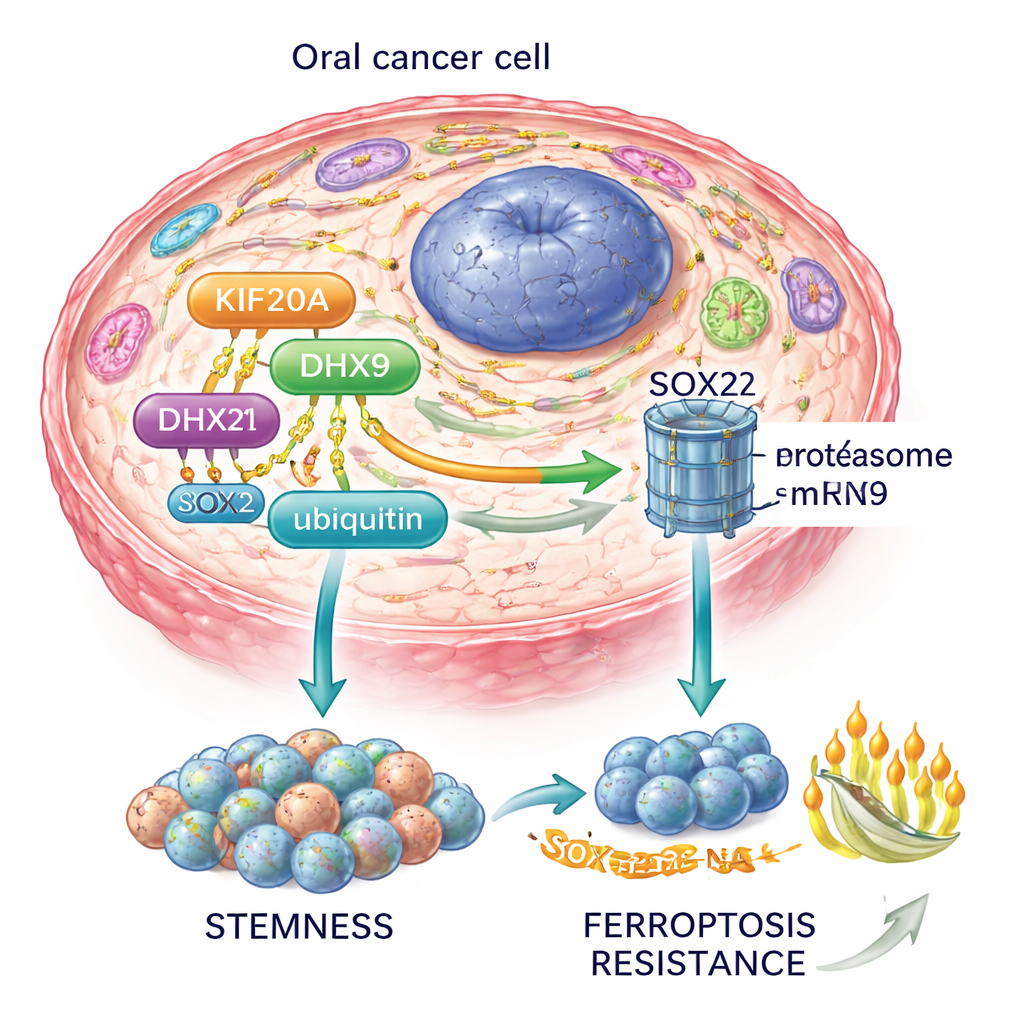
Kandydat na lek osłabiający odporne guzy
Aby zrobić krok w kierunku terapii, zespół przeszukał duże bazy danych lek–gen w poszukiwaniu związków przewidywanych jako przeciwdziałające wzorcom genowym związanym z KIF20A. Zidentyfikowali ENMD-2076, doustny inhibitor kinaz wielokrotnego celu, wcześniej testowany w innych nowotworach. W komórkach raka jamy ustnej z wysokim KIF20A ENMD-2076 obniżał poziomy KIF20A, DHX9 i SOX2, tłumił sygnalizację związaną z cechami macierzystości i hamował wzrost. W połączeniu ze standardowym lekiem chemioterapeutycznym cisplatyną, ENMD-2076 wywołał silniejszy efekt przeciwnowotworowy niż którakolwiek z substancji stosowanych osobno, zarówno w hodowlach komórkowych, jak i w guzach mysich, bez wyraźnego wzrostu toksyczności.
Co to oznacza dla przyszłych terapii
Dla czytelnika niebędącego specjalistą najważniejsze wnioski są takie: badanie ujawnia, jak jedno nadaktywne białko, KIF20A, pomaga guzom jamy ustnej utrzymać małą pulę „nasion” komórkowych przy życiu i chronić je przed obiecującą formą śmierci komórkowej. Mapując tę ścieżkę — od KIF20A przez DHX9 do SOX2 — badacze wskazują nowe cele terapeutyczne i pokazują, że istniejący eksperymentalny lek ENMD-2076 może osłabić tę oś i zwiększyć skuteczność cisplatyny w modelach. Choć potrzebne są dalsze prace nad bezpieczeństwem i potwierdzeniem korzyści u pacjentów, ustalenia wspierają perspektywę, w której blokowanie tego obwodu mogłoby pomóc zapobiegać nawrotom i przezwyciężać oporność na leki w raku jamy ustnej.
Cytowanie: Zhang, Z., Li, Y., Hu, J. et al. KIF20A inhibits TRIM21-dependent ubiquitination of DHX9 to boost SOX2 stability, enhancing OSCC stemness and ferroptosis resistance. Cell Death Dis 17, 218 (2026). https://doi.org/10.1038/s41419-026-08467-w
Słowa kluczowe: płaskonabłonkowy rak jamy ustnej, komórki macierzyste nowotworu, ferroptoza, KIF20A, SOX2