Clear Sky Science · pl
Selenometionina jako inhibitor ferroptozy działający dwiema drogami: dostarczanie selenu napędzające biosyntezę GPX4 poza transsulfuracją oraz zdolność redukcyjna do usuwania ROS niezależna od aktywności GPX4
Dlaczego warto chronić komórki przed „rdzewiejącą” śmiercią
Komórki w naszym organizmie mogą umierać na różne sposoby, a jednym z najnowszych i najciekawszych jest ferroptoza — rodzaj napędzanych przez żelazo uszkodzeń błon komórkowych przypominających rdzewienie. Proces ten jest powiązany z chorobami od uszkodzeń nerek po neurodegenerację. Pierwiastek śladowy selenium, znany wielu osobom z suplementów diety, odgrywa kluczową rolę w powstrzymywaniu tej niebezpiecznej formy śmierci komórek. W badaniu zbadano, jak powszechny aminokwas zawierający selen, selenometionina, może chronić komórki przed ferroptozą, stosując nie jedną, lecz dwie odrębne strategie ochronne.
Nowy obrońca znaleziony w szerokim przeszukiwaniu leków
Aby znaleźć małe cząsteczki blokujące ferroptozę, badacze przeskanowali tysiące związków z bibliotek leków zatwierdzonych przez FDA i produktów naturalnych. Do wywołania ferroptozy w liniach komórek nowotworowych ludzkich użyli związku chemicznego RSL3, a następnie monitorowali śmierć komórek oraz gromadzenie się uszkodzonych, zoksydowanych lipidów w błonach. Spośród wszystkich kandydatów selenometionina wyróżniła się jako silny środek ochronny: zmniejszała zarówno uszkodzenia lipidów, jak i śmierć komórek w różnych typach komórek i w dwóch głównych modelach ferroptozy — jednym wywołanym bezpośrednią inhibicją GPX4 (RSL3) i drugim przez pozbawienie komórek cystyny, budulca antyoksydantu glutathionu. Wyniki te wskazały selenometioninę jako szeroki i odporny inhibitor ferroptozy. 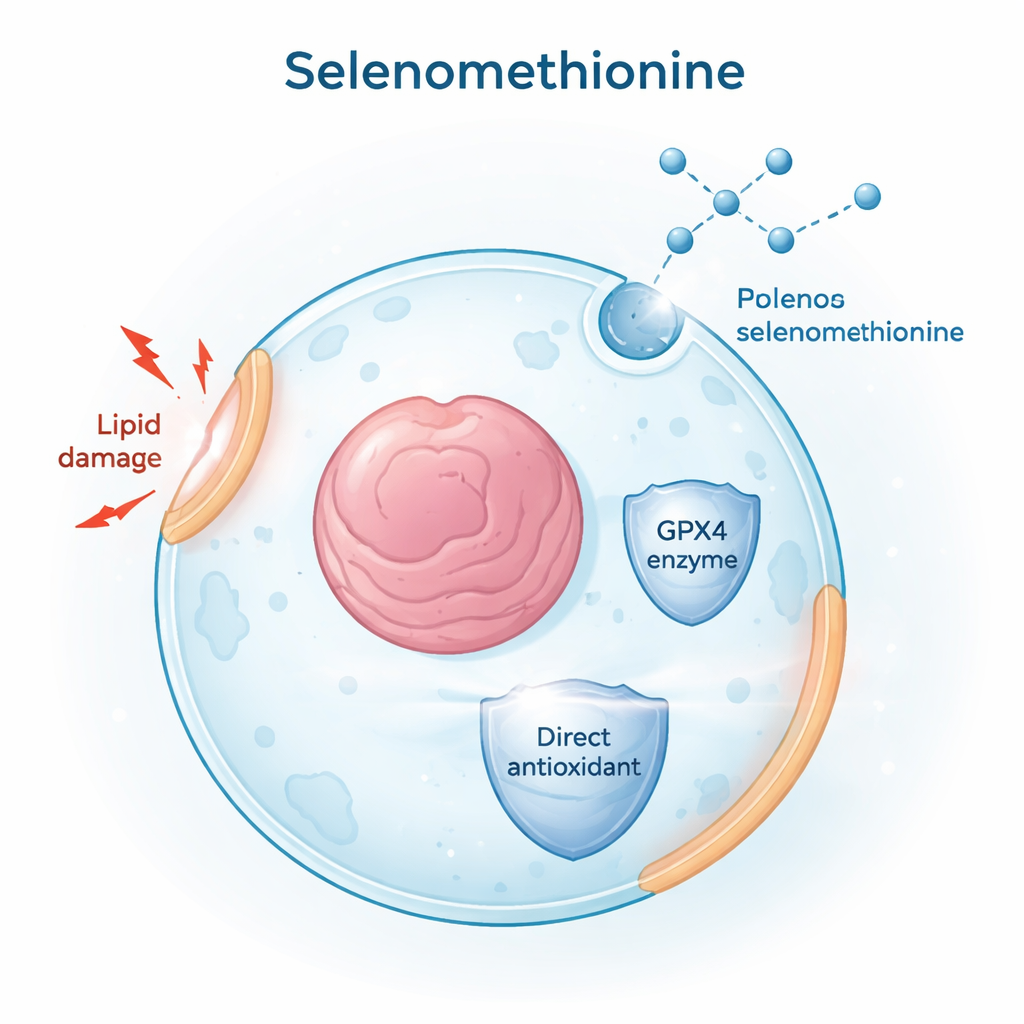
Dostarczenie selenu dla kluczowego enzymu ochronnego
Rdzeniową tarczą anty-ferroptotyczną w komórkach jest enzym GPX4, który do funkcjonowania wymaga selenu. Zespół postanowił ustalić, czy selenometionina jedynie zasila tę ścieżkę, czy robi coś więcej. Śledzili, jak selen pochodzący z selenometioniny może być przekształcony w formy odpowiednie do budowy GPX4, nawet gdy zwykła droga, zwana ścieżką transsulfuracji, była upośledzona lub zablokowana. Przy użyciu wyciszeń genowych i inhibitorów chemicznych enzymów uczestniczących w szlakach siarkowo‑selenowych stwierdzili, że selenometionina nadal zwiększała poziomy GPX4 i chroniła komórki. Pokazało to, że komórki potrafią wykorzystywać wiele dróg metabolicznych do pozyskiwania selenu z selenometioniny i podtrzymywania produkcji GPX4, nawet w tkankach, gdzie klasyczna ścieżka jest słaba.
Ochrona niezależna od zwykłego enzymu
Zaskakująco, gdy badacze całkowicie usunęli GPX4 z komórek za pomocą edycji genów CRISPR, selenometionina nadal chroniła przed ferroptozą. Nadal zmniejszała uszkodzenia lipidów błonowych i śmierć komórek, co wskazuje, że GPX4 nie wyjaśnia całej ochrony. Dalsze eksperymenty zasugerowały, że część tej ochrony wynika z włączenia selenometioniny do nowo syntetyzowanych białek, lecz to stanowi tylko część efektu. Autorzy skupili się następnie na reaktywności chemicznej samej selenometioniny. Odkryli, że może ona bezpośrednio neutralizować reaktywne formy tlenu (ROS), w tym nadtlenek wodoru, i jest przekształcana w utlenioną formę — sulfoxyd. Spektrometria mas potwierdziła ten produkt, a podanie komórkom wersji sulfoxydowej również zmniejszało ferroptozę, co sugeruje, że komórki mogą w cyklu redoks odzyskiwać ją z powrotem do aktywnej selenometioniny.
Z hodowli komórkowej do ochrony nerek u żywych zwierząt
Aby sprawdzić, czy te mechanizmy mają znaczenie w całym organizmie, zespół użył modelu myszy z ostrą niewydolnością nerek wywołaną lekiem przeciwnowotworowym cisplatyną, schorzeniem związanym z ferroptozą. Myszy leczone cisplatyną wykazywały spadek masy ciała, powiększenie nerek, pogorszenie funkcji nerek oraz wysokie poziomy markerów ferroptozy. Gdy zwierzęta otrzymywały selenometioninę, wiele z tych problemów uległo poprawie: masa ciała się odzyskała, obrzęk nerek zmniejszył się, parametry krwi świadczące o funkcji nerek normowały się, sygnały zapalne spadły, a chemiczne markery uszkodzenia lipidów zmalały. Tkanka nerkowa wykazywała też wyższe poziomy GPX4 i mniej uszkodzeń strukturalnych. Korzyści te były porównywalne do obserwowanych po zastosowaniu ferrostatyny-1, znanego eksperymentalnego inhibitora ferroptozy. 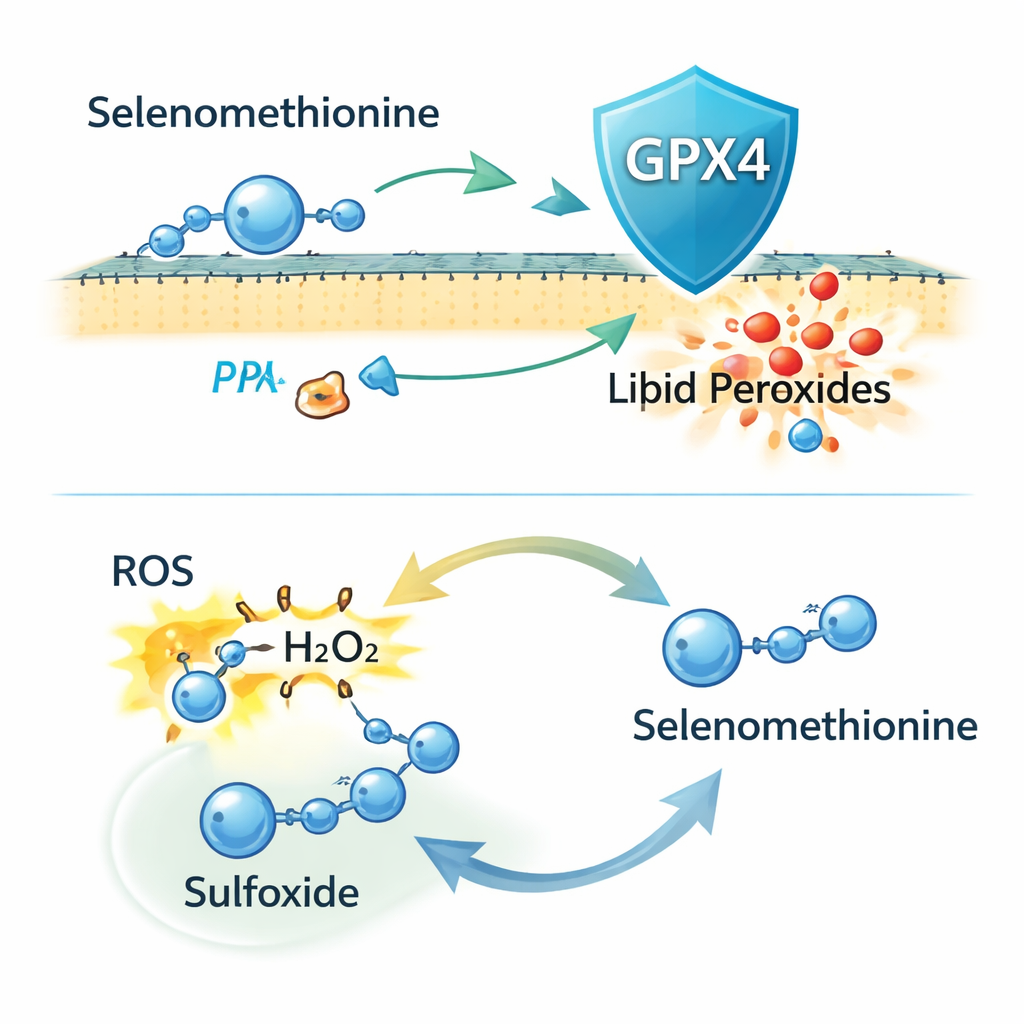
Co to oznacza dla przyszłych terapii
W prostych słowach praca ta sugeruje, że selenometionina działa jak dwufunkcyjny gaśniczy przeciw żelazowo-napędzanemu „rdzewieniu” błon komórkowych. Z jednej strony dostarcza selenu, dzięki czemu komórki mogą syntetyzować więcej enzymu GPX4, który pełni rolę wewnętrznego zespołu sprzątającego uszkodzone lipidy. Z drugiej strony sama selenometionina może pochłaniać szkodliwe utleniacze i być poddawana recyklingowi, oferując ochronę niezależną od GPX4. W połączeniu te cechy czynią selenometioninę obiecującym kandydatem do zapobiegania lub leczenia chorób, w których ferroptoza odgrywa centralną rolę, takich jak uszkodzenia nerek wywołane lekami, a potencjalnie także inne stany napędzane nadmiernym stresem oksydacyjnym.
Cytowanie: Xia, C., Sun, X., Shao, J. et al. Selenomethionine as a dual-mechanism ferroptosis inhibitor: selenium-supply-driven GPX4 biosynthesis beyond transsulfuration and reductive-capacity-mediated ROS scavenging independent of GPX4 activity. Cell Death Dis 17, 224 (2026). https://doi.org/10.1038/s41419-026-08466-x
Słowa kluczowe: ferroptoza, selen, selenometionina, stres oksydacyjny, ostra niewydolność nerek