Clear Sky Science · pl
Składnik chaperoniny TRiC, Cct3, jest niezbędny dla transportu aksonalnego, mielinizacji i dojrzewania złącza nerwowo‑mięśniowego
Kiedy okablowanie nerwowe zawodzi
Nasze mózgi i ciała polegają na długich, przypominających kable włóknach nerwowych, które przekazują sygnały szybko i niezawodnie. Aby spełniać tę funkcję, wiele nerwów jest owiniętych izolacyjną mieliną, a ich zakończenia muszą tworzyć precyzyjne kontakty z mięśniami. W artykule badano, co się dzieje, gdy zawodzi kluczowy „pomocnik” komórkowy odpowiedzialny za fałdowanie białek, zwany Cct3. Na przykładzie zebrafish i tkanek ludzkich autorzy pokazują, jak pojedynczy składnik dużej maszyny chaperonowej może zakłócić mielinę, połączenia nerwowo‑mięśniowe oraz wewnętrzny system transportowy, który utrzymuje neurony przy życiu i sprawne.
Komórkowy krawiec budujący neurony
W każdej komórce nowo zsyntetyzowane białka muszą przyjmować właściwe kształty, podobnie jak przy starannym szyciu garnituru. Kompleks TRiC, którego częścią jest podjednostka Cct3, jest jednym z głównych „krawców”, pomagającym prawidłowo fałdować około 10% wszystkich białek komórkowych — zwłaszcza białka strukturalne, takie jak aktyna i tubulina. Te elementy budulcowe tworzą wewnętrzny szkielet komórki i tory, po których przemieszczane są niezbędne ładunki. U pacjentów z wadliwymi wersjami CCT3 i powiązanych genów obrazy mózgu wykazują zmniejszoną istotę białą (bogate w mielinę okablowanie mózgu) oraz problemy z nerwami obwodowymi i mięśniami. Autorzy postanowili zrozumieć, jak utrata Cct3 wytrąca z równowagi rozwój i funkcję układu nerwowego.
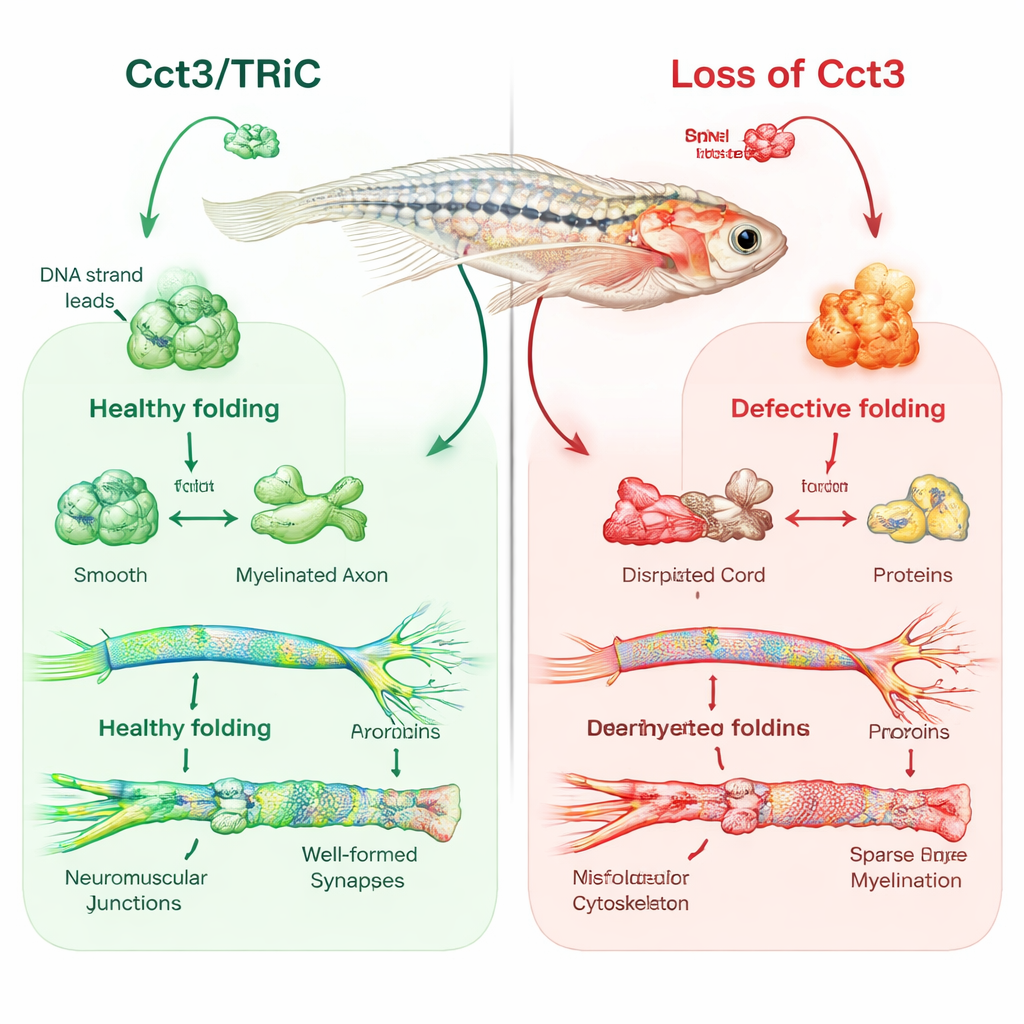
Zebrafish jako okno na izolację nerwów
Zespół zastosował edycję genów CRISPR/Cas9, aby uzyskać zebrafish pozbawione funkcjonalnego cct3. Te małe rybki miały mniejsze mózgi i oczy, gromadzenie płynu wokół serca, słabe reakcje na dotyk i ginęły w ciągu kilku dni. Gdy badacze przywrócili prawidłowe cct3, wstrzykując jego mRNA, wiele z tych defektów uległo poprawie, co potwierdziło, że utrata Cct3 była przyczyną. Koncentrując się na mielinie, użyli znaczników fluorescencyjnych i mikroskopii elektronowej, aby zobrazować warstwy izolacyjne otaczające włókna nerwowe. U normalnych rybek komórki tworzące mielinę w mózgu i nerwach obwodowych owijały aksony w porządne, warstwowe pochewki na czwarty dzień rozwoju. W przeciwieństwie do tego, mutanty cct3 miały znacznie mniej komórek mielinizujących i w istocie brak prawidłowej mieliny wokół wielu aksonów, mimo że na powierzchni aksony wydawały się mieć normalny kształt.
Krucha komórkowa pomoc i przeciążone połączenia nerwowo‑mięśniowe
Aby ustalić, dlaczego brakowało mieliny, autorzy zbadali komórki Schwanna i pokrewne komórki grzebienia nerwowego — komórki pomocnicze owijające nerwy obwodowe. U zdrowych rybek te komórki wydłużały cienkie wypustki, a potem dopracowywały swój kształt podczas tworzenia segmentów mieliny. U mutantów zaokrąglały się, skracały wypustki i ulegały fragmentacji. Ich jądra rozpadały się w typowym wzorze martwicy zaprogramowanej, a pojawienie się znacznika śmierci (aktywowanej kaspazy 3) wskazywało, że wiele z tych komórek obumierało przedwcześnie. Tymczasem na złączach nerwowo‑mięśniowych, gdzie nerwy łączą się z mięśniami, wzór „ognisk” receptorów na mięśniach nie ulegał dopracowaniu. Zamiast wielu małych, precyzyjnych skupień, mutanty miały mniej, większych plam receptorów, co przypomina uproszczone fałdowania synaptyczne zaobserwowane u pacjenta z mutacją CCT3.
Uszkodzone wewnętrzne tory i spowolniony ruch ładunków
Ponieważ TRiC pomaga fałdować aktynę i tubulinę, autorzy szczegółowo przyjrzeli się wewnętrznemu szkielecikowi aksonów ruchowych. Stwierdzili, że ogólne poziomy tubuliny były wyraźnie obniżone u mutantów, a liczba prawidłowych mikrotubul — pustych rurek pełniących rolę torów dla transportu — dramatycznie spadła zarówno w nerwach centralnych, jak i obwodowych. Chemiczne „znaczniki” na tubulinie, istotne dla stabilnych, zdolnych do transportu mikrotubul, również były poważnie zmienione. Dzięki obrazowaniu na żywo świecących mitochondriów i endosomów wewnątrz aksonów ruchowych zaobserwowali, jak te ładunki się poruszają. U zdrowych rybek organelle przemieszczały się szybko i kierunkowo wzdłuż aksonu. U mutantów wiele organelli zatrzymywało się lub jedynie kołysało tam i z powrotem, co odpowiada uszkodzonym torom i zaburzonemu transportowi.
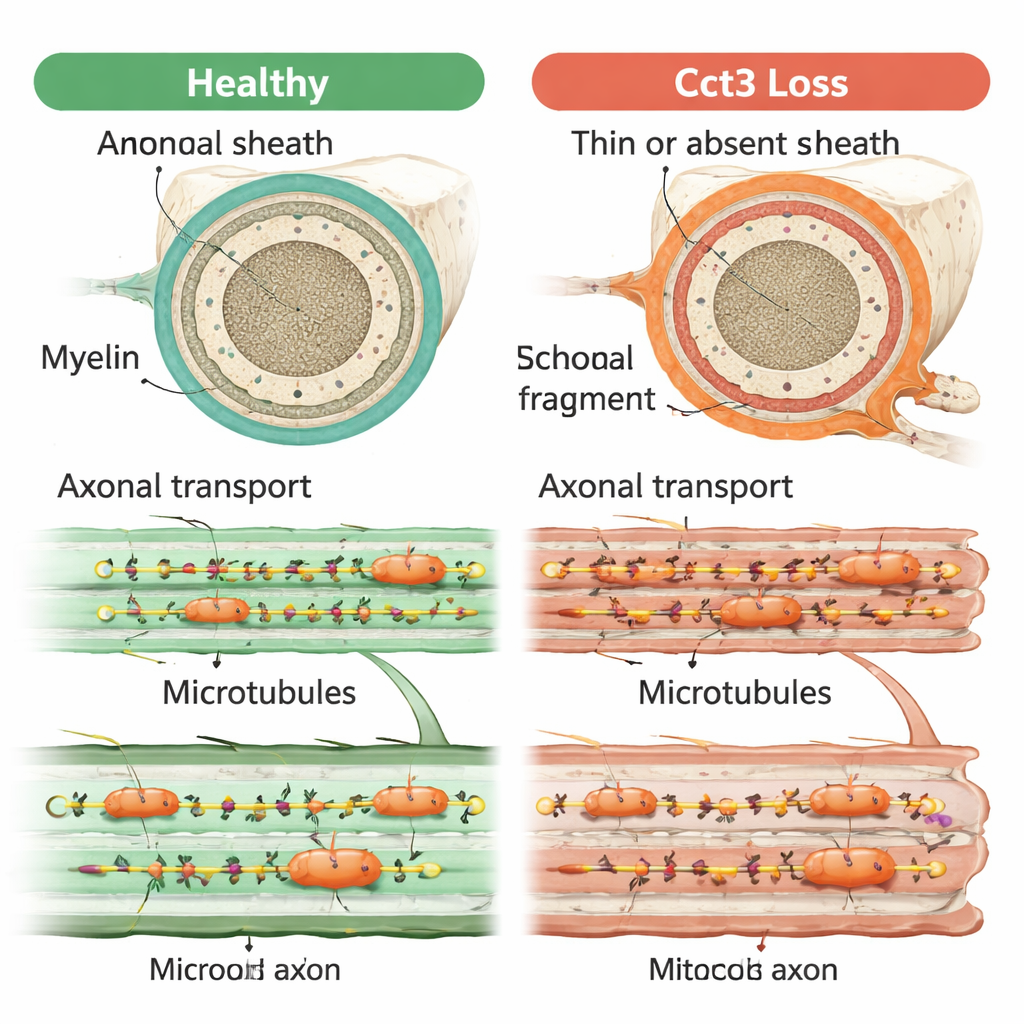
Jeden podstawowy problem odpowiadający za wiele objawów
Podsumowując, wyniki pokazują, że Cct3 jest niezbędny dla kilku powiązanych aspektów zdrowia nerwów: wspiera przetrwanie komórek pomocniczych tworzących mielinę, umożliwia prawidłowe owijanie mieliny oraz pozwala dojrzewającym złączom nerwowo‑mięśniowym na precyzyjne ukształtowanie. Wszystkie te role można sprowadzić do jego funkcji w fałdowaniu i utrzymaniu białek budujących cytoszkielet oraz mikrotubul — torów używanych do transportu aksonalnego. Gdy te tory zawodzą, kluczowe sygnały i materiały nie mogą dotrzeć we właściwe miejsca wzdłuż włókna nerwowego, co prawdopodobnie podważa zarówno komunikację z komórkami tworzącymi mielinę, jak i formowanie kontaktów nerwowo‑mięśniowych. Praca ta sugeruje, że upośledzony transport aksonalny może być wspólną nitką łączącą różnorodne problemy mózgowe i nerwowe obserwowane w zaburzeniach związanych z TRiC.
Cytowanie: Zhang, X., Zajt, K.K., Palaz, T. et al. The chaperonin TRiC component Cct3 is required for axonal transport, myelination, and neuromuscular junction refinement. Cell Death Dis 17, 221 (2026). https://doi.org/10.1038/s41419-026-08465-y
Słowa kluczowe: mielinizacja, transport aksonalny, złącze nerwowo‑mięśniowe, chaperony molekularne, model zebrafish