Clear Sky Science · pl
Nieprawidłowy transport i sygnalizacja BDNF–TrkB w neuronach istoty podstawnej mózgu w zespole Downa
Dlaczego to badanie mózgu ma znaczenie
Osoby z zespołem Downa żyją dłużej niż kiedykolwiek, ale jednocześnie mają bardzo wysokie ryzyko rozwoju demencji podobnej do choroby Alzheimera w wieku średnim. To badanie zagląda głęboko do pojedynczych komórek mózgowych, aby zrozumieć, dlaczego niektóre neurony są tak podatne na uszkodzenie. Śledząc, jak te komórki przemieszczają i reagują na kluczową cząsteczkę pełniącą rolę „nawozu” dla mózgu, badacze odkrywają zator wewnątrz neuronów, który może wyjaśniać utratę pamięci i wskazywać nowe strategie terapeutyczne.
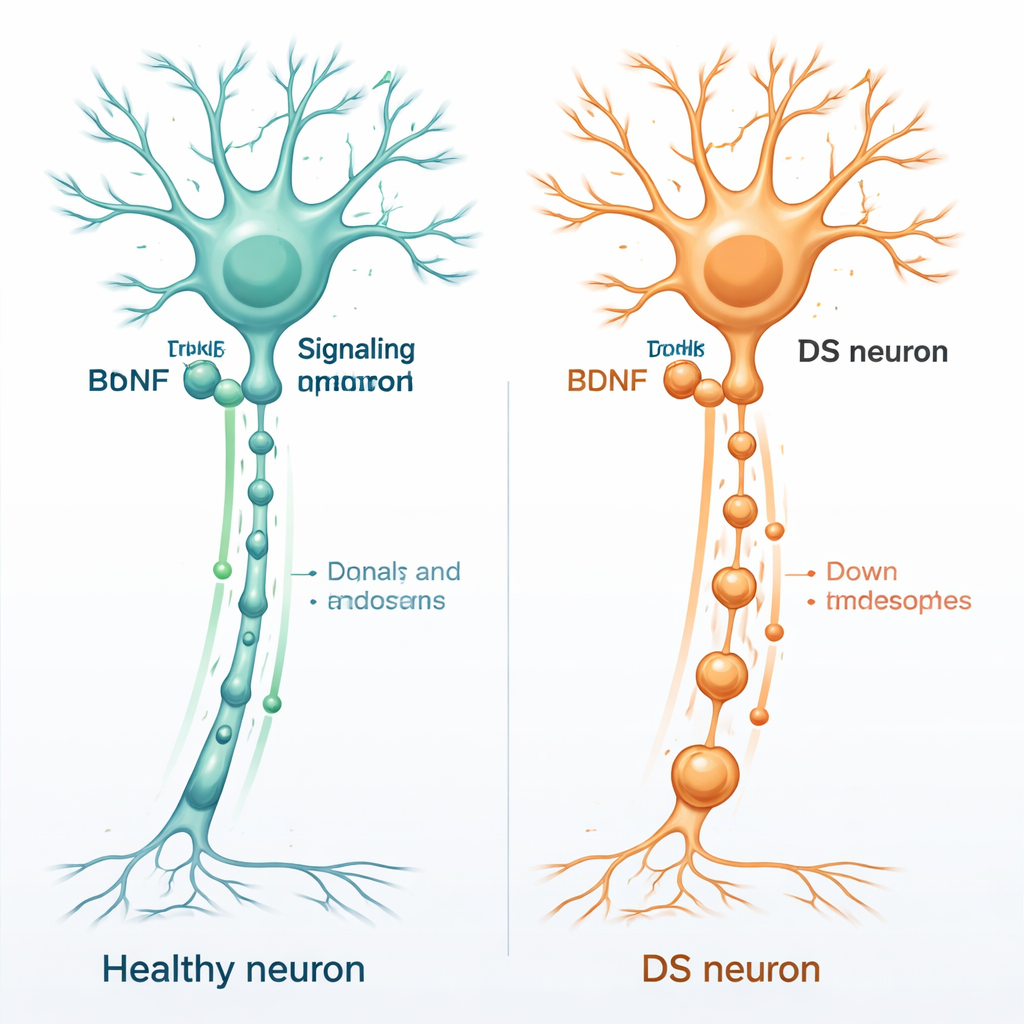
Nawóz mózgowy i kondycja komórek nerwowych
Zdrowe komórki mózgowe polegają na grupie cząsteczek wsparcia zwanych neurotrofinami, które działają jak nawóz dla neuronów. Jedną z najważniejszych jest pochodny mózgowy czynnik neurotroficzny, czyli BDNF. BDNF wiąże się z białkiem dokującym na neuronach o nazwie TrkB, zwykle na dalekich końcach włókien nerwowych. Gdy BDNF się przyłączy, cały kompleks BDNF–TrkB zostaje wciągnięty do małych pęcherzyków błonowych i transportowany z powrotem wzdłuż długiego włókna nerwowego do ciała komórki. Te poruszające się pęcherzyki, znane jako endosomy sygnalizacyjne, informują jądro, które geny włączyć, aby utrzymać neuron przy życiu, połączonym i plastycznym.
Kiedy komórki pakunkowe stają się za duże
Zespół skupił się na neuronach istoty podstawnej mózgu, grupie komórek silnie wspierającej pamięć i uwagę, które należą do pierwszych, które degenerują w zespole Downa i chorobie Alzheimera. Korzystając z modelu mysiego zespołu Downa o nazwie Dp1Tyb, barwili neurony markerem wczesnych endosomów i porównywali je z neuronami normalnymi. Neurony z zespołem Downa zawierały znacznie więcej wczesnych endosomów, z których ponad 50 procent było powiększonych w porównaniu z normą. Strukturami tymi zarządza Rab5, molekularny przełącznik pomagający tworzyć i sortować te wewnętrzne „kontenery wysyłkowe”. Badacze stwierdzili, że Rab5 był zatrzymany w nadaktywowanym stanie w neuronach z zespołem Downa, jeszcze przed stymulacją BDNF, co sugeruje, że system endosomalny był już nadmiernie pobudzony.
Zatory ruchu wzdłuż włókna nerwowego
Następnie naukowcy sprawdzili, czy ta zniekształcona wewnętrzna architektura zakłóca ruch sygnałów BDNF. Hodowali neurony w urządzeniach mikroprzepływowych, które oddzielają ciała komórek od ich zakończeń aksonalnych, umożliwiając stymulację jedynie końcówek aksonów. Podążając za nieszkodliwymi fluorescencyjnymi znacznikami, które korzystają z tej samej trasy transportowej co kompleksy BDNF–TrkB, mierzyli, jak szybko endosomy sygnalizacyjne poruszały się z powrotem w kierunku ciał komórek. W neuronach prawidłowych dodanie BDNF przyspieszało endosomy o około 30 procent i zmniejszało częstość zatrzymań, co odzwierciedlało silną odpowiedź na sygnały wzrostu. W neuronach z zespołem Downa jednak BDNF nie przyspieszało transportu ani nie zmniejszało pauz. Osobny eksperyment śledzący rzeczywiste receptory TrkB potwierdził, że mniej z nich docierało skutecznie do ciała komórki w neuronach z zespołem Downa.
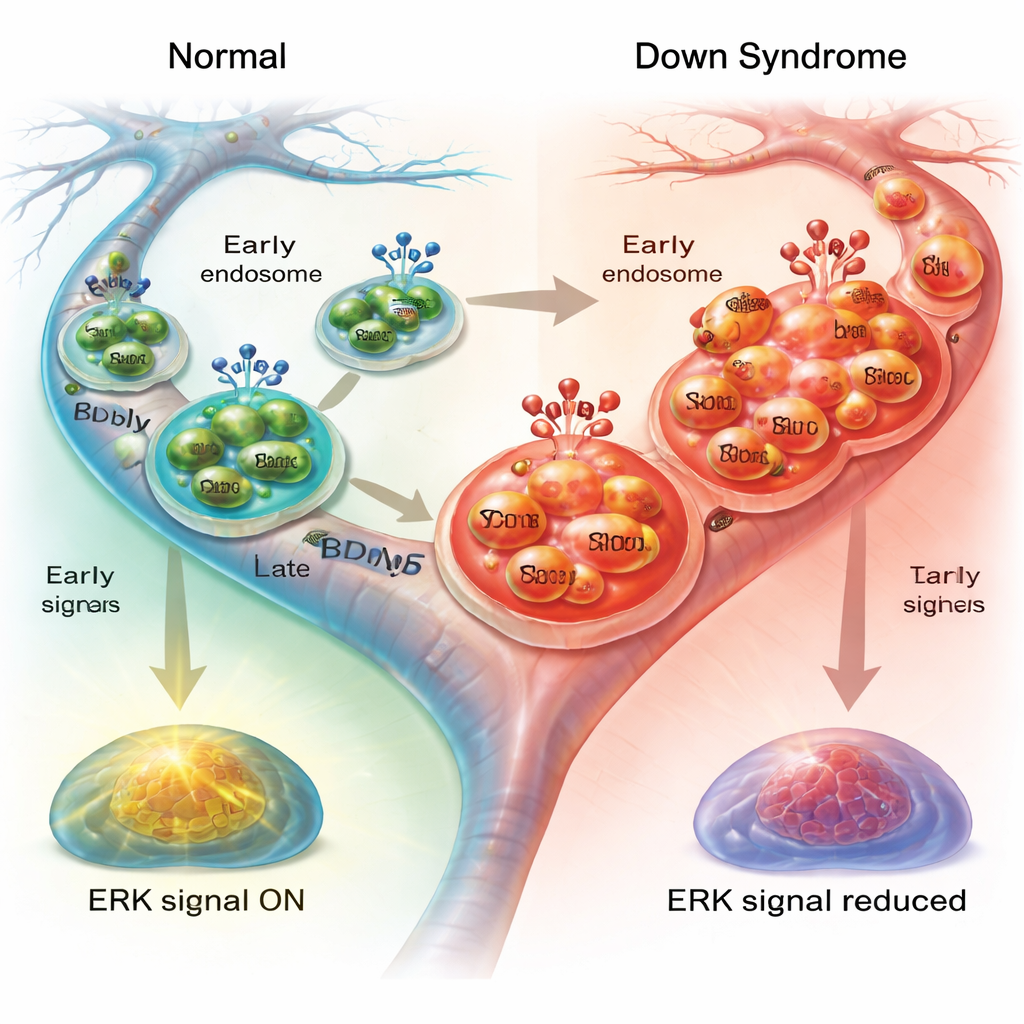
Stłumione sygnały wewnątrz komórki
Aby te podróżujące pęcherzyki wspierały zdrowie neuronu, muszą aktywować wewnętrzne szlaki sygnałowe po dotarciu do celu. Jedną z kluczowych dróg jest ERK1/2, para enzymów przekazujących wiadomość BDNF do jądra i pomagających regulować cytoszkielet oraz mechanizmy transportowe komórki. Gdy badacze zmierzyli aktywowany ERK1/2 po podaniu BDNF, zaobserwowali wyraźny wzrost w neuronach prawidłowych, ale znacznie słabszą odpowiedź w neuronach z zespołem Downa, szczególnie w aksonach. Zablokowanie ERK1/2 w zdrowych neuronach częściowo odtworzyło powolny transport obserwowany w komórkach z zespołem Downa, spowalniając endosomy i zwiększając liczbę pauz. W przeciwieństwie do tego, blokada ERK1/2 miała niewielki dodatkowy efekt w neuronach z zespołem Downa, co jest zgodne z sygnalizacją już osłabioną.
Co to oznacza dla starzenia się mózgu w zespole Downa
Podsumowując, wyniki sugerują samo-wzmacniający się problem w wrażliwych neuronach: Rab5 jest nadaktywny, wczesne endosomy pęcznieją, a kompleksy BDNF–TrkB zostają uwięzione w przedziałach, które nie przemieszczają się efektywnie. W rezultacie mniej sygnałów wzrostu dociera do ciała komórki, sygnalizacja ERK1/2 jest osłabiona, a mechanizmy napędzające transport na duże odległości są dodatkowo upośledzone. Z biegiem lat ten wadliwy system komunikacji może przyczyniać się do wczesnej i ciężkiej utraty neuronów istoty podstawnej obserwowanej u osób z chorobą Alzheimera związaną z zespołem Downa. Podkreślając powiązanie między „ruchem drogowym” endosomów a sygnalizacją czynników wzrostu, badanie wskazuje nowe pomysły terapeutyczne, których celem jest normalizacja aktywności Rab5, przywrócenie funkcji endosomów i wzmocnienie reakcji na BDNF, aby chronić te kluczowe neurony.
Cytowanie: Blackburn, E., Birsa, N., Lopes, A.T. et al. Impaired BDNF-TrkB trafficking and signalling in Down syndrome basal forebrain neurons. Cell Death Dis 17, 214 (2026). https://doi.org/10.1038/s41419-026-08464-z
Słowa kluczowe: Zespół Downa, Choroba Alzheimera, BDNF, transport aksonalny, endosomy