Clear Sky Science · pl
Sygnalizacja IRE1 w śródbłonku utrzymuje integralność bariery krew–mózg i ogranicza neurozapaleniem po urazie czaszkowo-mózgowym
Dlaczego ochron a wewnętrznej ściany mózgu ma znaczenie
Po uderzeniu w głowę bezpośrednie uszkodzenie to tylko część historii. W godzinach i dniach po urazie mózg uruchamia silną odpowiedź stresową i immunologiczną, która może potajemnie pogłębiać obrażenia. W tym badaniu zbadano, jak niewielki system wykrywający stres wewnątrz komórek wyściełających naczynia mózgowe pomaga utrzymać szczelność i spokój wewnętrznej ściany mózgu — bariery krew–mózg — po urazie czaszkowo-mózgowym. Zrozumienie tej ukrytej obrony może wskazać nowe terapie ograniczające trwałą niepełnosprawność po urazie głowy.
Stróże mózgu pod wpływem stresu
Mózg polega na wyspecjalizowanej barierze tworzonej przez komórki śródbłonka, które wyściełają wnętrze naczyń krwionośnych i ściśle kontrolują, co może przeniknąć z krwi do tkanki mózgowej. Uraz czaszkowo-mózgowy (TBI) może zaburzyć tę barierę krew–mózg, pozwalając na napływ cząsteczek zapalnych i komórek odpornościowych, co pogarsza uszkodzenia. W tych komórkach śródbłonka działa system kontroli jakości zwany odpowiedzią na nieprawidłowo złożone białka ( unfolded protein response), który pomaga komórkom radzić sobie ze stresem w strukturze zwanej retikulum endoplazmatycznym. Jednym z jego kluczowych elementów jest IRE1, działający jak sensor i regulator, gdy komórki są pod presją. Naukowcy postawili pytanie: czy ten czujnik stresu w śródbłonku pomaga bronić bariery po TBI, czy też pogarsza sytuację?
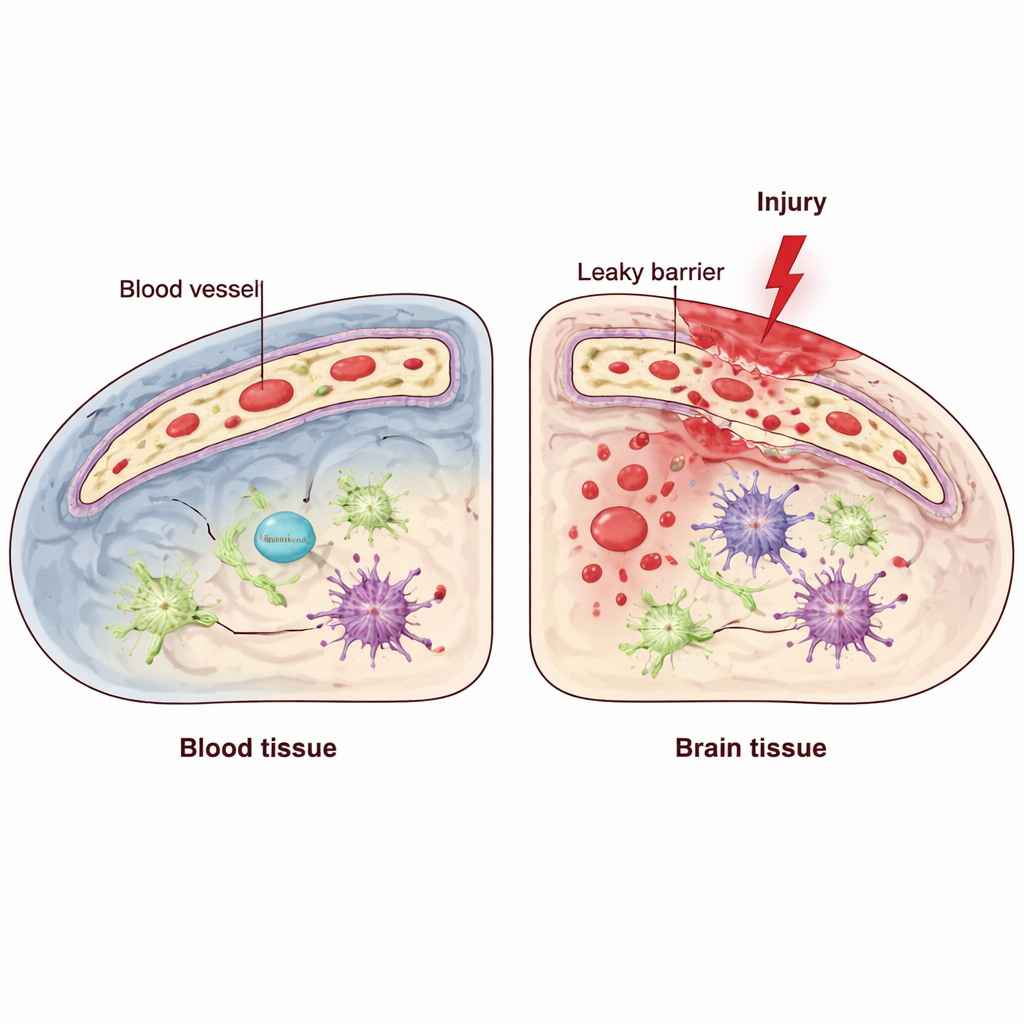
Wyłączanie czujnika komórkowego w komórkach naczyniowych
Aby to sprawdzić, zespół użył genetycznie zmodyfikowanych myszy, w których IRE1 można było selektywnie wyłączyć tylko w komórkach śródbłonka. Następnie wywołali kontrolowane uszkodzenie w obszarze ruchowym kory, naśladując aspekty ludzkiego TBI, i porównali te myszy z normalnymi miotami rodzeństwa. Testowali ruch za pomocą zadań mierzących równowagę i precyzyjne ustawianie łap oraz badali tkankę mózgową za pomocą mikroskopii wysokiej rozdzielczości i technik molekularnych. U normalnych myszy aktywność IRE1 wzrastała w komórkach naczyń krwionośnych w pobliżu urazu wkrótce po traumie, co sugeruje, że komórki śródbłonka szybko wykrywają i reagują na stres. Gdy IRE1 brakowało specyficznie w tych komórkach, zwierzęta wypadły gorzej w testach motorycznych, co wskazuje na gorszą rekonwalescencję funkcjonalną.
Przeciekanie naczyń, więcej komórek odpornościowych i obumierające neurony
Następnie badacze sprawdzili, jak dobrze utrzymywała się bariera krew–mózg. Zwykle duże białka krwi, takie jak przeciwciała, pozostają wewnątrz naczyń. Po TBI oczekuje się pewnego przecieku w pobliżu ogniska, ale myszy pozbawione śródbłonkowego IRE1 wykazywały znacznie bardziej rozległe przenikanie tych białek do mózgu. Mikroskopia ujawniła, że kluczowy białkowy element złączy, VE-kadheryna, który pomaga uszczelniać komórki śródbłonka, był zmniejszony w obszarze urazu, gdy brakowało IRE1, mimo że ogólna liczba naczyń wyglądała podobnie. To przeciekanie towarzyszyło napływowi komórek odpornościowych do mózgu wokół ogniska i wyższym poziomom sygnałów zapalnych. W tych samych regionach neurony częściej wykazywały oznaki degeneracji i programowanej śmierci komórkowej, a strefa uszkodzonej tkanki otaczającej rdzeń urazu była wyraźnie większa.
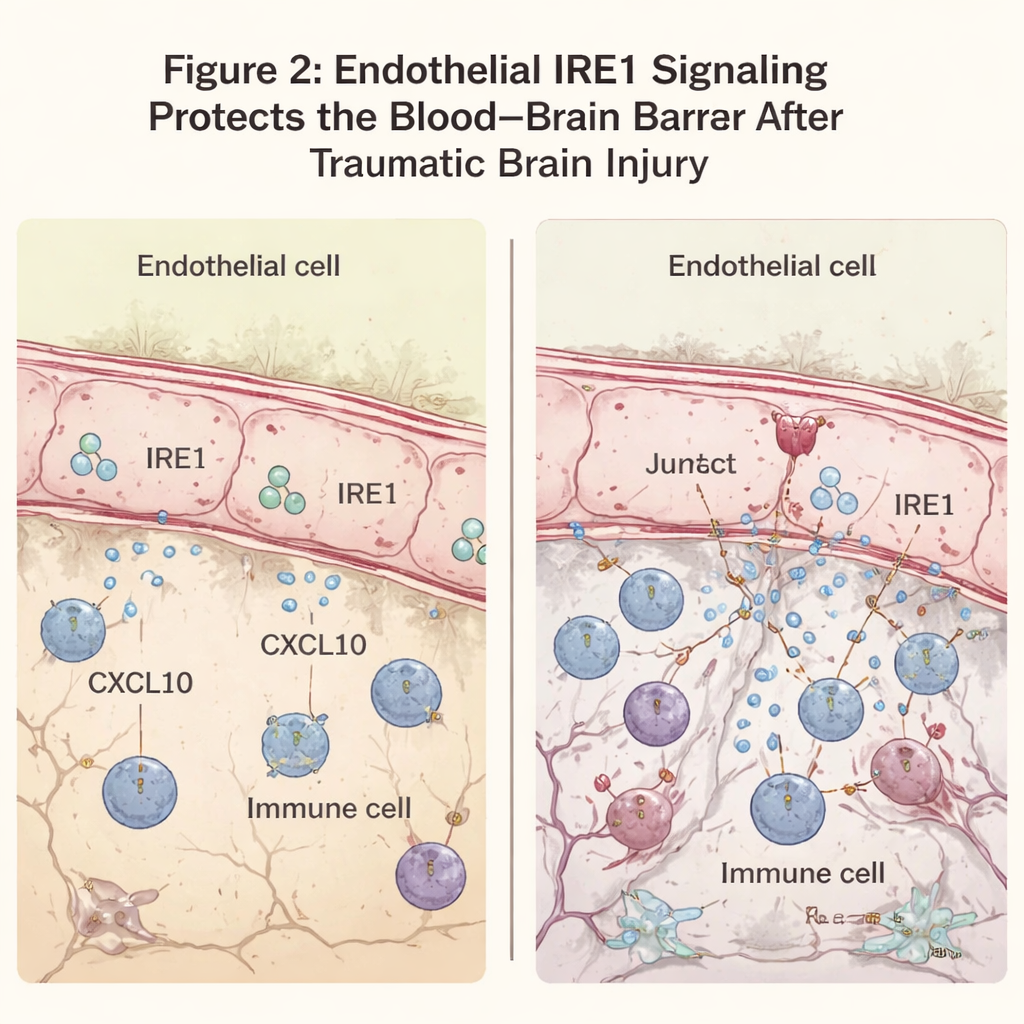
Lek przeciwstresowy łagodzi burzę sygnałów
Aby zrozumieć molekularne podstawy, zespół przeanalizował geny aktywowane po urazie. U myszy bez śródbłonkowego IRE1 geny związane z odpowiedzią przeciwwirusową i zapalną były silnie zwiększone. Wyróżniał się wśród nich CXCL10, chemokina — rodzaj molekularnego sygnału przyciągającego komórki odpornościowe, która może dodatkowo osłabić barierę. CXCL10 była szczególnie podwyższona w komórkach śródbłonka w pobliżu ogniska, gdy brakowało IRE1. W hodowanych komórkach śródbłonka mózgu wystawionych na czynnik zapalny zmniejszenie stresu retikulum endoplazmatycznego za pomocą leku TUDCA obniżyło zarówno aktywność IRE1, jak i produkcję CXCL10. Podanie TUDCA uszkodzonym myszom zmniejszyło CXCL10 i markery komórek odpornościowych w uszkodzonej korze oraz poprawiło wyniki motoryczne, co sugeruje, że stłumienie tej ścieżki stresowej może złagodzić wtórne uszkodzenia.
Co to oznacza dla osób po urazie głowy
Mówiąc prosto, praca ta sugeruje, że sensor stresu IRE1 w komórkach wyściełających naczynia mózgowe działa jako strażnik po urazie czaszkowo-mózgowym. Gdy jest obecny i funkcjonuje, pomaga utrzymać szczelność bariery krew–mózg, ogranicza uwalnianie chemicznych sygnałów przyciągających komórki odpornościowe i powstrzymuje rozprzestrzenianie się zapalenia oraz utratę neuronów wokół ogniska. Gdy jest wyłączony, bariera staje się bardziej nieszczelna, komórki odpornościowe napływają, a więcej tkanki mózgowej ulega uszkodzeniu. Ponieważ komórki naczyń są stosunkowo dostępne dla leków krążących we krwi, ukierunkowanie ich odpowiedzi na stres — za pomocą związków takich jak TUDCA lub dokładniejszych terapii w przyszłości — może stać się praktyczną strategią zmniejszania długoterminowych szkód po urazie głowy.
Cytowanie: Fan, Q., Takarada-Iemata, M., Tanaka, T. et al. Endothelial IRE1 signaling maintains blood–brain barrier integrity and limits neuroinflammation after traumatic brain injury. Cell Death Dis 17, 210 (2026). https://doi.org/10.1038/s41419-026-08461-2
Słowa kluczowe: uraz czaszkowo-mózgowy, bariera krew–mózg, komórki śródbłonka, neurozapalenie, stres komórkowy