Clear Sky Science · pl
CD36 zwiększa wrażliwość komórek potrójnie ujemnego raka piersi na ferroptozę indukowaną palmitynianem
Dlaczego tłuszcz wokół guzów może być i sprzymierzeńcem, i wrogiem
Guzy piersi rozwijają się w tkance naturalnie bogatej w tłuszcz, a komórki nowotworowe znane są z „odżywiania się” pobliskimi kwasami tłuszczowymi. W tym badaniu naukowcy opisują zaskakujący zwrot akcji: przy odpowiednich warunkach jeden z najpowszechniejszych tłuszczów w organizmie, kwas palmitynowy, może w rzeczywistości pomagać w zabijaniu szczególnie agresywnej postaci raka piersi, wywołując specyficzny rodzaj śmierci komórki. Zrozumienie tego mechanizmu może wskazać nowe możliwości leczenia dla pacjentów, którzy obecnie mają niewiele opcji.
Trudny do leczenia rak piersi pod mikroskopem
Potrójnie ujemny rak piersi (TNBC) nie ma receptorów dla hormonów i czynników wzrostu, które są celem wielu współczesnych leków, co czyni go jednym z najtrudniejszych typów raka piersi w leczeniu. Guzy te żyją w bliskim kontakcie z komórkami tłuszczowymi, które uwalniają duże ilości kwasów tłuszczowych, w tym nasyconego kwasu palmitynowego. Naukowcy chcieli sprawdzić, czy kwas palmitynowy jedynie napędza wzrost guza, czy też może tworzyć słaby punkt, który da się wykorzystać do zabijania komórek nowotworowych.
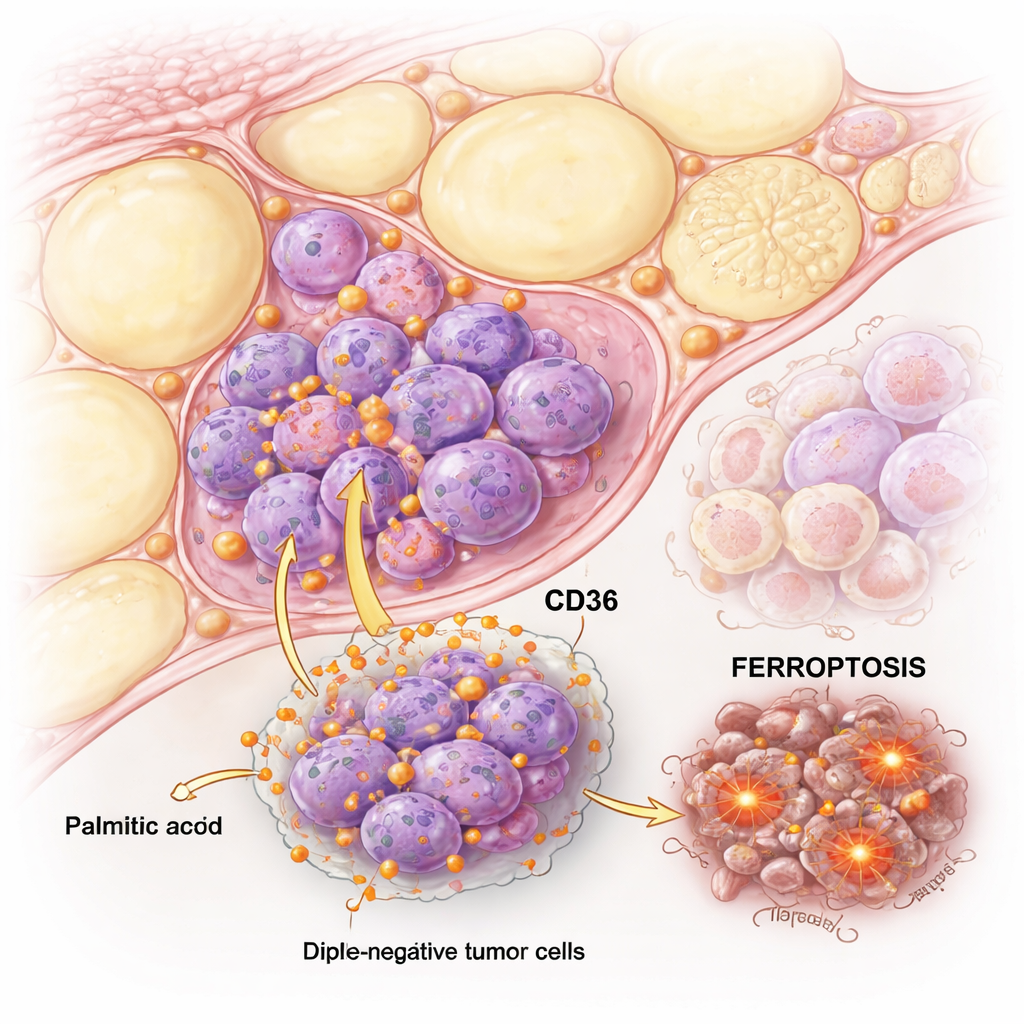
Kiedy kwas palmitynowy doprowadza komórki nowotworowe do krawędzi
Zespół porównał komórki TNBC z hormonowrażliwymi komórkami „luminalnymi” raka piersi i wystawił je na rosnące stężenia kwasu palmitynowego. Oba rodzaje komórek mogły zostać uszkodzone przez wysokie dawki, ale komórki TNBC okazały się znacznie bardziej wrażliwe. Szczegółowe testy wykazały, że w komórkach luminalnych kwas palmitynowy głównie wywoływał klasyczną apoptozę, porządną formę śmierci komórkowej. W komórkach TNBC jednak kwas palmitynowy uruchamiał zarówno apoptozę, jak i mniej znaną drogę zwaną ferroptozą, zależną od żelaza i niszczenia lipidów błon komórkowych.
Drzwi dla kwasów tłuszczowych o nazwie CD36
Aby zrozumieć, dlaczego komórki TNBC reagowały tak odmiennie, badacze skupili się na CD36, białku na powierzchni komórki, które działa jak bramka dla długołańcuchowych kwasów tłuszczowych. Komórki TNBC naturalnie miały znacznie więcej CD36 niż komórki luminalne, a ekspozycja na kwas palmitynowy dodatkowo podnosiła poziom CD36. Oznaczało to, że komórki TNBC pobierały więcej kwasu palmitynowego, gromadziły więcej uszkodzonych lipidów, wytwarzały więcej reaktywnych form tlenu w mitochondriach i kumulowały więcej wolnego żelaza wewnątrz komórki — wszystkie te sygnały są kluczowe dla ferroptozy. Gdy CD36 zostało zablokowane za pomocą leku lub zmniejszone przy pomocy narzędzi genetycznych, ferroptoza indukowana kwasem palmitynowym istotnie spadała.
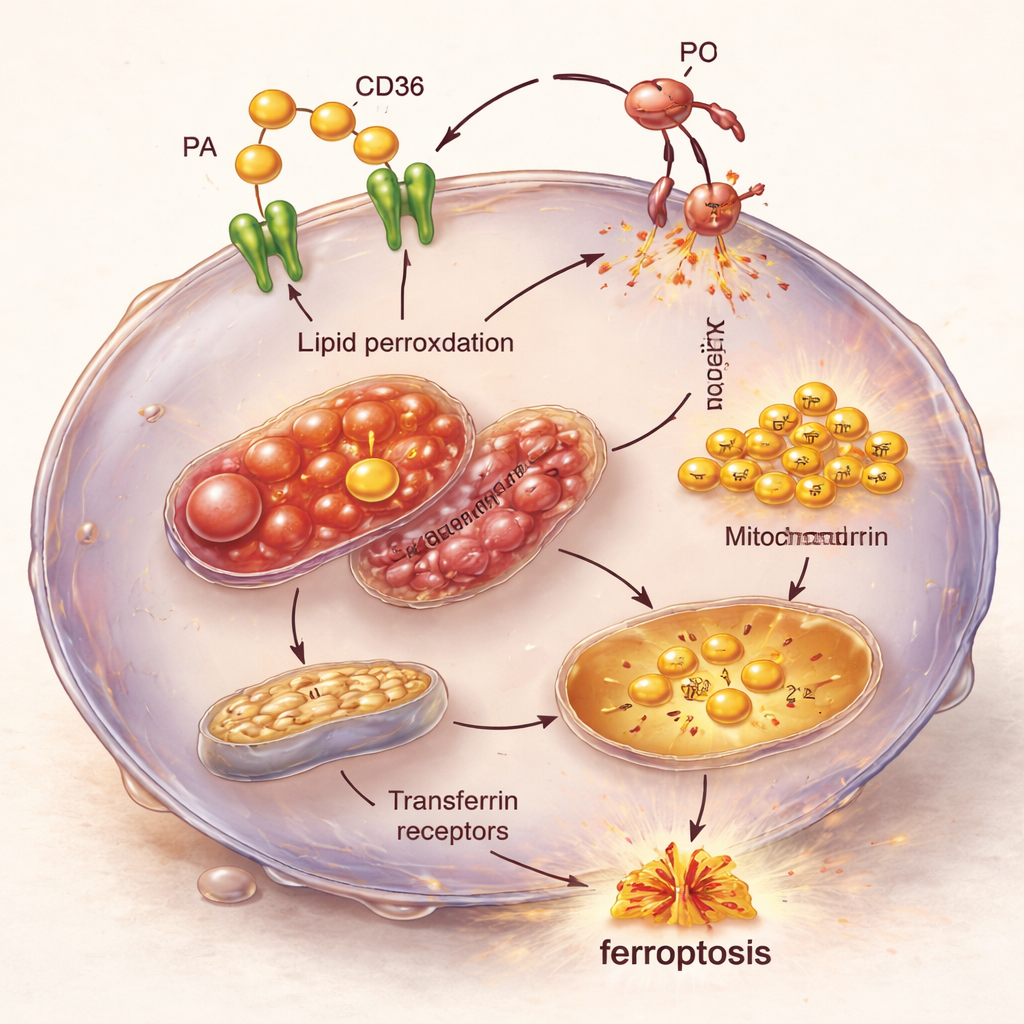
Przybliżenie reakcji łańcuchowej wewnątrz komórki
Mikroskopia i analizy aktywności genów ujawniły wewnętrzną reakcję łańcuchową stojącą za tą podatnością. Komórki TNBC przeładowane kwasem palmitynowym i CD36 wykazywały napęczniałe, strukturalnie uszkodzone mitochondria oraz rosnące poziomy żelaza dostarczanego przez receptory transferryny. Jednocześnie włączane były geny sprzyjające ferroptozie, podczas gdy geny zwykle chroniące przed tym rodzajem śmierci komórkowej były wyciszane. W efekcie powstaje idealna burza: nadmiar napływającego tłuszczu, więcej żelaza dostępnego do podtrzymywania reakcji chemicznych oraz osłabione mechanizmy obronne przeciwko uszkodzeniom lipidów — wszystko to razem popycha komórki TNBC w kierunku ferroptozy.
Którzy pacjenci mogą skorzystać najbardziej?
Nowotwór nie jest jednorodny, nawet w obrębie TNBC. Na podstawie próbek guzów hodowanych u myszy oraz dużych baz danych pacjentów autorzy stwierdzili, że CD36 był szczególnie wysoki w określonym podtypie TNBC zwanym luminal androgen receptor (LAR), który wcześniej zauważono jako bardziej wrażliwy na ferroptozę. Inne podtypy TNBC o wysokim poborze żelaza także miały zazwyczaj wyższe poziomy CD36. Ten wzorzec sugeruje, że CD36 mógłby służyć jako marker identyfikujący pacjentów, których guzy są naturalnie predysponowane do terapii opartych na ferroptozie.
Przekształcenie powszechnego tłuszczu w sojusznika terapeutycznego
Mówiąc prosto, praca ta pokazuje, że obfity tłuszcz dietetyczny i tkankowy — kwas palmitynowy — może pomóc zniszczyć niektóre komórki potrójnie ujemnego raka piersi, gdy wykazują one wysokie poziomy transportera tłuszczu CD36. Poprzez wywoływanie przeciążenia tłuszczem, kumulacji żelaza i uszkodzeń błon komórkowych, CD36 zwiększa prawdopodobieństwo, że te komórki nowotworowe ulegną ferroptozie — destrukcyjnej drodze, której nie potrafią uniknąć. Jeśli przyszłe terapie będą mogły bezpiecznie wzmacniać tę ścieżkę — lub łączyć ją z lekami, które dodatkowo osłabiają obronę komórek — klinicyści mogą zamienić tę metaboliczną słabość w nowy, bardziej precyzyjny sposób atakowania jednych z najbardziej agresywnych guzów piersi.
Cytowanie: Closset, L., Foy, JP., Louadj, L. et al. CD36 enhances sensitivity of triple negative breast cancer cells to palmitate-induced ferroptosis. Cell Death Dis 17, 219 (2026). https://doi.org/10.1038/s41419-026-08460-3
Słowa kluczowe: potrójnie ujemny rak piersi, ferroptoza, CD36, kwas palmitynowy, metabolizm guza