Clear Sky Science · pl
Deubikwitynacja heksokinazy 2 przez USP30 kontroluje metaboliczne przeznaczenie glukozy i rozwój nowotworu
Jak komórki nowotworowe przekalibrowują użycie cukru
Komórki nowotworowe słyną ze swojego „słodkiego zęba”: spalają cukier w nietypowy sposób, aby zasilić szybki wzrost. W tym badaniu odkryto nowy przełącznik — białko o nazwie USP30 — które pomaga komórkom nowotworowym decydować, jak wykorzystać glukozę. Poprzez precyzyjne modulowanie innego białka, heksokinazy 2 (HK2), USP30 może skłonić komórki nowotworowe do intensywniejszego spalania cukru i szybszego wzrostu, wskazując nowy cel dla przyszłych leków przeciwnowotworowych. 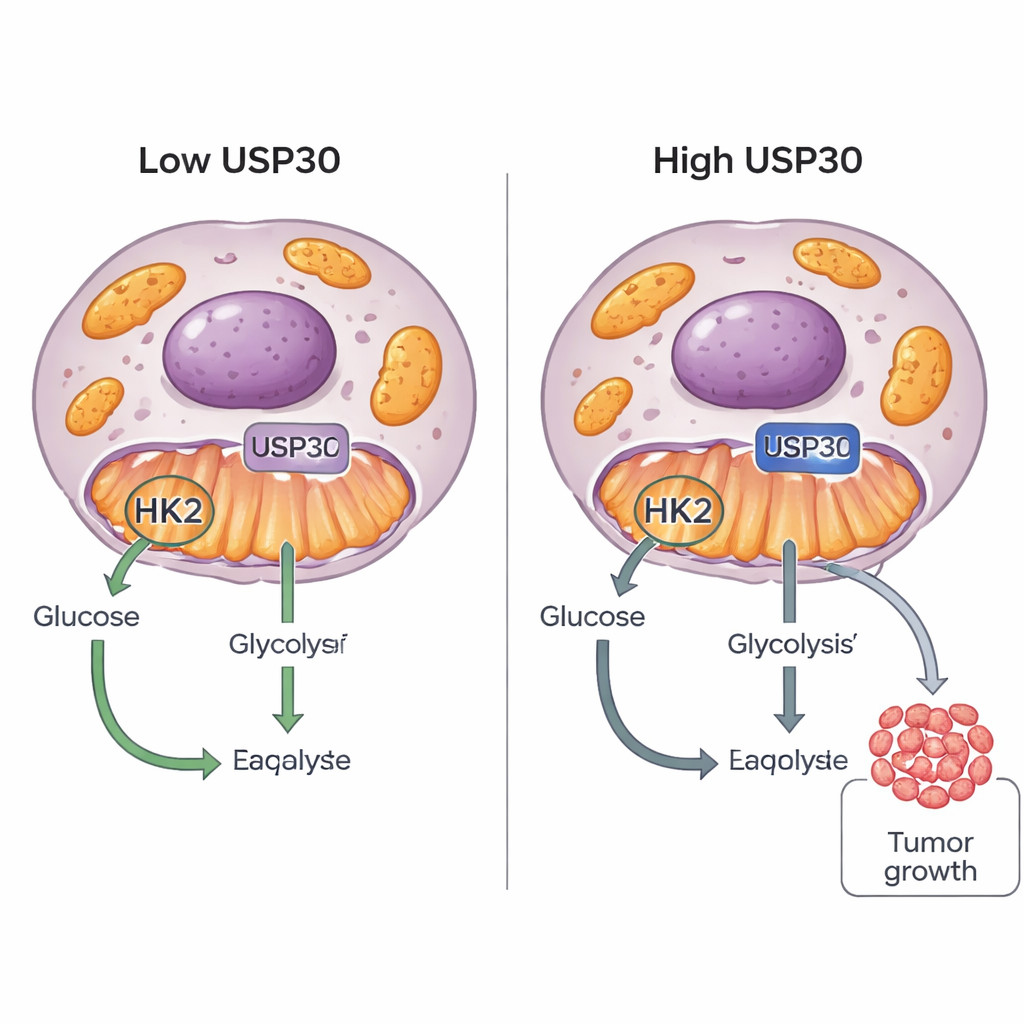
Słodkożerna strategia wewnątrz guzów
Większość zdrowych komórek wydobywa energię z substancji odżywczych wydajnie, ale wiele komórek nowotworowych preferuje szybki i prosty tor zwany glikolizą tlenową, znaną też jako efekt Warburga. Pobierają duże ilości glukozy i szybko przekształcają ją w mleczan, nawet gdy tlen jest dostępny. Ta strategia robi więcej niż tylko wytwarzanie energii: dostarcza składników budulcowych do syntezy DNA, lipidów i białek, pomaga guzom przetrwać stres i może osłabiać ataki układu odpornościowego. Na wejściu do tej ścieżki stoi heksokinaza — enzym, który przyłącza grupę fosforanową do napływającej glukozy, zobowiązując ją do dalszego rozkładu i reakcji wspierających wzrost.
Enzym mitochondrialny w świetle reflektorów
USP30 to enzym umieszczony na zewnętrznej powierzchni mitochondriów, elektrowni komórki. Należy do rodziny deubikwitynaz, które usuwają maleńkie znaczniki białkowe zwane ubikwityną z innych białek, często zmieniając ich stabilność, lokalizację lub aktywność. O USP30 wiadomo było wcześniej w kontekście komórek nerwowych i kontroli jakości mitochondriów, ale jego wpływ na nowotwory był niejasny. Analiza dużych baz danych genów nowotworowych wykazała, że guzy z wyższym poziomem USP30 częściej wykazywały sygnatury silniejszego spalania glukozy i słabszego spalania tłuszczów, co sugeruje, że USP30 może pomagać nowotworom przełączać się na metabolizm oparty na cukrze.
Łączenie USP30 z metabolicznymi strażnikami glukozy
Aby zbadać to powiązanie, zespół obniżył lub usunął USP30 w kilku liniach komórek nowotworowych i zmierzył, jak przetwarzają energię. Korzystając z urządzeń śledzących produkcję kwasu i zużycie tlenu w czasie rzeczywistym, stwierdzono, że utrata USP30 gwałtownie zmniejsza zarówno glikolizę, jak i oddychanie mitochondrialne. Produkcja mleczanu i zużycie glukozy spadły, pokazując, że „silnik” spalania cukru w komórkach zwolnił. Zestaw eksperymentów z użyciem spektrometrii mas wykazał następnie, że USP30 fizycznie wchodzi w interakcje z kilkoma enzymami powiązanymi z metabolizmem glukozy, szczególnie z heksokinazami HK1 i HK2. Testy uzupełniające pokazały, że ta interakcja zależy od aktywności katalitycznej USP30 i zachodzi bezpośrednio, a nie tylko poprzez pośredników.
Precyzyjny biologiczny uchwyt na heksokinazę 2
Wnikliwsze badania wykazały, że USP30 usuwa specyficzne rodzaje łańcuchów ubikwityny — tzw. nietypowe wiązania — z HK1 i HK2. W przypadku HK2 edycja ta zachodzi na pojedynczym istotnym aminokwasie, lizynie 144 (K144). Gdy K144 jest zmieniona tak, że nie może już przenosić ubikwityny, HK2 staje się bardziej stabilna, silniej wiąże się z kanałowym białkiem VDAC1 na mitochondriach i wykazuje wyższą aktywność enzymatyczną. Komórki zaprojektowane tak, aby nosić tę mutację K144, kierowały więcej HK2 do mitochondriów, paliły więcej glukozy, wydzielały więcej mleczanu i wykazywały szybszy wzrost oraz ruch w hodowlach. U myszy guzy pochodzące z komórek z mutacją K144 HK2 rosły większe i szybciej niż guzy z normalną HK2, podkreślając znaczenie tego drobnego molekularnego przełącznika. 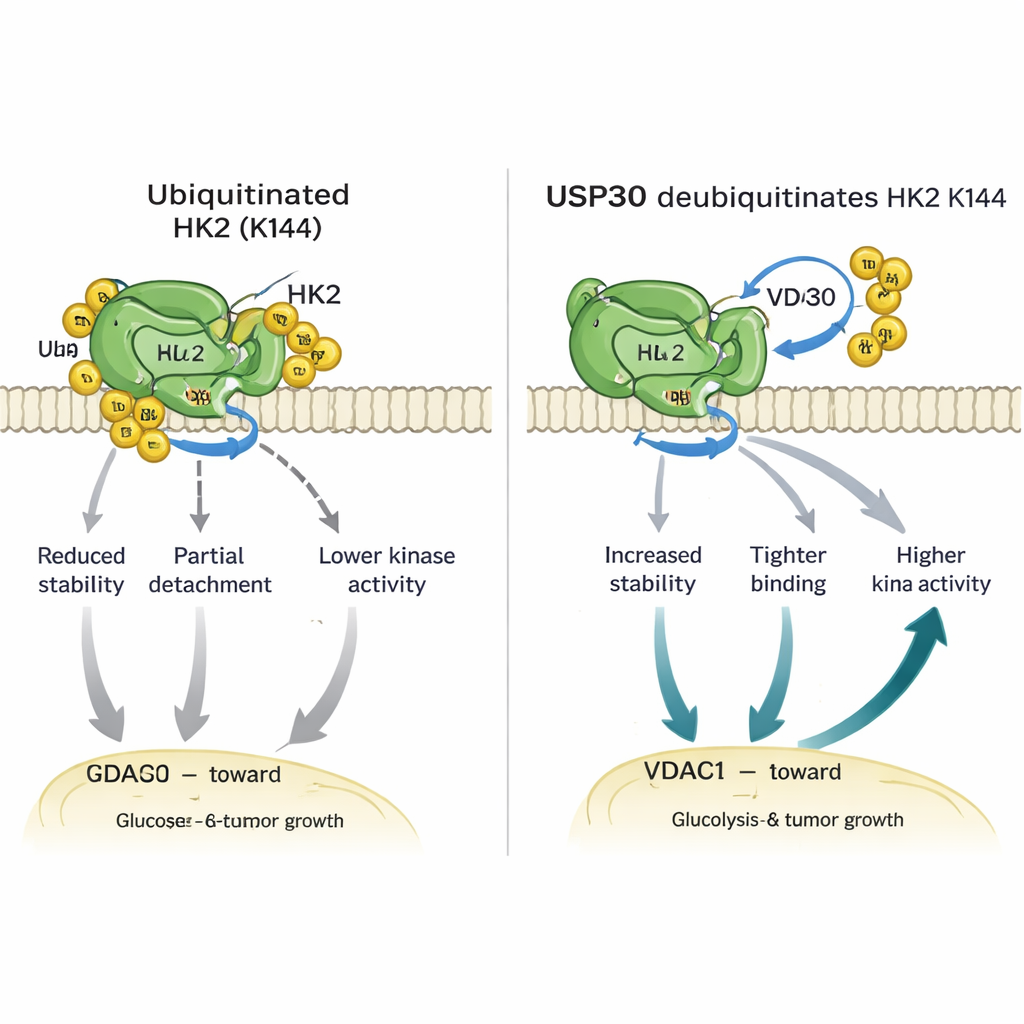
Zamiana przełącznika metabolicznego w przewagę wzrostową
Wyniki mapują jasny łańcuch zdarzeń: USP30 wiąże się z HK2, zdejmuje znaczniki ubikwityny z K144 i w ten sposób utrzymuje HK2 aktywną i zakotwiczoną na mitochondriach. To zwiększa glikolizę, zasila podziały i migrację komórek nowotworowych i ostatecznie przyspiesza wzrost guza. Gdy USP30 jest nieobecny lub nieaktywny, HK2 staje się mniej stabilna i mniej wydajna, a komórki nowotworowe tracą część swojej metabolicznej przewagi. Z perspektywy laika USP30 działa jak mechanik utrzymujący „silnik cukrowy” komórki nowotworowej w sprawności — usuń mechanika, a silnik zaczyna zaciągać.
Co to oznacza dla przyszłych terapii przeciwnowotworowych
Dla osoby niebędącej specjalistą kluczowe przesłanie jest takie, że komórki nowotworowe polegają na precyzyjnym sterowaniu sposobem spalania cukru, a USP30 jest nowo odkrytym pokrętłem na tym panelu kontroli. Stabilizując HK2 w jednym konkretnym miejscu, USP30 pomaga guzom utrzymywać metabolizm żarłoczny względem glukozy i rosnąć bardziej agresywnie. Leki blokujące USP30 lub zakłócające jego uchwyt na HK2 przy lizynie 144 mogłyby osłabić guzy przez „zagłodzenie” ich silnika cukrowego, niekoniecznie szkodząc w takim samym stopniu komórkom normalnym. Ta praca więc dodaje istotne ogniwo do układanki, jaką jest przeprogramowywanie metabolizmu w nowotworach, i sugeruje obiecujący nowy kierunek dla terapii celowanych.
Cytowanie: Haowei, Z., Li, X., Liao, W. et al. USP30-mediated Deubiquitination of Hexokinase 2 controls the metabolic fate of glucose and tumor progression. Cell Death Dis 17, 225 (2026). https://doi.org/10.1038/s41419-026-08459-w
Słowa kluczowe: metabolizm nowotworów, glikoliza, heksokinaza 2, USP30, efekt Warburga