Clear Sky Science · pl
Stabilizacja SERPINB5 zależna od m5C sprzyja postępowi raka szyjki macicy i oporności na chemioterapię
Dlaczego to badanie ma znaczenie dla pacjentek
Rak szyjki macicy wciąż stanowi śmiertelne zagrożenie dla wielu kobiet na świecie, zwłaszcza gdy przestaje odpowiadać na standardowe leki chemioterapeutyczne, takie jak paklitaksel i winkrystyna. W tym badaniu odkryto ukrytą drogę molekularną w komórkach raka szyjki macicy, która pomaga im rosnąć, przerzucać się i unikać działania powszechnie stosowanych terapii. Ujawnienie tej ścieżki wskazuje nowe sposoby, w jaki lekarze mogliby przewidywać, które guzy będą oporne na leczenie, oraz jak zaprojektować leki przywracające wrażliwość.
Chemiczna etykieta na RNA, która napędza nowotwór
Większość osób zna DNA jako nośnik informacji genetycznej, ale komórki polegają też na RNA jako roboczej kopii instrukcji genetycznych. Autorzy skupili się na małej chemicznej etykiecie na RNA zwanej 5-metyloocytozyną (m5C). Dzięki mapowaniu o wysokiej rozdzielczości w próbkach od pacjentek stwierdzili, że nowotwory szyjki macicy mają znacznie więcej znaków m5C na RNA niż prawidłowa tkanka szyjki. Znaki te były szczególnie częste w odcinkach RNA kodujących białka i miały tendencję do występowania w genach związanych z wzrostem komórek, inwazją oraz zdolnością komórek nowotworowych do unikania układu odpornościowego. Ten wzór sugeruje, że komórki nowotworowe przeprogramowują chemię RNA, by wzmocnić programy napędzające złośliwość.
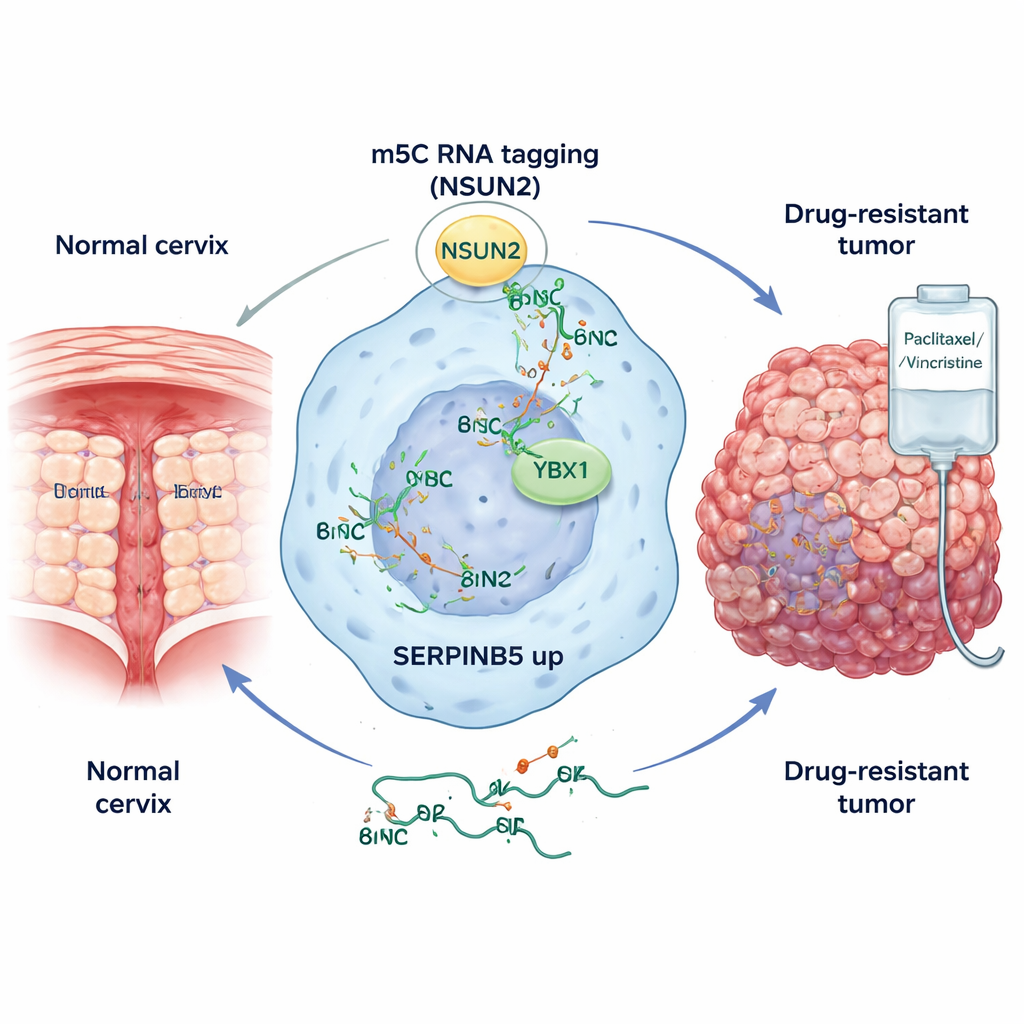
Wyróżnienie kluczowego sprawcy: SERPINB5
Aby ustalić, które m5C-znakowane RNA mają rzeczywisty wpływ na zachowanie nowotworu, zespół połączył kilka zaawansowanych metod: sekwencjonowanie RNA z próbek zbiorczych, transkryptomikę przestrzenną pokazującą, gdzie geny są aktywne w przekroju guza, oraz sekwencjonowanie pojedynczych komórek. Następnie zbudowali niestandardowy model komputerowy MORGAN do priorytetyzacji kandydatów — genów, których aktywność rośnie wraz z obecnością m5C. Spośród kilku genów powiązanych z rakiem wyróżnił się jeden: SERPINB5, zwany też maspiną. W guzach szyjki macicy SERPINB5 był silnie eksprymowany w wyodrębnionej populacji komórek nowotworowych, rzadko obserwowanej w tkance prawidłowej. Komórki pozytywne dla SERPINB5 skupiały się w obszarach guza bogatych w szybko dzielące się komórki i wykazywały sygnatury genowe związane z replikacją DNA, zmianami kształtu komórek oraz zdolnością do przebudowy otaczającej tkanki.
Jak obwód metylacji stabilizuje SERPINB5
Naukowcy zapytali potem, w jaki sposób SERPINB5 staje się tak obficie obecny w raku szyjki macicy. Odkryli, że enzym NSUN2 jest głównym „pisarzem” znaków m5C na RNA SERPINB5. W próbkach guzów i liniach komórkowych poziomy NSUN2 były podwyższone, a preferowany motyw sekwencyjny NSUN2 odpowiadał miejscom m5C znalezionym na transkryptach SERPINB5. Gdy NSUN2 został zmniejszony lub genetycznie usunięty, RNA SERPINB5 stawało się mniej stabilne, a poziomy białka spadały — ale tylko wtedy, gdy aktywność katalityczna NSUN2 była utrzymana. Drugie białko, YBX1, pełniło rolę „czytnika”: selektywnie wiązało się z m5C-oznaczonym RNA SERPINB5 i dodatkowo chroniło je przed degradacją. Razem NSUN2 i YBX1 tworzą obwód metylacji RNA, który utrzymuje wysokie poziomy SERPINB5 w komórkach nowotworowych.
Kierowca agresywnego wzrostu i oporności na leki
Testy funkcjonalne ujawniły, jak ważny jest SERPINB5 dla zachowania guza. Gdy zespół obniżył poziomy SERPINB5 w liniach komórek raka szyjki macicy, komórki dzieliły się wolniej, miały mniejszą zdolność migracji i inwazji oraz tworzyły znacznie mniejsze guzy u myszy. Analizy genowe wykazały, że SERPINB5 pomaga utrzymywać cechy podobne do komórek macierzystych, wspiera tworzenie naczyń krwionośnych i sprzyja przejściu komórek w bardziej ruchliwe, inwazyjne stany. Co istotne, SERPINB5 przeprogramowywał także sposób, w jaki komórki radzą sobie z podziałem: zwiększał produkcję regulatorów mitozy i białek motorycznych mikrotubul, takich jak CENPE, CDK1 i CCNB1, które nadzorują aparat wrzeciona rozdzielający chromosomy podczas podziału komórkowego.
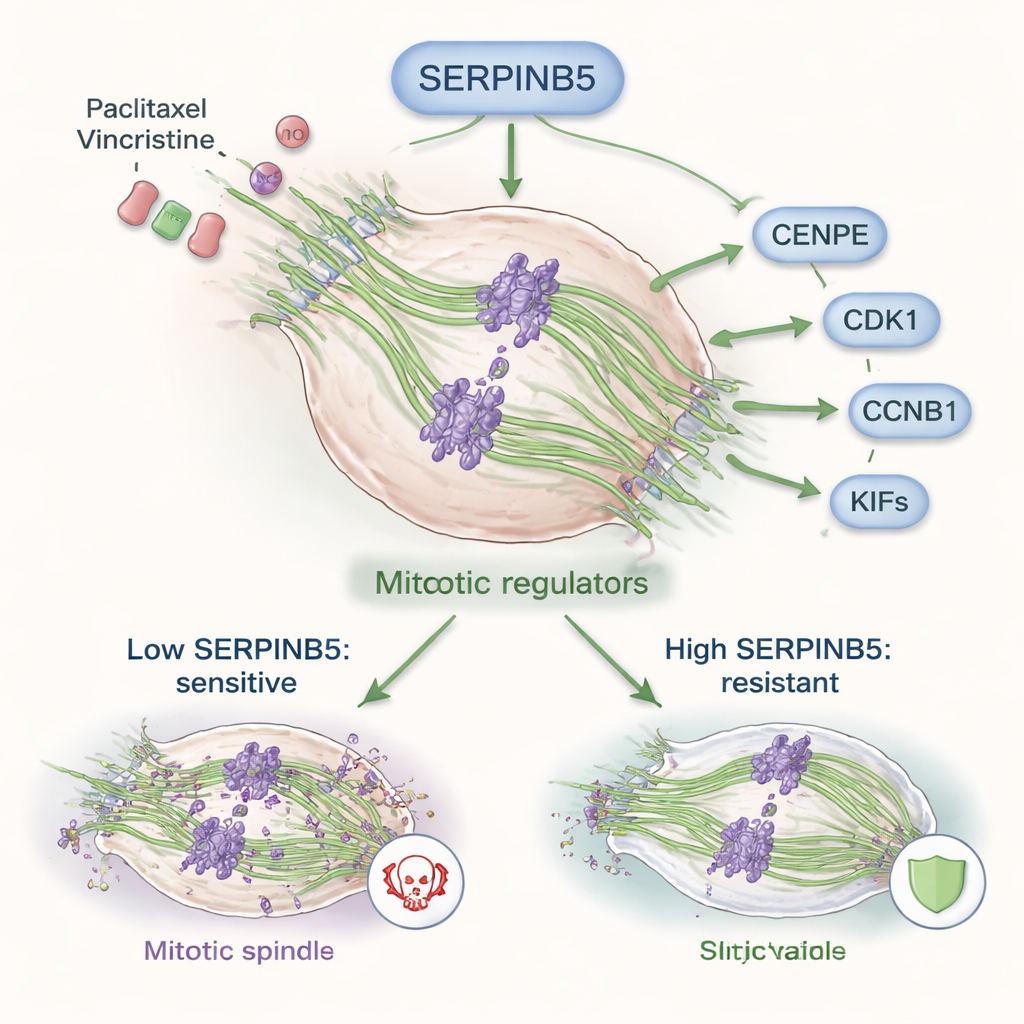
Utrudnianie skuteczności chemioterapii
Paklitaksel i winkrystyna zabijają komórki nowotworowe głównie przez zakłócanie funkcji mikrotubul — włókien strukturalnych tworzących wrzeciono mitotyczne. Zablokowanie tego mechanizmu wymusza na komórkach długotrwałe, śmiertelne zatrzymanie podziału. Badanie pokazuje, że wysokie poziomy SERPINB5 pomagają komórkom nowotworowym przeskoczyć przez tę blokadę. Gdy SERPINB5 został wyciszony, komórki stały się bardziej wrażliwe na oba leki, a do zmniejszenia żywotności potrzebne były niższe dawki. Podobny efekt zaobserwowano po wyeliminowaniu NSUN2, a ponowne wprowadzenie SERPINB5 do komórek pozbawionych NSUN2 przywracało dużą część oporności na leki. Próbki guzów pacjentek, które nie odpowiedziały na terapię opartą na paklitakselu, również wykazywały wyższe poziomy białka SERPINB5 niż guzy wrażliwe na leki, co podkreśla kliniczne znaczenie odkrycia.
Co to oznacza dla przyszłego leczenia
Dla czytelnika nietechnicznego kluczowy przekaz jest taki: niektóre nowotwory szyjki macicy przetrwają i będą się rozrastać, chroniąc pojedynczy, wpływowy transkrypt RNA i jego produkt białkowy — SERPINB5 — za pomocą systemu chemicznych etykiet na RNA. Oś NSUN2–YBX1–SERPINB5 działa jak molekularna tarcza, pomagając guzom szybko się dzielić i opierać przednia linia chemioterapii skierowanej przeciw mikrotubulom. Celowanie w tę oś — przez hamowanie NSUN2, blokowanie wiązania YBX1, bezpośrednie obniżanie SERPINB5 lub monitorowanie SERPINB5 jako biomarkera — mogłoby zwiększyć skuteczność standardowych leków i pomóc zidentyfikować pacjentki, które najprawdopodobniej skorzystają z określonych terapii.
Cytowanie: Liu, J., Zhou, L., Yao, P. et al. M5C-driven stabilization of SERPINB5 promotes cervical cancer progression and chemotherapy resistance. Cell Death Dis 17, 215 (2026). https://doi.org/10.1038/s41419-026-08453-2
Słowa kluczowe: rak szyjki macicy, oporność na chemioterapię, metylacja RNA, SERPINB5, NSUN2