Clear Sky Science · pl
Specyficzne dla oocytów wyłączenie podjednostek eIF2 powoduje apoptozę oocytów myszy w wczesnych pęcherzykach wzrastających poprzez dysfunkcje mitochondrialne i uszkodzenia DNA
Dlaczego życie komórek jajowych ma znaczenie
Kobiety rodzą się ze wszystkimi komórkami jajowymi, jakie kiedykolwiek będą miały, przechowywanymi w maleńkich strukturach jajnika zwanych pęcherzykami. Gdy pęcherzyki utracone są zbyt szybko, może rozwinąć się przedwczesna niewydolność jajników (POI), stan prowadzący do wczesnej niepłodności i często objawów przypominających menopauzę w młodszym wieku. W tym badaniu na myszach postawiono podstawowe, ale istotne pytanie: co dzieje się w komórkach jajowych, gdy kluczowy etap w syntezie nowych białek zawodzi i jak to prowadzi do przedwczesnej utraty płodności?
Przełącznik startu produkcji białek w komórce
Aby pozostać w dobrym stanie, oocyty muszą nieustannie wytwarzać właściwe białka we właściwym czasie. Centralną rolę w tym procesie odgrywa trójczłonowy aparat molekularny zwany eIF2, który pomaga rozpoczynać produkcję białek z informacji genetycznej. Badacze selektywnie wyłączyli dwie podjednostki eIF2, nazwane eIF2α i eIF2β, jedynie w oocytach myszy na wczesnych etapach wzrostu pęcherzyków. Gdy brakowało którejkolwiek z tych podjednostek, samice myszy stały się całkowicie bezpłodne. Ich jajniki były mniejsze, a normalny postęp od wczesnych pęcherzyków do dojrzałych, uwalniających komórki jajowe pęcherzyków w dużej mierze zahamował się — we wszystkich dalszych stadiach obserwowano znacznie mniej pęcherzyków. Z czasem praktycznie wszystkie pęcherzyki zostały wyczerpane, naśladując ciężką, wczesną postać POI.
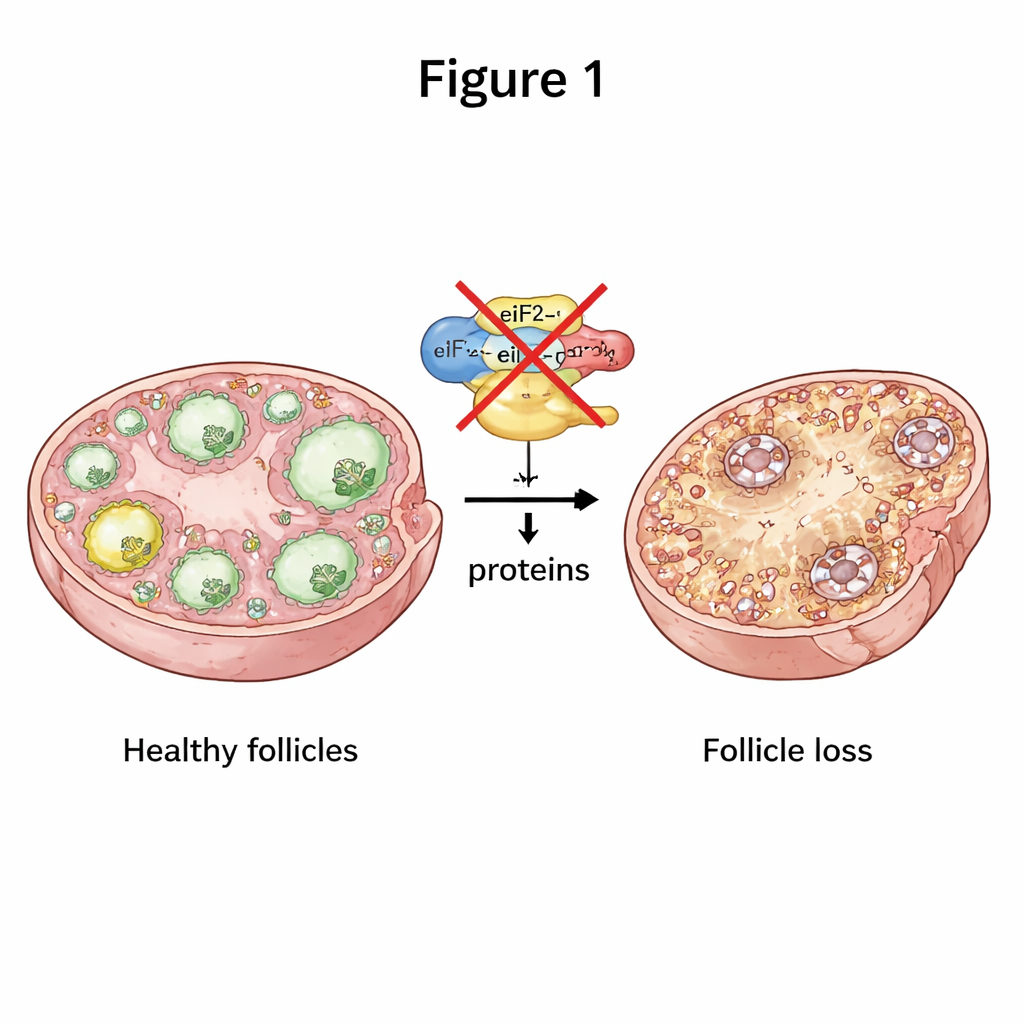
Gdy komunikacja w jajniku ulega załamaniu
Pęcherzyki to nie samotne komórki jajowe; to ścisłe partnerstwo między oocytem a otaczającymi go „komórkami pomocniczymi” — komórkami ziarnistymi. Zespół odkrył, że bez eIF2β oocyty wytwarzały znacznie mniej kilku kluczowych białek sygnałowych, które normalnie wspierają wzrost komórek ziarnistych i dostarczanie składników odżywczych. Fizyczne mostki między oocytem a komórkami ziarnistymi były zdezorganizowane i skrócone, a mikrokosmki na powierzchni oocytu wyglądały zahamowane i uszkodzone w mikroskopie elektronowym. Komórki ziarniste w tych pęcherzykach dzieliły się mniej i częściej umierały. Ten rozpad dwustronnej komunikacji oznaczał, że pęcherzyki nie mogły prawidłowo rosnąć, co wypychało jajnik w kierunku utraty pęcherzyków.
Awarie zasilania w „bateriach” oocytu
Mitochondria, często nazywane elektrowniami komórkowymi, są szczególnie ważne w oocytach, ponieważ dostarczają energii niezbędnej do wzrostu i późniejszego rozwoju embrionu. W oocytach pozbawionych eIF2β ogólny poziom nowej syntezy białek spadł, a wiele białek związanych z mitochondriami było zredukowanych. Mitochondria stały się abnormlanie wydłużone, zgrupowane blisko powierzchni komórki i wykazywały osłabiony potencjał błonowy, niższe poziomy energii (ATP) oraz mniejszą liczbę kopii mitochondrialnego DNA. Równocześnie komórki gromadziły wysokie poziomy reaktywnych form tlenu (ROS), agresywnych cząsteczek tlenowych mogących uszkadzać elementy komórkowe. Razem te zmiany ujawniły głębokie załamanie dynamiki i funkcji mitochondriów.
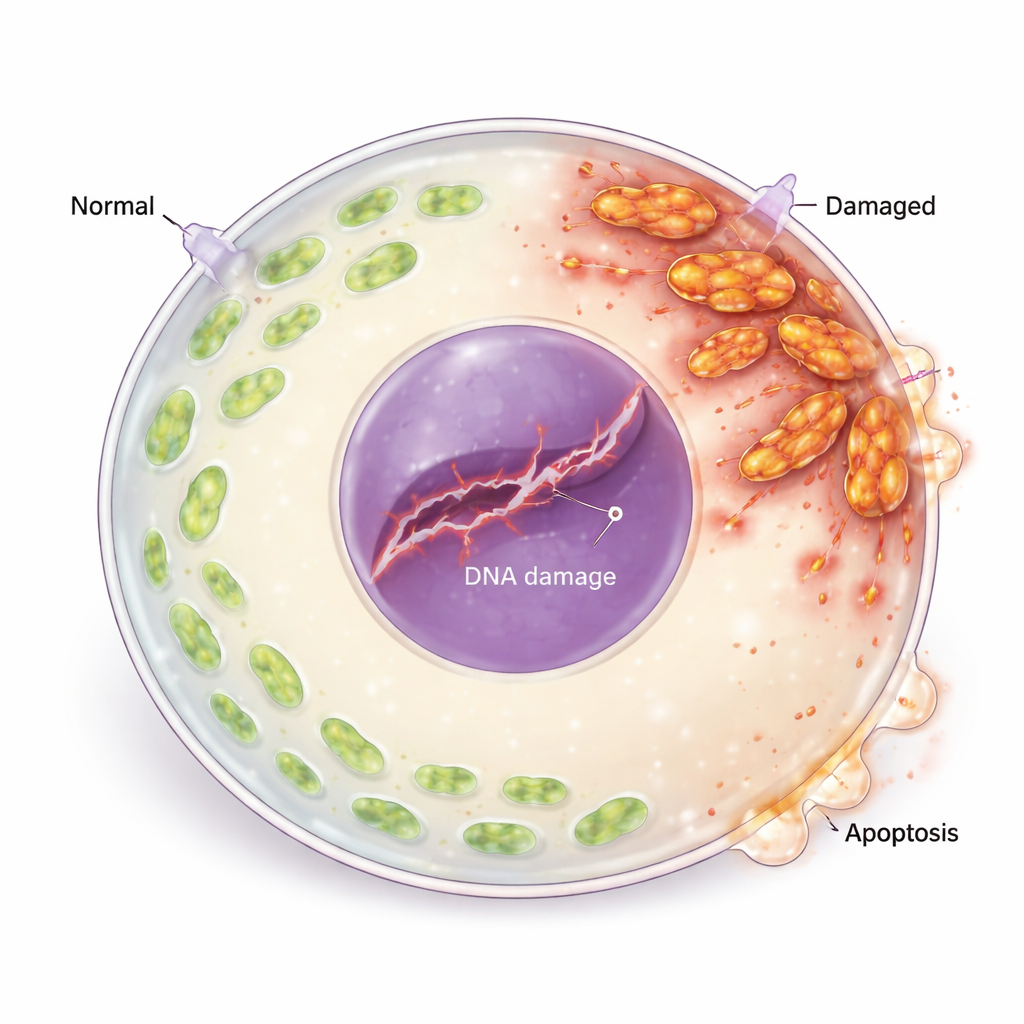
Od stresu oksydacyjnego do uszkodzeń DNA i śmierci komórki
Nadmierne ROS nie tylko szkodziły mitochondriom; uszkadzały także materiał genetyczny oocytu. Badacze zaobserwowali wzrost markerów przerw w nici DNA i aktywację maszynerii odpowiedzi na uszkodzenia DNA, w tym białek, które wykrywają i sygnalizują urazy genetyczne. Jeden z kluczowych białek naprawczych był zredukowany, co sugeruje, że uszkodzenia nie były skutecznie naprawiane. Dalej, równowaga regulatorów życia i śmierci przesunęła się: wzrosły białka proapoptotyczne, a zmalały białka ochronne, i oocyty wykazywały wyraźne cechy zaprogramowanej śmierci komórkowej (apoptozy). Gdy zespół leczył oocyty przeciwutleniaczem (N-acetylocysteiną), poziomy ROS spadły, markery uszkodzeń DNA i apoptozy zmniejszyły się, a dojrzewanie oocytów poprawiło się, co bezpośrednio łączy stres oksydacyjny z utratą komórek jajowych.
Co to oznacza dla wczesnej niewydolności jajników
Śledząc wydarzenia od jednego kompleksu molekularnego (eIF2) przez wadliwą produkcję białek, załamanie mitochondriów, stres oksydacyjny, uszkodzenia DNA, aż po śmierć oocytów, praca ta opisuje szczegółowy łańcuch zdarzeń mogący zniszczyć rezerwę jajnikową. Badanie wzmacnia hipotezę, że mutacje w czynnikach inicjujących translację, już zaobserwowane u niektórych kobiet z POI, mogą bezpośrednio uszkadzać oocyty przez tę ścieżkę. Wskazuje też potencjalne sposoby interwencji: przeciwutleniacze, modulatory odpowiedzi na stres czy terapie chroniące wczesne pęcherzyki (takie jak hormon anty-Müllerowski, który częściowo zachował pęcherzyki uśpione u tych myszy) mogą pewnego dnia wspierać płodność u pacjentek, których jajniki są wrażliwe na podobne stresy.
Cytowanie: Liu, H., Wang, W., Li, B. et al. Oocyte-specific knockout of eIF2 subunits causes apoptosis of mouse oocytes within the early growing follicles via mitochondrial dysfunctions and DNA damage. Cell Death Dis 17, 196 (2026). https://doi.org/10.1038/s41419-026-08449-y
Słowa kluczowe: przedwczesna niewydolność jajników, apoptoza oocytów, dysfunkcja mitochondriów, translacja białek, reaktywne formy tlenu