Clear Sky Science · pl
Transglutaminaza 2 pogarsza przeżywalność raka jajnika poprzez bezpośrednie inaktywowanie GSK3β
Dlaczego te badania mają znaczenie dla zdrowia kobiet
Rak jajnika jest jednym z najbardziej śmiertelnych nowotworów u kobiet, ponieważ zazwyczaj wykrywany jest późno i często nawraca nawet po agresywnej chemioterapii. To badanie ujawnia, jak mało znany białkowy pomocnik, transglutaminaza 2 (TGase 2), pomaga komórkom raka jajnika przetrwać leczenie i rozprzestrzeniać się po organizmie. Wyeksponowanie tego ukrytego sprzymierzeńca nowotworu wskazuje nowe drogi, które mogą uczynić istniejące leki bardziej skutecznymi i spowolnić lub zatrzymać śmiertelne przerzuty.
Ukryty czynnik napędowy w agresywnych guzach
Lekarze od dawna obserwują, że wiele raków jajnika nabywa oporność na chemioterapię i szeroko się rozprzestrzenia w jamie brzusznej. Jednym z głównych winowajców jest proces zwany przejściem nabłonkowo-mezenchymalnym (EMT), w którym komórki nowotworowe luzują swoje połączenia, stają się bardziej ruchome i zachowują się bardziej jak inwazyjne „włóczykije” niż zorganizowane komórki tkanki. Autorzy pracy pokazują, że TGase 2, obecna na bardzo niskim poziomie w prawidłowym jajniku, ale znacznie częściej w guzach jajnika, jest silnie powiązana z tą przemianą. W szerokim panelu ludzkich próbek tkankowych poziomy TGase 2 wzrastały stopniowo od wczesnych stadiów guza do choroby zaawansowanej i przerzutowej, a jej obfitość ściśle korelowała z aktywnością wielu genów związanych z EMT, które kontrolują ruch komórek, wzrost i tworzenie naczyń krwionośnych. 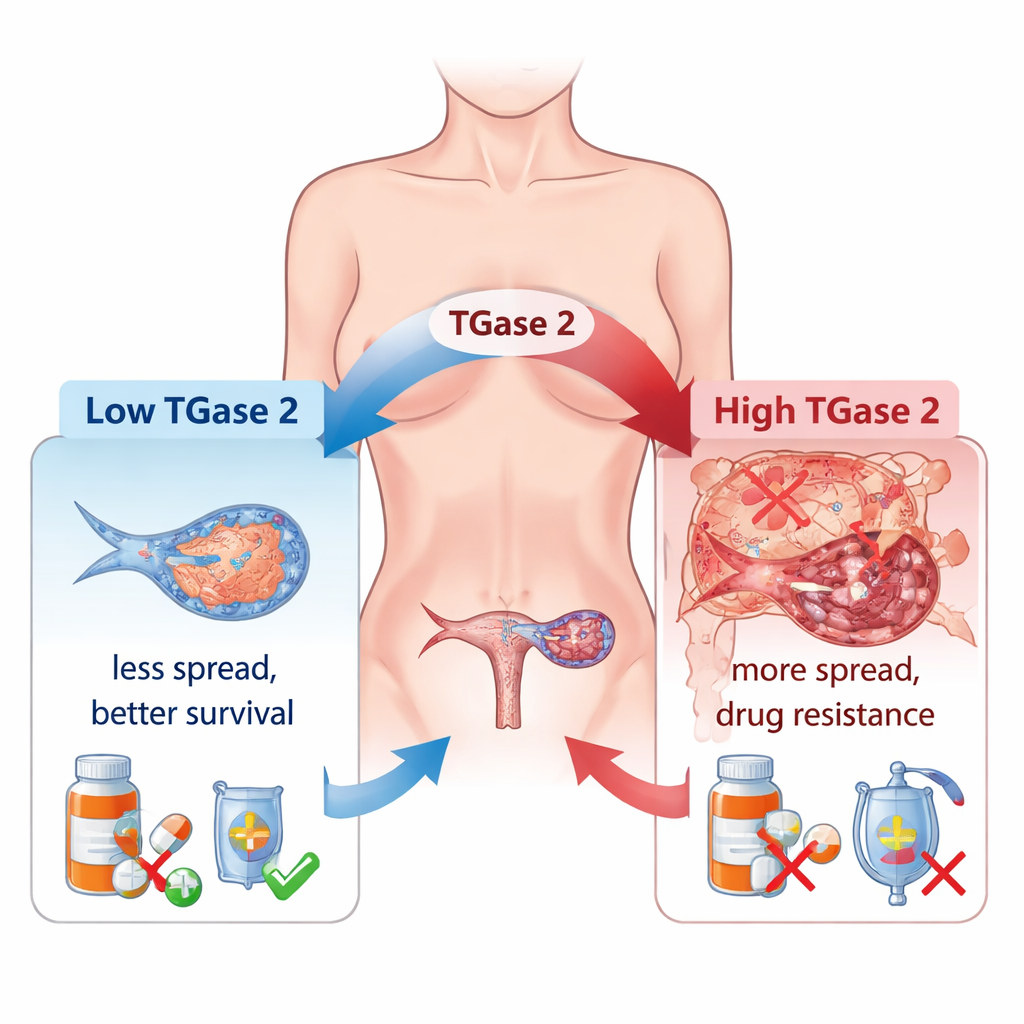
Jak TGase 2 wyłącza kluczowy wyłącznik bezpieczeństwa
Aby zrozumieć, co TGase 2 rzeczywiście robi wewnątrz komórek nowotworowych, badacze skupili się na jej relacji z innym białkiem, GSK3β. W warunkach zdrowych GSK3β działa jak hamulec przed inwazją: utrzymuje niskie poziomy cząsteczki sygnałowej zwanej β-kateniną, co z kolei powstrzymuje geny napędzające EMT. Zespół odkrył, że TGase 2 fizycznie wiąże się z GSK3β, osłabia jej aktywność i sprzyja kierowaniu jej na zniszczenie przez komórkowy system recyklingu, czyli autofagię. Przy wysokiej obfitości TGase 2 komórki raka jajnika przemieszczały się łatwiej i wykazywały wyższe poziomy klasycznych markerów EMT, takich jak fibryonektyna, wimentyna i β-katenina. Gdy badacze zmniejszyli ilość TGase 2 za pomocą narzędzi genetycznych, cechy inwazyjne osłabły, a sygnalizacja β-kateniny została stłumiona, co dowodzi, że TGase 2 dezaktywuje kluczowy wyłącznik przeciw przerzutom.
Od komórek nowotworowych do żywych zwierząt
Zespół zapytał następnie, czy zablokowanie TGase 2 faktycznie mogłoby spowolnić rozwój nowotworu u zwierząt.Zmodyfikowali komórki raka jajnika tak, by brakowało w nich genu TGase 2, i wszczepili je myszom. W porównaniu z myszami otrzymującymi zwykłe komórki nowotworowe, zwierzęta z komórkami pozbawionymi TGase 2 rozwijały mniejsze obciążenie guzem i żyły dłużej. W odrębnym modelu naśladującym rozsiew przez krwiobieg myszy wstrzyknięte komórkami bez TGase 2 miały znacznie mniej i mniejsze przerzuty w płucach. Co ważne, te przerzutowe ogniska wykazywały wyższe poziomy GSK3β, co pasuje do koncepcji, że usunięcie TGase 2 przywraca naturalny hamulec inwazji i pomaga ograniczyć chorobę.
Przekształcanie laboratoryjnej wskazówki w strategię lekową
Ponieważ usuwanie genu nie jest praktyczne u pacjentów, autorzy przetestowali małą cząsteczkę o nazwie streptonigryna, wcześniej znaną z wiązania tego samego końca TGase 2, który używa do chwytania innych białek. Odkryli, że streptonigryna może zaburzyć interakcję TGase 2 z GSK3β w komórkach, zmniejszyć ich ko-lokalizację i ograniczyć migrację komórek nowotworowych. W modelach mysich raka jajnika doustne podawanie streptonigryny spowolniło wzrost guzów, zmniejszyło zmiany przerzutowe i wydłużyło przeżycie. Co najbardziej uderzające, połączenie streptonigryny ze standardowymi lekami chemioterapeutycznymi, takimi jak cisplatyna czy paklitaksel, wydłużało życie myszy o tygodnie w porównaniu z samą chemioterapią. Sama chemioterapia miała tendencję do podnoszenia poziomów TGase 2 i obniżania GSK3β, pośrednio przesuwając komórki w stronę EMT, ale dodanie inhibitora TGase 2 odwracało ten trend i ograniczało nowo nabytą ruchliwość komórek. 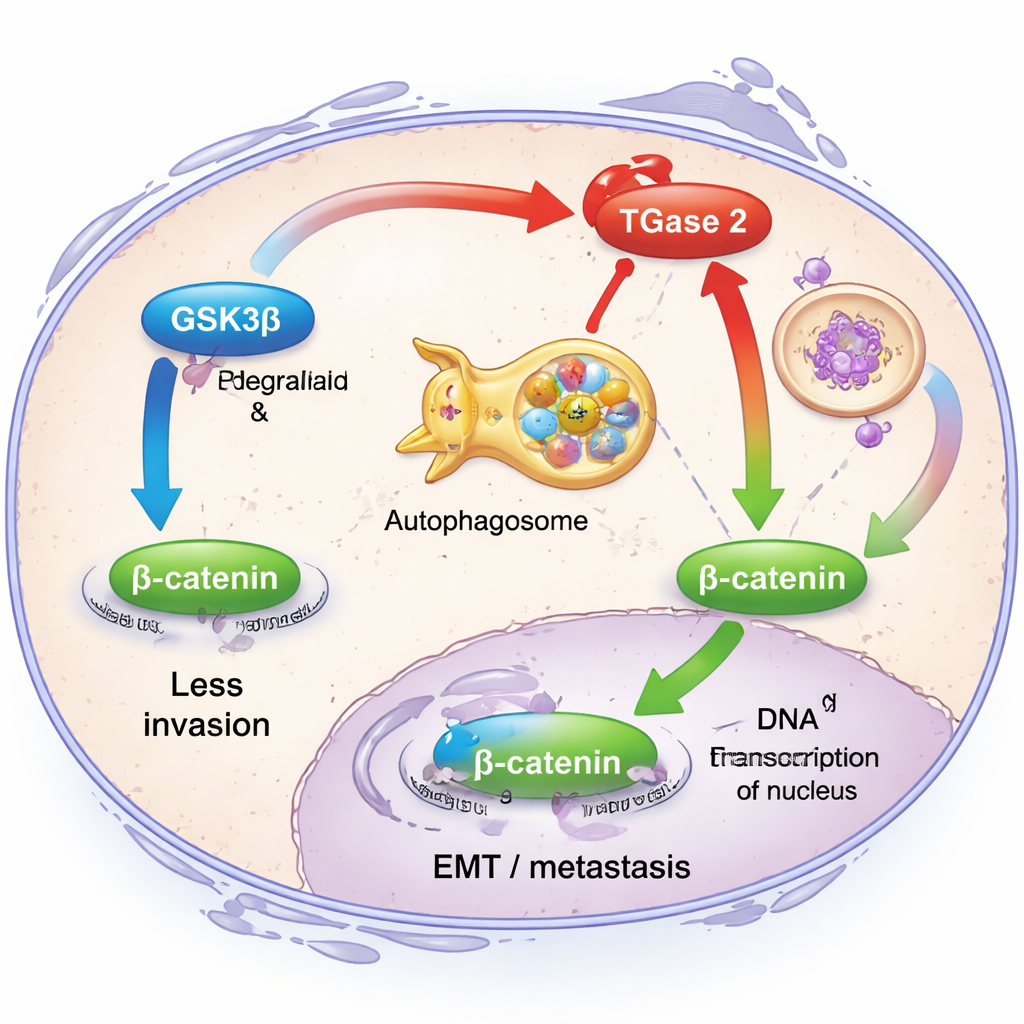
Co to może znaczyć dla przyszłego leczenia
Dla osoby niebędącej specjalistą najważniejszy wniosek jest taki, że komórki raka jajnika wykorzystują TGase 2, aby wyłączyć wbudowany hamulec przeciw przerzutom i przetrwać intensywną chemioterapię. Poprzez bezpośrednie inaktywowanie GSK3β i stabilizowanie β-kateniny, TGase 2 pomaga guzom stać się bardziej inwazyjnymi i odpornymi na leki. Praca ta sugeruje, że leki celujące w region N-terminalny TGase 2 — takie jak streptonigryna lub przyszłe, bezpieczniejsze związki wzorowane na niej — mogłyby poprawić skuteczność istniejącej chemioterapii, zmniejszyć ryzyko nawrotu i poprawić przeżywalność. Mówiąc prosto, ukierunkowanie na TGase 2 może zamknąć „drogę ucieczki” nowotworu, utrzymując guzy jajnika bardziej wrażliwe na leczenie i mniej zdolne do szerzenia się.
Cytowanie: Lee, H., Kang, J.H., Kim, H.J. et al. Transglutaminase 2 exacerbates ovarian cancer survival by directly inactivating GSK3β. Cell Death Dis 17, 199 (2026). https://doi.org/10.1038/s41419-026-08447-0
Słowa kluczowe: rak jajnika, oporność na leki, przerzuty, przejście nabłonkowo-mezenchymalne, terapia celowana