Clear Sky Science · pl
Hamowanie internalizacji receptora B‑komórkowego (BCR) indukowanej przez autoantygeny jako strategia terapeutyczna w chłoniaku rozlanym z dużych komórek B (DLBCL)
Dlaczego to ma znaczenie dla pacjentów
Chłoniak rozlany z dużych komórek B (DLBCL) jest najczęstszym szybko rosnącym nowotworem krwi u dorosłych, a wielu chorych nadal doświadcza nawrotów po standardowej chemioterapii skojarzonej z immunoterapią. Badanie to ujawnia zaskakującą słabość dużej podgrupy tych guzów: ich zależność od anteny na powierzchni komórki zwanej receptorem B‑komórkowym (BCR). Pokazując, że blokowanie mechanizmu wciągania tej anteny do wnętrza komórki może osłabić przeżycie komórek nowotworowych, praca otwiera drogę do ponownego wykorzystania długo stosowanych leków przeciwwymiotnych i przeciwpsychotycznych jako pomocniczych terapii celowanych przeciw chłoniakowi.
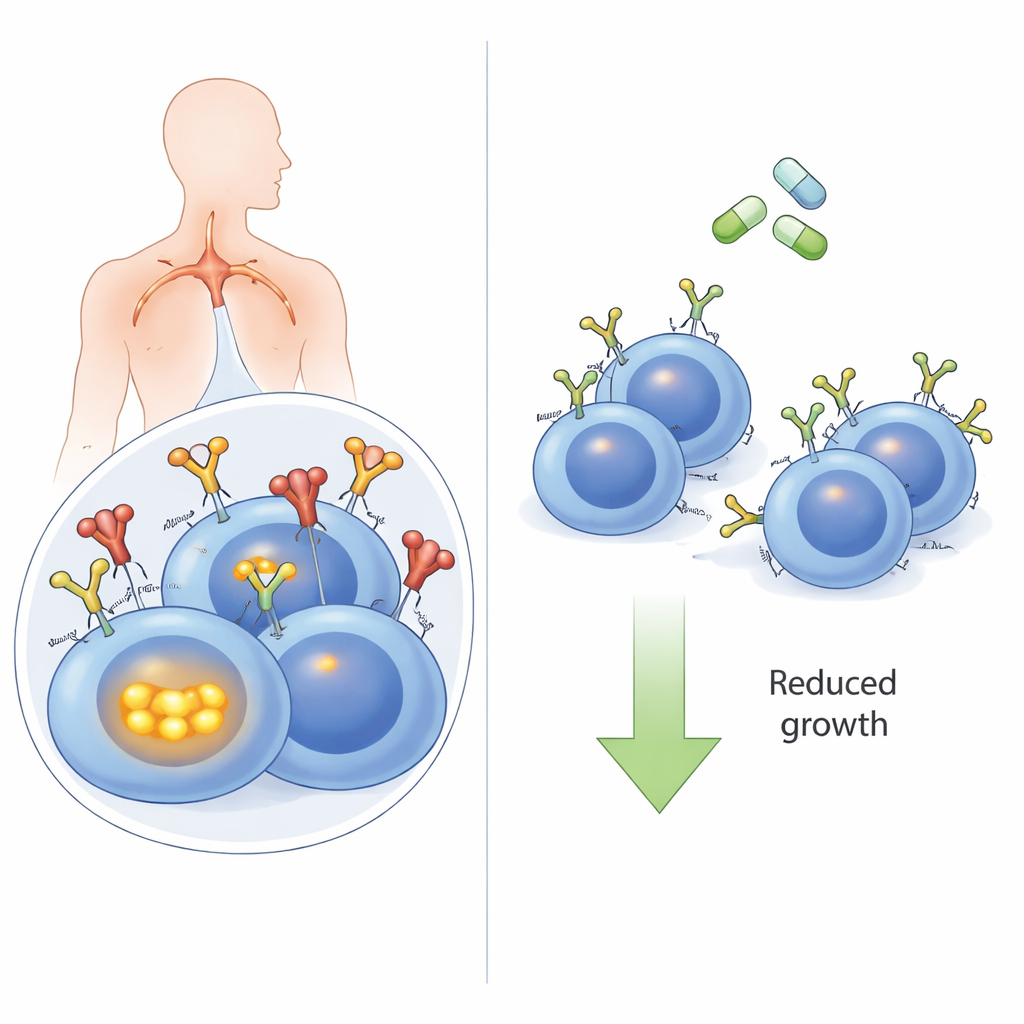
Antenna komórki nowotworowej
Komórki B, rodzaj białych krwinek, używają na swojej powierzchni receptora B‑komórkowego do rozpoznawania zagrożeń. W wielu przypadkach DLBCL, zwłaszcza w wysokiego ryzyka podtypie „aktywowanych komórek B” (ABC), ten sam receptor zostaje zawłaszczony, aby wysyłać ciągłe sygnały „pozostań przy życiu i rośnij”. Często te BCR rozpoznają własne cząsteczki organizmu (autoantygeny), działające jak zaciśnięcy dzwonek do drzwi. Gdy autoantygeny się wiążą, BCR robi więcej niż tylko nadawać sygnał na powierzchni: zostaje wciągnięty do wnętrza komórki i dołącza do wewnętrznego kompleksu białkowego z czujnikami takimi jak TLR9 i MYD88. Ten nadkompleks następnie włącza NFκB, silny szlak promujący wzrost. Dotąd nie było jasne, czy ta wewnętrzna podróż receptora jest rzeczywiście wymagana do generowania sygnałów napędzających nowotwór.
Przeprogramowanie anteny, by sprawdzić jej znaczenie
Aby odpowiedzieć na to pytanie, badacze użyli edycji genów CRISPR, aby precyzyjnie zmienić „końcówki” BCR w liniach komórkowych chłoniaka. Zastąpili naturalne, samoreaktywne regiony rozpoznające wersjami, które rozpoznają ovalbuminę — nieszkodliwe białko jaja używane w laboratorium. Zmienione receptory przestały łapać swoje zwykłe autoantygeny, ale wciąż mogły być kontrolowanie aktywowane przez dodaną ovalbuminę. W komórkach chłoniaka typu ABC, które normalnie zależą od wiązania z autoantygenem, ta zamiana ostro zmniejszyła aktywność wielu kluczowych enzymów sygnałowych i stłumiła geny zależne od NFκB. Komórki rosły wolniej, mimo że faktycznie wykazywały więcej BCR na powierzchni, co pokazuje, że ciągłe zaangażowanie przez autoantygeny i towarzyszące wewnętrzne sygnalizowanie są kluczowe dla ich przeżycia.
Wciąganie receptorów do wnętrza: kluczowy krok
Zespół przyjrzał się bezpośrednio, co dzieje się z BCR po zetknięciu z antygenem. W ich modelach inżynieryjnych zarówno wyzwalacze oparte na przeciwciałach, jak i ovalbumina powodowały znikanie receptora z powierzchni komórki w ciągu kilku minut, potwierdzając szybką internalizację. Działo się to nie tylko wtedy, gdy antygen krążył poza komórką, lecz także gdy był sztucznie prezentowany na błonie tej samej komórki, naśladując pewne rzeczywiste sytuacje w guzach. Genetyczne zablokowanie tego wewnętrznego ruchu, z użyciem formy dominująco‑ujemnej białka dynamin‑2, niezbędnego dla endocytozy zależnej od klatryny, utrzymywało BCR na powierzchni, zmniejszało wewnętrzne kompleksy BCR–TLR9–NFκB, redukowało geny docelowe NFκB i spowalniało wzrost komórek. Co ciekawe, gdy endocytoza była zablokowana, niektóre „tło” sygnałów BCR na powierzchni wzrosło, co sugeruje, że komórki nowotworowe mogą próbować kompensować przez zwiększenie słabszego, tonicznnego trybu sygnalizacji.
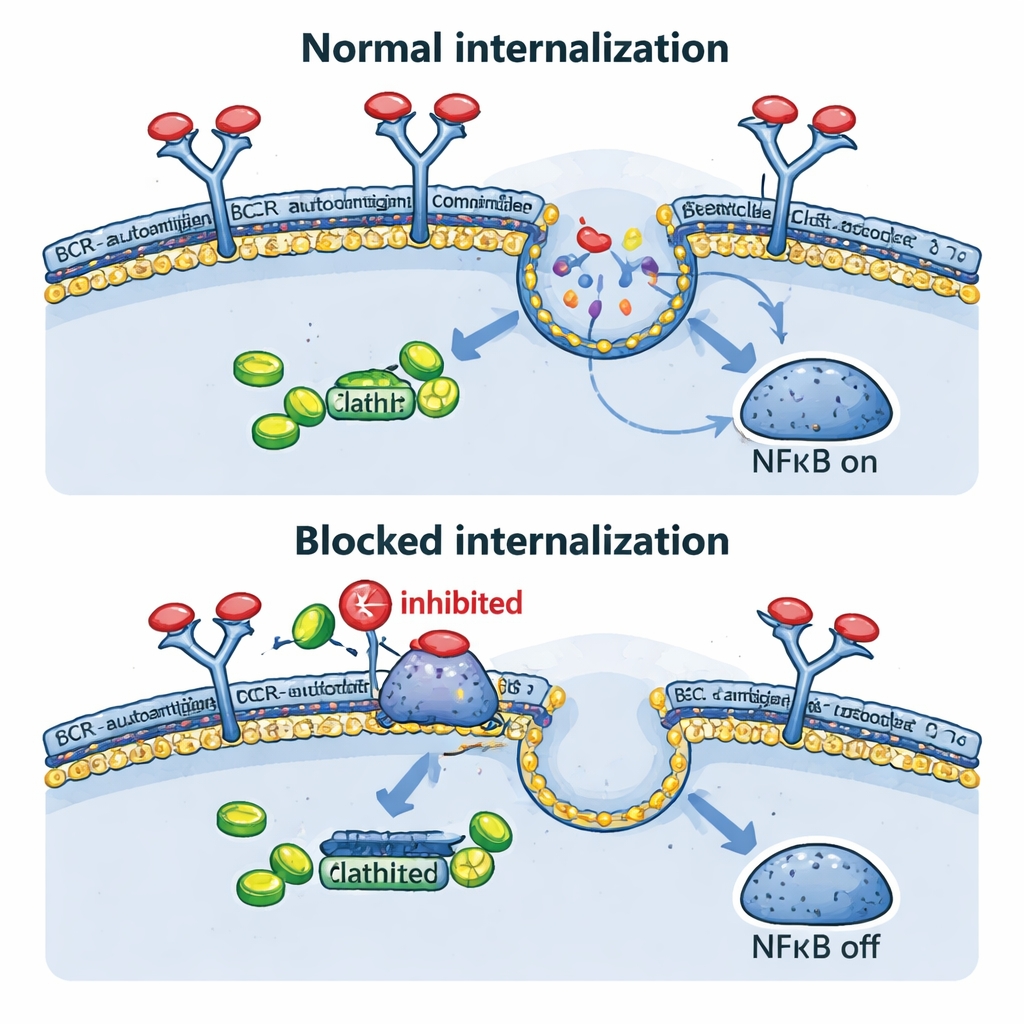
Stare leki, nowe zastosowania
Ponieważ opracowywanie nowych leków jest powolne i kosztowne, autorzy sprawdzili, czy istniejące leki blokujące endocytozę mogą naśladować eksperymenty genetyczne. Fenotiazyny, rodzina leków przeciwpsychotycznych i przeciwwymiotnych, są znane z hamowania dynamin‑2 i pobierania receptorów zależnego od klatryny. W komórkach chłoniaka związki takie jak prochlorperazyna i chlorpromazyna zwiększały poziomy BCR na powierzchni i silnie ograniczały internalizację indukowaną przez antygen. Doprowadziło to do obniżenia aktywności genów napędzanych przez NFκB i zmniejszenia przeżywalności komórek DLBCL typu ABC, szczególnie tych z nienaruszonymi składnikami BCR. U myszy z przeszczepami ludzkiego chłoniaka, prochlorperazyna w dawkach osiągalnych klinicznie znacząco spowolniła wzrost guza. Co więcej, łączenie fenotiazyn z lekami blokującymi inne enzymy powiązane z BCR, takimi jak SYK i PI3Kδ, dało silniejsze efekty przeciwnowotworowe niż każde z tych leczeń osobno.
Co to może oznaczać dla leczenia
Podsumowując, badanie pokazuje, że w istotnej podgrupie DLBCL sygnały napędzające nowotwór nie pochodzą jedynie z receptorów na powierzchni komórki; krytycznie zależą od wciągnięcia kompleksu BCR–antygen do wnętrza przez specyficzną ścieżkę endocytozy. Przerwanie tego etapu — zarówno za pomocą trików genetycznych, jak i leków z grupy fenotiazyn — osłabia sygnalizację NFκB i upośledza przeżycie komórek nowotworowych, jednocześnie potencjalnie zwiększając wrażliwość na istniejące inhibitory szlaku BCR. Ponieważ fenotiazyny mają już dobrze poznane dawki i profil bezpieczeństwa jako leki przeciwwymiotne, praca ta dostarcza realistycznego planu dla badań klinicznych testujących je, samodzielnie lub w skojarzeniu, u pacjentów, których chłoniaki wykazują zależność BCR od autoantygenów.
Cytowanie: Górniak, P., Polak, A., Rams, A. et al. Inhibition of autoantigen-induced B-cell receptor (BCR) internalization as a therapeutic strategy in diffuse large B cell lymphoma (DLBCL). Cell Death Dis 17, 216 (2026). https://doi.org/10.1038/s41419-026-08446-1
Słowa kluczowe: chłoniak rozlany z dużych komórek B, receptor B‑komórkowy, <keyword>fenotiazyny, szlak sygnałowy NFkB