Clear Sky Science · pl
Analiza wielo‑omiczna w czasie narażenia na paklitaksel w ludzkich neuronach czuciowych pochodzących z iPSC ujawnia mechanizmy chemioterapią wywołanej neuropatii obwodowej
Dlaczego niektóre leki przeciwnowotworowe uszkadzają nerwy
Chemioterapia przyczyniła się do przeżycia milionów osób z rakiem, ale wielu pacjentów płaci za to ukrytą cenę: miesiące lub lata piekącego bólu, mrowienia i drętwienia w dłoniach i stopach. W tym badaniu zadano proste, lecz istotne pytanie: co dokładnie robi szeroko stosowany lek przeciwnowotworowy paklitaksel z ludzkimi komórkami nerwowymi czuciowymi i czy zrozumienie tych zmian może naprowadzić na lepsze sposoby zapobiegania i leczenia tego uszkodzenia nerwów?
Od komórek pacjentów do laboratoryjnie hodowanych neuronów czuciowych
Zamiast polegać na eksperymentach na zwierzętach, badacze rozpoczęli od komórek od pięciu ludzkich dawców, w tym pacjentów z rakiem piersi, którzy otrzymali paklitaksel. Przeprogramowali te komórki do indukowanych pluripotencjalnych komórek macierzystych, a następnie ukierunkowali je do postaci neuronów czuciowych — tego samego typu komórek nerwowych, które przekazują sygnały dotyku i bólu ze skóry do rdzenia kręgowego. Te laboratoryjnie hodowane neurony tworzyły długie, delikatne włókna i wykazywały aktywność elektryczną podobną do rzeczywistych neuronów czuciowych w organizmie. Zespół następnie wystawił je na rosnące dawki paklitakselu, naśladując stężenia leku obserwowane u pacjentów, i śledził kondycję komórek przez kilka dni. Przy niskich stężeniach neurony radziły sobie dobrze, ale przy dawce istotnej klinicznie (100 nM) ich przeżywalność zaczęła spadać po około dwóch dniach, co oznacza początek toksycznego uszkodzenia nerwów.
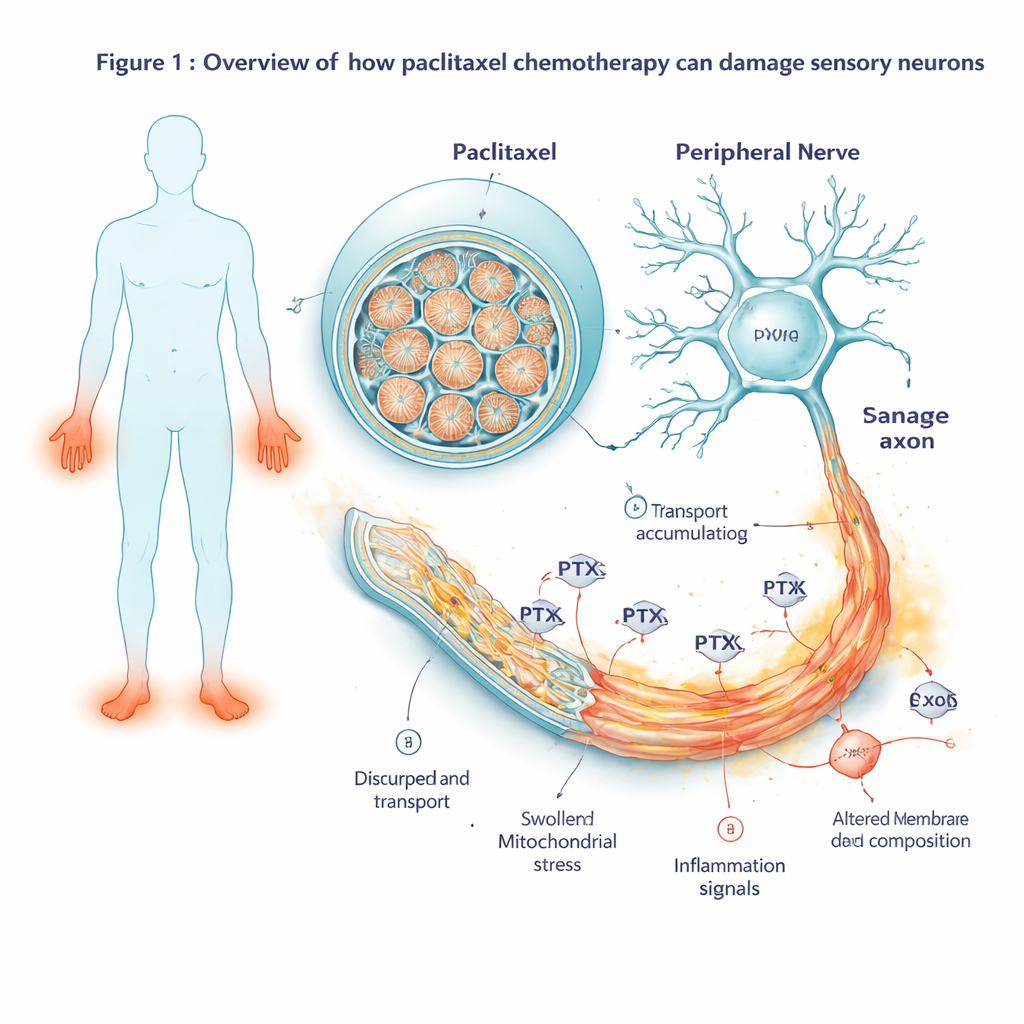
Obserwacja zmian aktywności genów w czasie
Aby zobaczyć, jak komórki reagowały zanim zaczęły się widocznie pogarszać, naukowcy mierzyli, które geny włączają się lub wyłączają w wielu punktach czasowych — od dwóch godzin po ekspozycji na lek do kilku dni po jego usunięciu. Na wczesnym etapie zaobserwowali aktywację klasycznego programu stresu komórkowego skupionego wokół genu JUN. W miarę trwania ekspozycji sygnał stresowy rozszerzał się w pełną kaskadę autodestrukcji: geny skłaniające komórki do zaprogramowanej śmierci były wyraźnie włączane, podczas gdy mechanizmy ochronne zostały przytłoczone. Równocześnie zwiększała się aktywność genów związanych z zapaleniem i sygnalizacją bólową. Neurony zaczęły produkować więcej mediatorów zapalnych, peptydów związanych z bólem i receptorów zwiększających wrażliwość na bodźce szkodliwe — zmiany odzwierciedlające te obserwowane w bolesnych chorobach nerwów.
Dogłębne spojrzenie na białka i lipidy w neuronach
Ponieważ geny są tylko planami, zespół zbadał również białka faktycznie obecne w neuronach oraz ich skład lipidowy (tłuszczowy). Po 48 godzinach ekspozycji na paklitaksel wiele z tych samych sygnałów stresowych i zapalnych wykrytych na poziomie RNA pojawiło się również jako zwiększone poziomy białek, co potwierdzało, że neurony realizują te szkodliwe programy. Co uderzające, białka niezbędne do transportu aksonalnego — molekularne „silniki” i rusztowania przesuwające ładunki wzdłuż długich włókien nerwowych — były wyraźnie zredukowane. Dotyczyło to m.in. kinezyn oraz białek regulujących stabilność mikrotubul. Na poziomie lipidów neurony wykazały spadek kluczowych prekursorów cholesterolu i lipidów błonowych oraz wzrost magazynowanych tłuszczów zwanych triacyloglicerolami. Razem te przesunięcia sugerują, że paklitaksel nie tylko uruchamia szlaki prowadzące do śmierci komórki, ale też osłabia strukturę fizyczną i równowagę energetyczną włókien nerwowych.
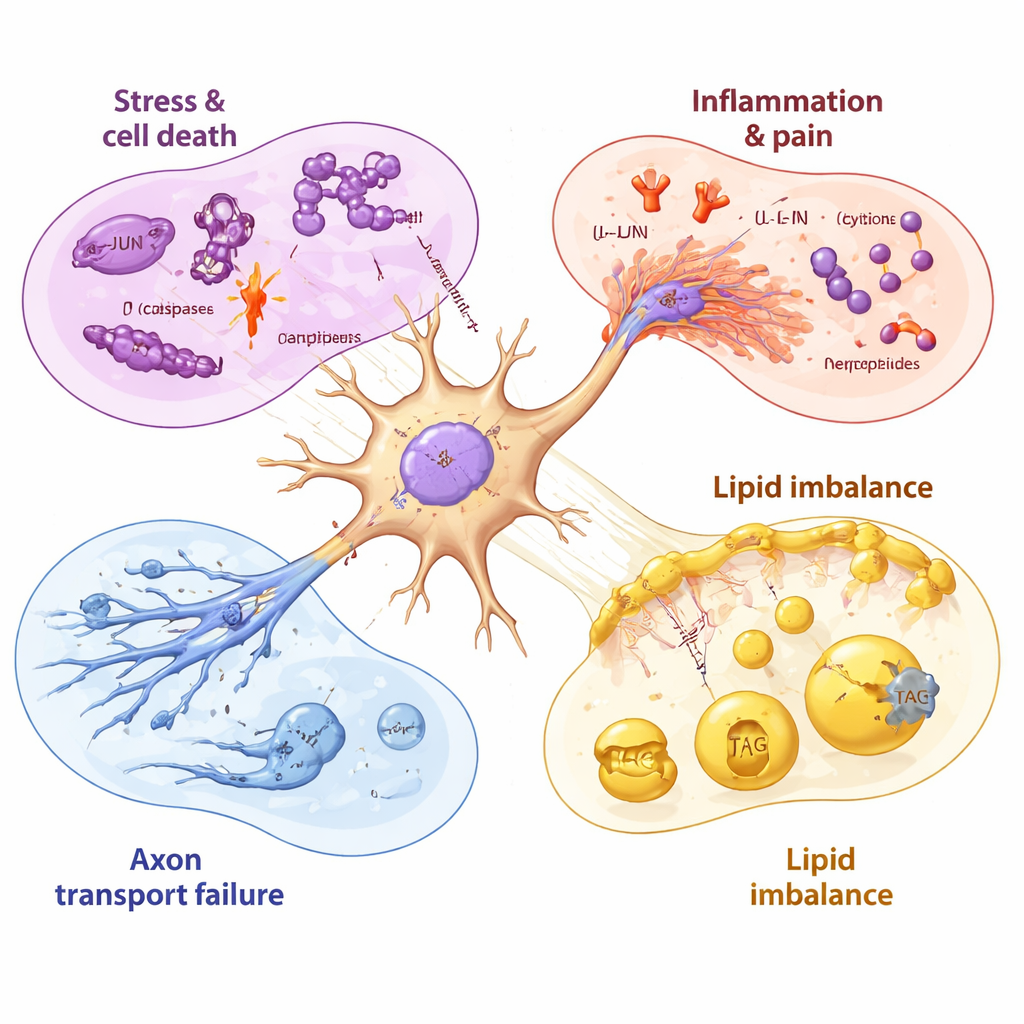
Oś czasu urazu nerwów i niepełne odzyskiwanie
Dzięki próbkowaniu neuronów przed, w trakcie i po ekspozycji na lek, badacze mogli uporządkować te zdarzenia w czasie. Geny mitochondrialne (związane z energetyką) były zaburzone w ciągu godzin, następnie uruchamiał się gen stresowy JUN, a potem silniejsza aktywacja programów śmierci komórkowej i zapalnych w momencie, gdy przeżywalność zaczęła spadać. Nawet po usunięciu paklitakselu wiele szkodliwych sygnałów pozostawało podwyższonych przez dni, podczas gdy geny potrzebne do wytwarzania zdrowych lipidów błonowych nadal spadały. Niektóre późno pojawiające się molekuły, takie jak pompa usuwająca leki, która może wypompowywać paklitaksel, oraz pewne czynniki wzrostu, sugerowały, że neurony próbują się chronić i naprawiać — jednak te odpowiedzi wydawały się stosunkowo powolne i niekompletne w porównaniu z szybkim, wczesnym pchnięciem ku uszkodzeniu.
Co to oznacza dla pacjentów żyjących z bólem nerwów
Dla osoby niebędącej specjalistą przesłanie jest takie: paklitaksel uszkadza neurony czuciowe poprzez skoordynowaną serię uderzeń — stresuje ich systemy energetyczne, przestawia genetyczne przełączniki w kierunku śmierci komórki, wywołuje zapalenie i wzmacnia sygnalizację bólu, zakłóca wewnętrzne „autostrady transportowe” w włóknach nerwowych i zmienia lipidy utrzymujące stabilność błon nerwowych. Mapując te zmiany w neuronach pochodzenia ludzkiego w szczegółowy sposób, badanie wskazuje konkretne, możliwe do farmakologicznego celowania mechanizmy — takie jak specyficzni regulatorzy stresu, receptory zapalne i enzymy syntezy lipidów — które można by zablokować lub wspierać, aby chronić nerwy bez osłabiania leczenia przeciwnowotworowego. Choć nowe terapie będą wymagały dalszych badań, praca ta oferuje jaśniejszą mapę drogową do zapobiegania lub łagodzenia uszkodzeń nerwów wywołanych chemioterapią, poprawiając jakość życia osób, które przeżyły raka.
Cytowanie: Schinke, C., Maierhof, S.K., Hew, L. et al. Time‑resolved multi-omic analysis of paclitaxel exposure in human iPSC‑derived sensory neurons unveils mechanisms of chemotherapy‑induced peripheral neuropathy. Cell Death Dis 17, 211 (2026). https://doi.org/10.1038/s41419-026-08445-2
Słowa kluczowe: chemioterapią wywołana neuropatia obwodowa, paklitaksel, neurony czuciowe, neurozapalenie, degeneracja aksonów