Clear Sky Science · pl
Odwracalna metylacja argininy reguluje aktywność mitochondrialnego IDH2: skoordynowana kontrola przez CARM1 i KDM3A/4A
Precyzyjne strojenie „elektrowni” komórki
Mitochondria, często nazywane elektrowniami komórek, robią znacznie więcej niż tylko wytwarzają energię. Stale dostosowują sposób pozyskiwania i spalania paliwa do potrzeb organizmu, a zaburzenia tych mechanizmów mogą przyczyniać się do chorób takich jak cukrzyca, niewydolność serca czy rak. W tej pracy odkryto ukryty „regulator natężenia” wewnątrz mitochondriów: małą chemiczną etykietę na pojedynczym aminokwasie kluczowego enzymu IDH2, która pomaga decydować, czy mitochondria pracują oszczędnie, czy zwiększają produkcję energii.
Maleńka etykieta o dużych konsekwencjach
Białka w naszych komórkach nie są statyczne; często są modyfikowane małymi grupami chemicznymi, które zmieniają ich właściwości. Chociaż wiele takich modyfikacji w jądrze i cytoplazmie jest dobrze poznanych, modyfikacje zachodzące w mitochondriach są mniej zbadane. Autorzy skupili się na jednym rodzaju oznaczenia — metylacji argininy — i sprawdzili, czy może ono regulować aktywność enzymów mitochondrialnych. Skoncentrowali się na enzymie IDH2, ważnym ogniwie cyklu kwasów trikarboksylowych (TCA), który pomaga przekształcać składniki odżywcze w energię i niezbędne metabolity. Przy użyciu narzędzi biochemicznych i spektrometrii mas wykazali, że IDH2 nosi specyficzną metylową oznakę na jednym aminokwasie, argininie 188, a tą modyfikację wprowadza enzym CARM1, który zaskakująco działa także wewnątrz mitochondriów.
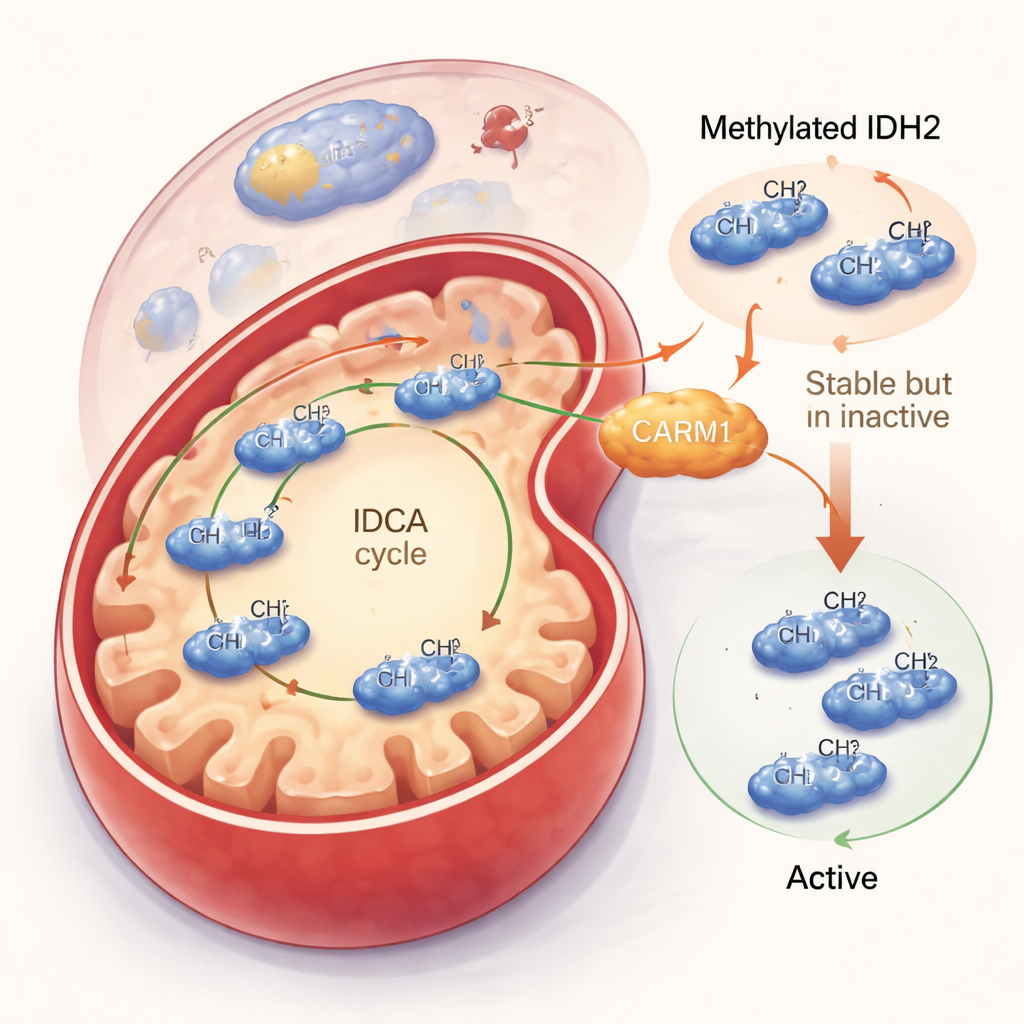
Wyłączanie IDH2 przy jednoczesnym wydłużeniu jego żywotności
Zespół zapytał następnie, co ta metylacja faktycznie robi. Gdy CARM1 był aktywny i metylował IDH2, białko to stawało się bardziej stabilne i dłużej utrzymywało się w komórce. Ten pozorny plus miał jednak swoją cenę: metylowany IDH2 był mniej aktywny. W eksperymentach na komórkach i z oczyszczonym białkiem metylowany IDH2 produkował mniej swojego głównego produktu, alfaketoglutaranu, i wytwarzał mniej ochronnego NADPH. Natomiast wersja IDH2 niemogąca być metylowana w pozycji argininy 188 częściej przyjmowała aktywną formę dimeru, działała szybciej i zwiększała poziomy zarówno alfaketoglutaranu, jak i NADPH. Chociaż całkowita ilość tego niemetylowanego IDH2 była mniejsza, każda cząsteczka wykonywała więcej pracy, co prowadziło do netto wzrostu wydajności mitochondrialnej.
Odwracalny przełącznik z dwoma „gumkami”
Co istotne, ta metylowa etykieta nie jest trwała. Badacze wykazali, że dwa enzymy znane głównie z usuwania innego typu modyfikacji, demetylazy lizynowe KDM3A i KDM4A, potrafią także zetrzeć metylację argininy na IDH2. Gdy te demetylazy były obecne, metylowana arginina w pozycji 188 traciła dodatkowe grupy chemiczne, IDH2 stawał się mniej stabilny, ale bardziej aktywny, a jego forma dimeru zwiększała się. Komórki z wyższą aktywnością KDM3A lub KDM4A wykazywały większy potencjał błony mitochondrialnej i szybsze zużycie tlenu, co wskazuje, że mitochondria działały bardziej intensywnie w trybie oksydacyjnym. Gdy te enzymy były osłabione, następowało odwrotne zjawisko: aktywność IDH2 spadała, a wydajność mitochondriów malała, co podkreśla, że mamy do czynienia z odwracalnym systemem kontroli, a nie jednostronną zmianą.
Powiązanie metabolizmu i chorób
Ponieważ IDH2 został powiązany z rakiem i innymi schorzeniami, autorzy zbadali, jak ten metylacyjny przełącznik może wpływać w kontekstach przypominających chorobę. W różnych liniach komórkowych, zarówno normalnych, jak i nowotworowych, zaobserwowali, że wyższe poziomy białka IDH2 często szły w parze z większą metylacją i — paradoksalnie — niższą aktywnością enzymatyczną, co sugeruje, że „więcej białka” nie zawsze oznacza „więcej funkcji”. W zestawach danych raka piersi pacjenci z wyższymi poziomami białka IDH2 mieli skłonność do gorszego przeżycia, mimo że aktywność genu IDH2 nie korelowała z wynikami. Wyniki wspierają model, w którym metylacja napędzana przez CARM1 spowalnia cykl TCA i skłania komórki ku alternatywnym, sprzyjającym rakowi sposobom wykorzystania składników odżywczych, podczas gdy demetylazy takie jak KDM3A i KDM4A mogą przesuwać komórki z powrotem w stronę efektywniejszej produkcji energii.
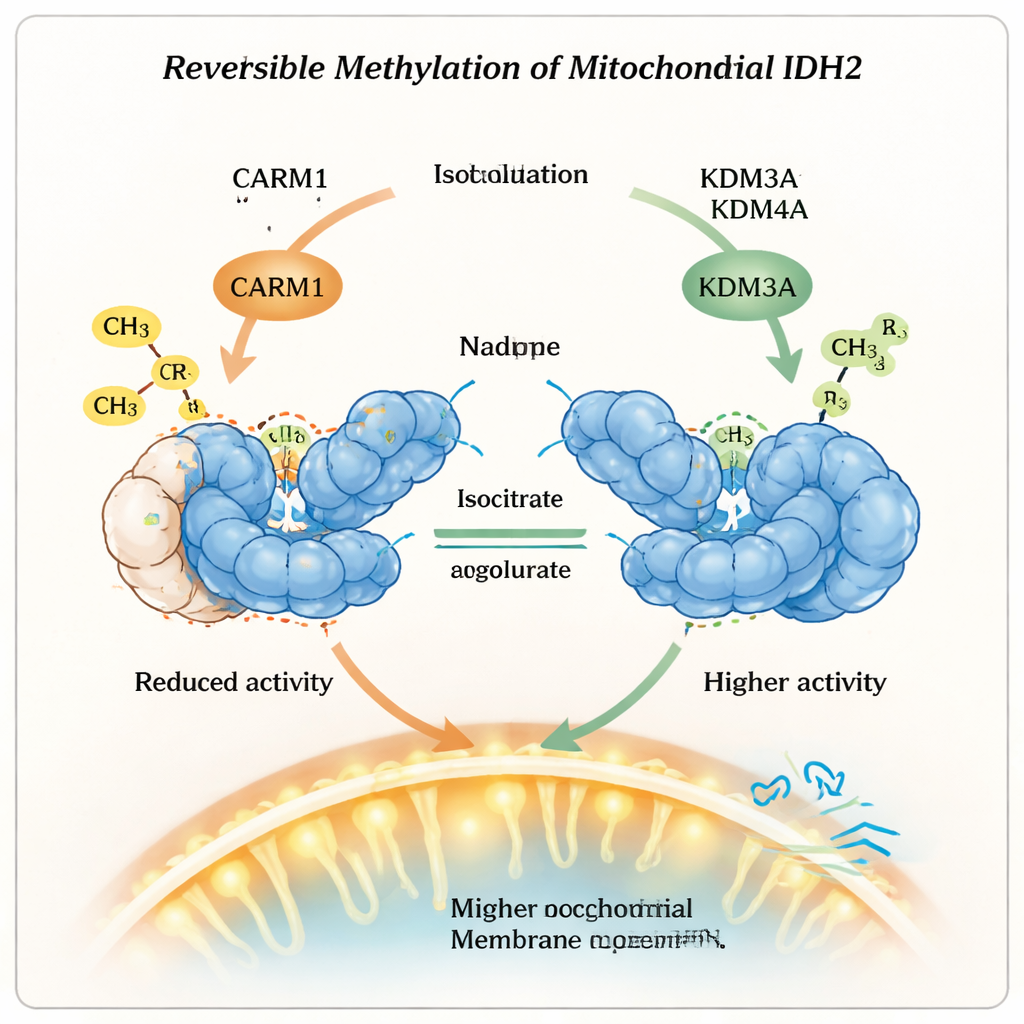
Co to znaczy dla zdrowia i terapii
Mówiąc prosto, ta praca pokazuje, że mitochondria nie tylko włączają lub wyłączają enzymy, lecz używają odwracalnych znaków chemicznych jako precyzyjnych regulatorów. Dodając grupę metylową, CARM1 przekształca IDH2 w formę dłużej trwającą, ale mniej aktywną; usuwając ten znak, KDM3A i KDM4A kosztem pewnej stabilności przywracają większą moc. Ta równowaga wpływa na to, czy komórki wybierają szybkie, ale mniej wydajne spalanie cukrów, czy wolniejsze, bardziej efektywne wytwarzanie energii. Zrozumienie tego metylacyjnego „regulatora natężenia” na IDH2 otwiera nowe możliwości terapeutyczne mające na celu skorygowanie zaburzonego metabolizmu mitochondrialnego w chorobach takich jak rak czy schorzenia metaboliczne, poprzez celowanie w enzymy, które zapisują i wymazują te małe, lecz wpływowe modyfikacje chemiczne.
Cytowanie: Cho, Y., Winarto, J., Song, DG. et al. Reversible arginine methylation regulates mitochondrial IDH2 activity: coordinated control by CARM1 and KDM3A/4A. Cell Death Dis 17, 195 (2026). https://doi.org/10.1038/s41419-026-08444-3
Słowa kluczowe: mitochondria, IDH2, metylacja argininy, metabolizm komórkowy, CARM1