Clear Sky Science · pl
Zapętlenie zapalne MIF-p38-GSDMD w keratynocytach leży u podstaw skórnego tocznia indukowanego UVB
Dlaczego światło słoneczne może być poważnym problemem w toczniu
Dla większości ludzi słońce daje jedynie opaleniznę lub, w najgorszym wypadku, oparzenie słoneczne. Dla wielu pacjentów z toczniem jednak kilka minut promieniowania ultrafioletu B (UVB) może wywołać bolesne, długo utrzymujące się wysypki, a nawet pogorszyć przebieg całej choroby. Badanie to odsłania ukrytą „pętlę sprzężenia zwrotnego” wewnątrz komórek skóry, która pomaga wyjaśnić, dlaczego ich skóra jest tak wrażliwa na światło — i wskazuje na nowe, bardzo lokalne terapie mogące złagodzić reakcję bez tłumienia całego układu odpornościowego.
Komórki skóry jako nieoczekiwani sprawcy
Lekarze od dawna wiedzą, że skórny toczeń rumieniowaty (CLE) wiąże się z przewlekłym zapaleniem i bliznowaceniem skóry, lecz uwagę często skupiano na napływających komórkach odpornościowych. Autorzy zastosowali sekwencjonowanie RNA pojedynczych komórek i zamiast tego przyjrzeli się budulcowym komórkom skóry — keratynocytom w warstwie zewnętrznej i fibroblastom pod nimi. Odkryli, że u pacjentów z toczniem pewne podgrupy keratynocytów są powiększone i wykazują silny „podpis interferonowy”, czyli trwałe włączenie genów alarmujących o infekcji wirusowej. W tych nieprawidłowych keratynocytach wyróżniał się jeden białkowy przekaźnik: czynnik hamujący migrację makrofagów, MIF, produkowany na znacznie wyższym poziomie niż bardziej znane molekuły zapalne, takie jak TNF czy IL‑6.
Ukryty przekaźnik uwalniany przez światło
Stwierdzenie wysokiego poziomu MIF w keratynocytach nie wyjaśniało jeszcze, dlaczego światło UVB jest tak groźne. Gdy zespół naświetlił hodowane keratynocyty UVB, odkrył, że całkowita ilość MIF w komórkach niemal się nie zmienia — natomiast białko jest uwalniane do otaczającego płynu w zależności od dawki. Im więcej UVB, tym więcej MIF wyciekało, co ściśle korelowało ze znacznikiem uszkodzenia błony komórkowej. Gdy ten płyn bogaty w MIF zastosowano na świeżych keratynocytach i fibroblastach, wywołał on klasyczne zmiany przypominające CLE: więcej cytokin zapalnych i enzymów rozkładających oraz przebudowujących macierz podporową skóry. Wyciszenie MIF narzędziami genetycznymi lub zablokowanie go małą cząsteczką znacznie zmniejszało te szkodliwe reakcje, pokazując, że MIF pochodzący z keratynocytów nie jest tylko obserwatorem, lecz kluczowym wzmacniaczem uszkodzeń wywołanych UVB. 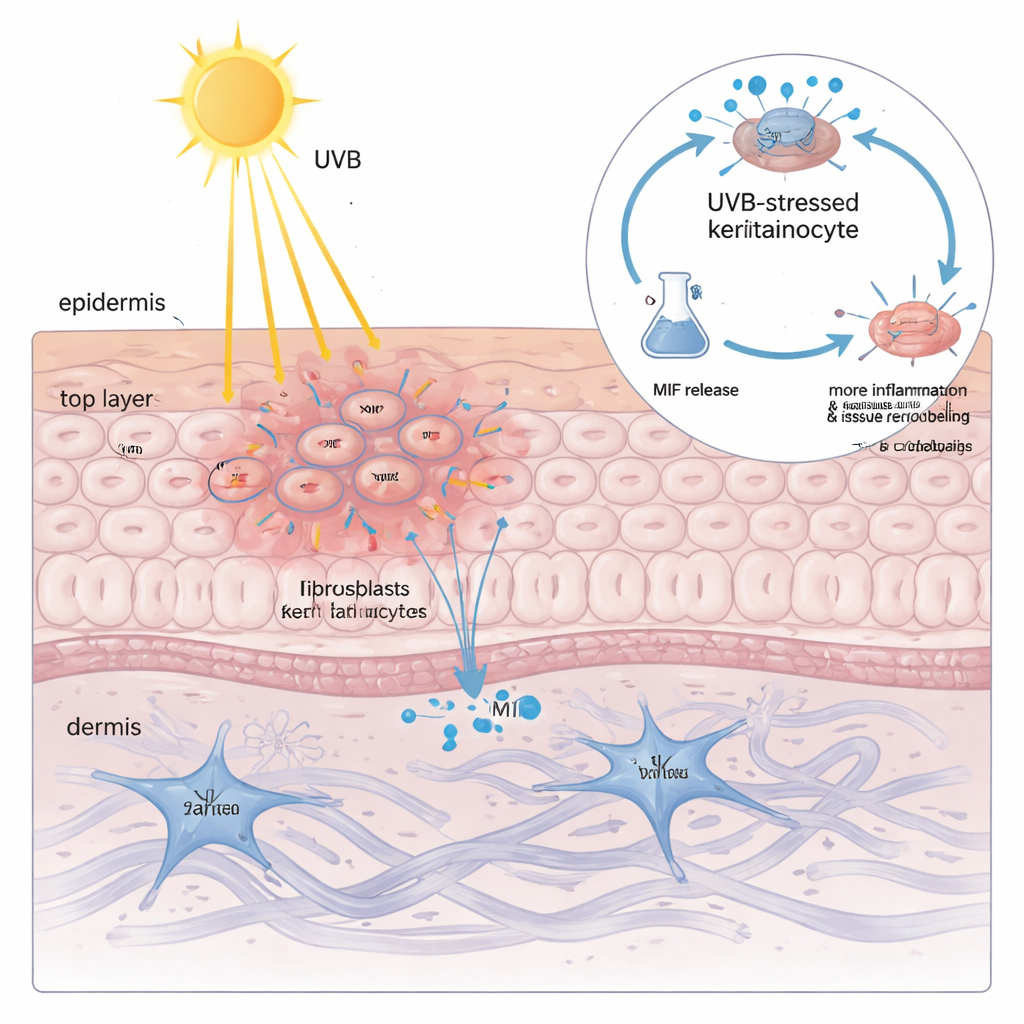
Samopodtrzymująca się pętla zapalna w keratynocytach
Aby zrozumieć, jak UVB zmusza keratynocyty do uwalniania MIF, naukowcy zbudowali model keratynocytów „przypominający toczeń” przez załadowanie komórek ich własnym DNA i RNA, naśladując niewłaściwie rozregulowane szczątki genetyczne obserwowane w toczniu. W tym uprzednio uaktywnionym stanie UVB uruchomiło tzw. ribotoksyczną odpowiedź na stres: sygnał uszkodzenia z rybosomów, który włącza kinazę ZAKα, a dalej enzym stresowy p38. Ta ścieżka zwiększała poziom kolejnego białka, czynnika transkrypcyjnego C/EBPβ, który wiązał się z regionem kontrolnym genu NLRP3 i go aktywował. NLRP3 następnie napędzał rozszczepienie GSDMD, białka tworzącego pory, które przebija otwory w błonie komórkowej i wywołuje zapalną formę śmierci komórki znaną jako pyroptoza. Co istotne, MIF uciekał głównie przez te pory GSDMD — nie przez normalne pęcherzyki wydzielnicze. Po wydostaniu się na zewnątrz MIF wiązał się ze swoim receptorowym białkiem powierzchniowym CD74 na keratynocytach, ponownie aktywując p38, NLRP3 i GSDMD i zamykając tym samym zgubne koło: UVB → p38 → NLRP3 → pory GSDMD → uwolnienie MIF → większa aktywacja p38.
Od wnikliwego opisu molekularnego do nowych, miejscowych terapii
Ta pętla nie była tylko ciekawostką laboratoryjną. U myszy predysponowanej do tocznia ekspozycja na UVB wywołała ciężkie zmiany skórne z wysokimi poziomami MIF, aktywacją p38, NLRP3 i rozszczepionego GSDMD w naskórku. Gdy badacze zastosowali wirus do terapii genowej, by specyficznie wyciszyć gen Mif w skórze, wysypki indukowane przez UVB były znacznie łagodniejsze, a markery zapalenia i przebudowy tkanek spadły zarówno w keratynocytach, jak i fibroblastach. Aby uniknąć działań niepożądanych na cały organizm, opracowali także rozpuszczalne plastry z mikroniciami naładowane inhibitorem MIF ISO‑1. Krótkie przyciśnięcie tych maleńkich igiełek do skóry bezboleśnie dostarczało lek do górnych warstw. Leczone myszy predysponowane do tocznia miały znacznie mniej i łagodniejsze zmiany po UVB, a molekularny podpis pętli MIF‑p38‑GSDMD był wyraźnie stłumiony. 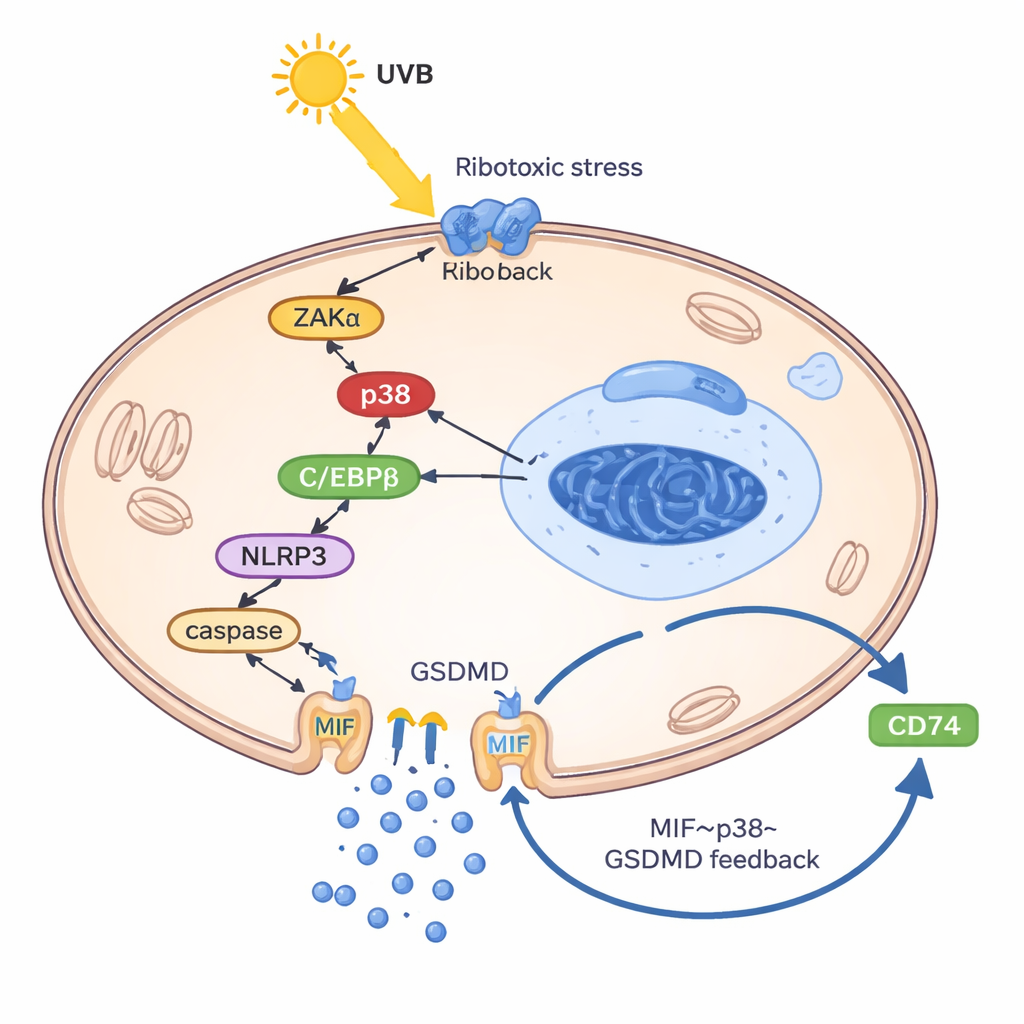
Co to oznacza dla osób z toczniem
Mówiąc wprost, praca ta pokazuje, że w toczniu pewne komórki skóry są zaprogramowane do nadmiernej reakcji na UVB poprzez uwalnianie potężnej „wzmacniającej” cząsteczki MIF przez samodzielnie wytworzone pory w błonie. To wzmocnienie potem napędza maszynerię zapalną dalej, nawet po ustaniu początkowej ekspozycji na światło. Mapując tę pętlę krok po kroku, badanie sugeruje, że blokowanie MIF bezpośrednio w skórze — za pomocą wyciszania genów lub inteligentnych systemów dostarczania, takich jak plastry z mikroniciami — mogłoby przerwać cykl zaostrzeń wrażliwych na światło, bez szerokiego tłumienia układu odpornościowego. Jeśli podobne strategie okażą się bezpieczne i skuteczne u ludzi, mogą dać osobom z toczniem nowe sposoby, by żyć bardziej komfortowo na świetle.
Cytowanie: Guo, C., Luo, S., Luo, J. et al. A MIF-p38-GSDMD inflammatory loop in keratinocytes underlies UVB-induced cutaneous lupus. Cell Death Dis 17, 198 (2026). https://doi.org/10.1038/s41419-026-08443-4
Słowa kluczowe: skórny toczeń, nadwrażliwość na światło, keratynocyty, pętla zapalna, terapia mikroniciami