Clear Sky Science · pl
Honokiol blokuje rozwój guza i przerzuty poprzez efekty ukierunkowane na mitochondria
Przekształcanie związku z drzewa w broń przeciw rakowi
Wiele leków przeciwnowotworowych pochodzi z roślin, a naukowcy wciąż odkrywają, jak niektóre z tych naturalnych cząsteczek działają wewnątrz naszych komórek. W tym badaniu skupiono się na honokiolu, substancji występującej w korze magnolii, od dawna stosowanej w medycynie tradycyjnej, i wykazano, że może bezpośrednio atakować maleńkie elektrownie w komórkach nowotworowych, spowalniając wzrost guzów i blokując ich rozprzestrzenianie się, przy jednoczesnym stosunkowo niewielkim oddziaływaniu na komórki normalne.
Stacje energetyczne wewnątrz naszych komórek
Każda komórka polega na mitochondriach, często nazywanych „stacjami energetycznymi” komórki, w celu wytwarzania cząsteczki energii ATP. W nowotworach mitochondria robią więcej niż tylko produkcję paliwa — pomagają decydować, czy komórka przetrwa, czy zginie. Jedna duża maszyna molekularna, syntaza ATP, znajduje się w wewnętrznej błonie mitochondrium i syntetyzuje ATP. Komórki nowotworowe często nadprodukują białko partnerskie zwane IF1, które przyczepia się do syntazy ATP i działa jak blokada bezpieczeństwa, pomagając guzom przeciwstawiać się formie samobójczej zwanej przejściem przepuszczalności mitochondrialnej i następującej po niej śmierci komórki.
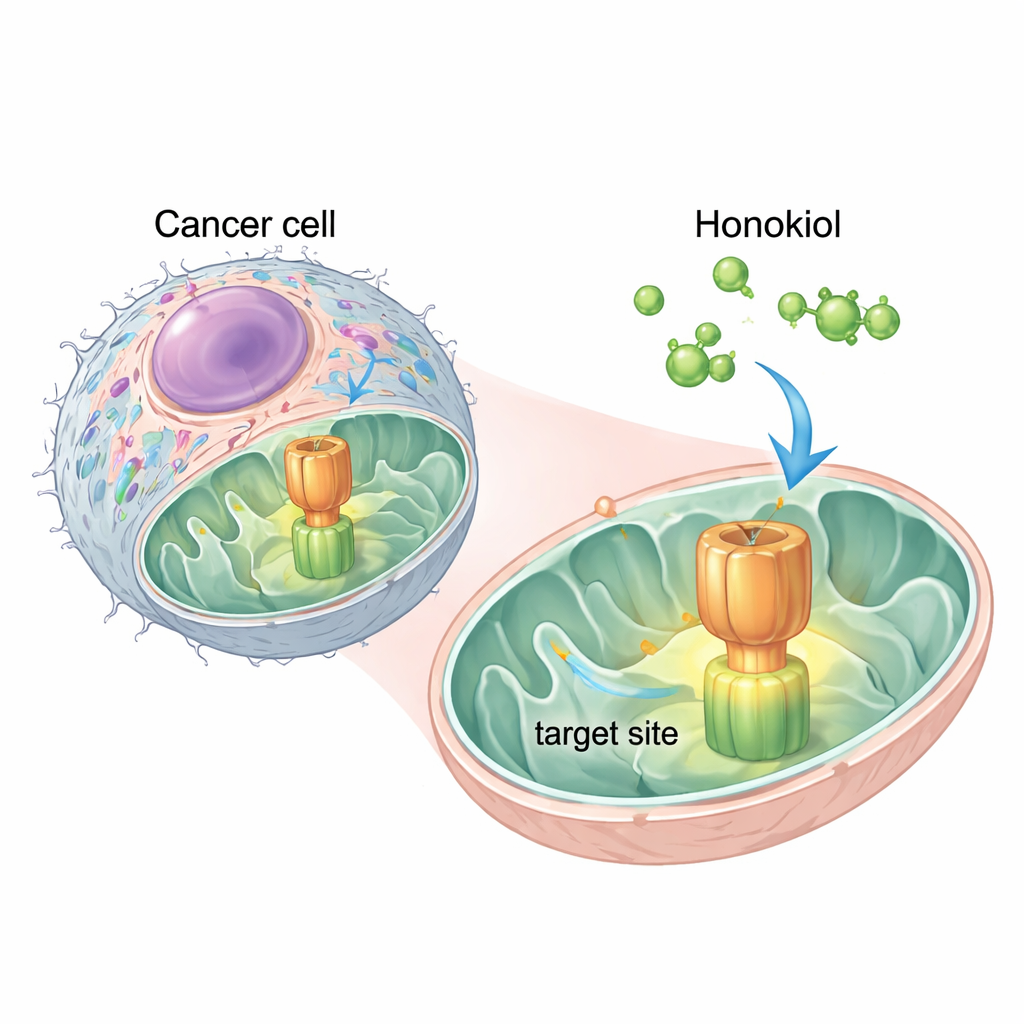
Naturalna cząsteczka trafia w krytyczny przełącznik
Naukowcy wykorzystali symulacje komputerowe, by sprawdzić, gdzie honokiol mógłby się zakotwiczyć na syntazie ATP. Znaleźli dwa obiecujące miejsca „dokowania” na jednym z jej elementów, w regionie zwanym OSCP. Najsilniejsze miejsce nakładało się z tej samej łatki, której używa IF1, by trzymać się syntazy ATP. Sugerowało to, że honokiol może działać jak molekularny klin, wsuwając się w OSCP i odpychając IF1. Eksperymenty na ludzkich komórkach raka szyjki macicy HeLa potwierdziły tę hipotezę: dodanie honokiolu zmniejszyło fizyczny kontakt między IF1 a OSCP, nie zakłócając innych części enzymu, co wskazuje na specyficzny efekt.
Z komórek do żywych zwierząt: mniej guza, mniej rozprzestrzeniania
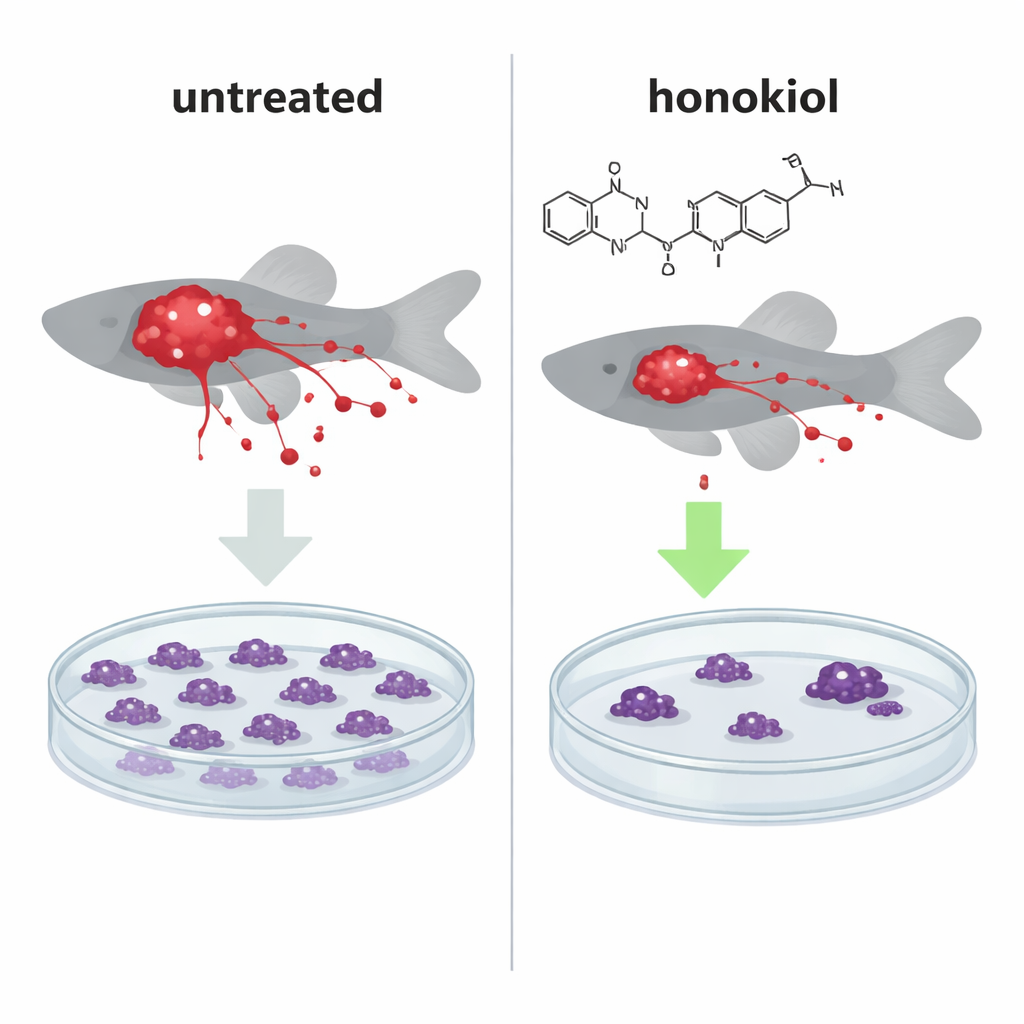
Aby sprawdzić, czy to molekularne popchnięcie ma realne konsekwencje, zespół wszczepił świecące ludzkie komórki nowotworowe do maleńkich embrionów zebrafisza, uznanego modelu całego organizmu do śledzenia wzrostu guza i przerzutów. U ryb wstrzykniętych normalnymi, bogatymi w IF1 komórkami HeLa, leczenie honokiolem znacząco zmniejszyło masy guza i ograniczyło liczbę komórek nowotworowych rozprzestrzeniających się do odległych obszarów, co przypominało obraz u ryb wstrzykniętych komórkami z wyciszeniem IF1 pozbawionymi ochronnego białka. Co ciekawe, honokiol zmniejszał też liczbę komórek przerzutowych nawet wtedy, gdy IF1 było nieobecne, co sugeruje drugi, niezależny od IF1 mechanizm ograniczania rozprzestrzeniania się raka.
Zmuszanie wadliwych elektrowni do uruchomienia mechanizmu samodestrukcji
W powrocie do prób w naczyniu, honokiol zmniejszył zdolność komórek nowotworowych do tworzenia dużych kolonii w miękkim agarze, teście imitującym stresujące, niskotlenowe warunki panujące w guzach litych. Stało się to bez istotnego spowolnienia zwykłego podziału komórek czy podstawowego oddechu mitochondrialnego, wskazując raczej na zmianę w sposobie, w jaki mitochondria decydują między życiem a śmiercią. Pomiary gospodarki wapniowej wykazały, że honokiol powodował otwieranie się poru przejścia przepuszczalności przy niższych poziomach wapnia, co jest znanym wyzwalaczem pęcznienia i uwalniania czynników promujących śmierć. Przy umiarkowanych dawkach efekt ten zależał od wypchnięcia IF1; przy wyższych dawkach honokiol działał przez drugie miejsce wiążące na OSCP i poprzez zwiększenie reaktywnych form tlenu, uczulając nawet komórki pozbawione IF1 na zaprogramowaną śmierć komórki.
Powstrzymywanie komórek nowotworowych przed migracją
Rak staje się najbardziej niebezpieczny, gdy komórki odrywają się i przemieszczają do nowych organów. W testach „zadrapaniowych” na wzór rany, honokiol silnie spowalniał zbiorową migrację arkuszy komórek nowotworowych i redukował markery przejścia epitelialno-mezenchymalnego, procesu wyposażającego komórki guza w zdolność do ruchu i inwazji. Szczegółowe obrazy mikroskopii elektronowej ujawniły, że migrujące komórki zwykle powiększają i przekształcają mitochondria, dodając wewnętrzne fałdy, aby sprostać wysokim wymaganiom energetycznym na czele ruchu. Pod wpływem honokiolu mitochondria na froncie ruchu stały się zamiast tego spuchnięte i uszkodzone strukturalnie — cechy otwarcia poru przejścia przepuszczalności — podczas gdy mitochondria w obszarach nieruchomych były mniej dotknięte lub nawet zwiększały się ich liczby, w zależności od obecności IF1.
Co to oznacza dla przyszłych terapii przeciwnowotworowych
Mówiąc krótko, praca ta pokazuje, że honokiol potrafi trafić w niewielki region regulacyjny mitochondrialnej maszyny produkującej ATP i odwrócić wbudowany wyłącznik bezpieczeństwa, który komórki nowotworowe często mają zaryglowany. Poprzez odsunięcie IF1 i bezpośrednie pchnięcie poru w stronę otwarcia, honokiol skłania komórki guza do samodestrukcji i utrudnia im migrację oraz zasiewanie przerzutów. Ponieważ efekty te wynikają z cech wspólnych dla wielu nowotworów — a nie z pojedynczego markera powierzchniowego — celowanie w region OSCP syntazy ATP może zainspirować nową klasę terapii wykorzystujących słabości „stacji energetycznych” komórek nowotworowych przy ograniczaniu szkód dla tkanek zdrowych.
Cytowanie: Grandi, M., Boldrin, F., Risato, G. et al. Honokiol blocks tumor development and metastasis through mitochondrion-targeted effects. Cell Death Dis 17, 186 (2026). https://doi.org/10.1038/s41419-026-08441-6
Słowa kluczowe: honokiol, mitochondria, syntaza ATP, apoptoza, przerzuty