Clear Sky Science · pl
Zapalenie płuc związane z inhibitorami punktów kontrolnych układu odpornościowego: aktualne postępy i przypuszczalna rola terapii komórkami macierzystymi mezenchymalnymi
Kiedy leczenie nowotworu szkodzi płucom
Leki uwalniające układ odpornościowy do walki z nowotworem zmieniły opiekę nad chorobami takimi jak rak płuca czy czerniak. Ta nowa siła ma jednak swoją cenę: u niektórych pacjentów ten sam atak immunologiczny, który niszczy guzy, zwraca się przeciw płucom, wywołując stan zwany zapaleniem płuc związanym z inhibitorami punktów kontrolnych układu odpornościowego (ICIP). Przegląd wyjaśnia, czym jest ICIP, dlaczego się pojawia, jak lekarze obecnie go leczą i dlaczego szczególny typ komórek macierzystych — mezenchymalne komórki macierzyste (MSC) — może pewnego dnia zaoferować bezpieczniejszy, bardziej precyzyjny sposób stłumienia stanu zapalnego bez rezygnacji z kontroli nowotworu. 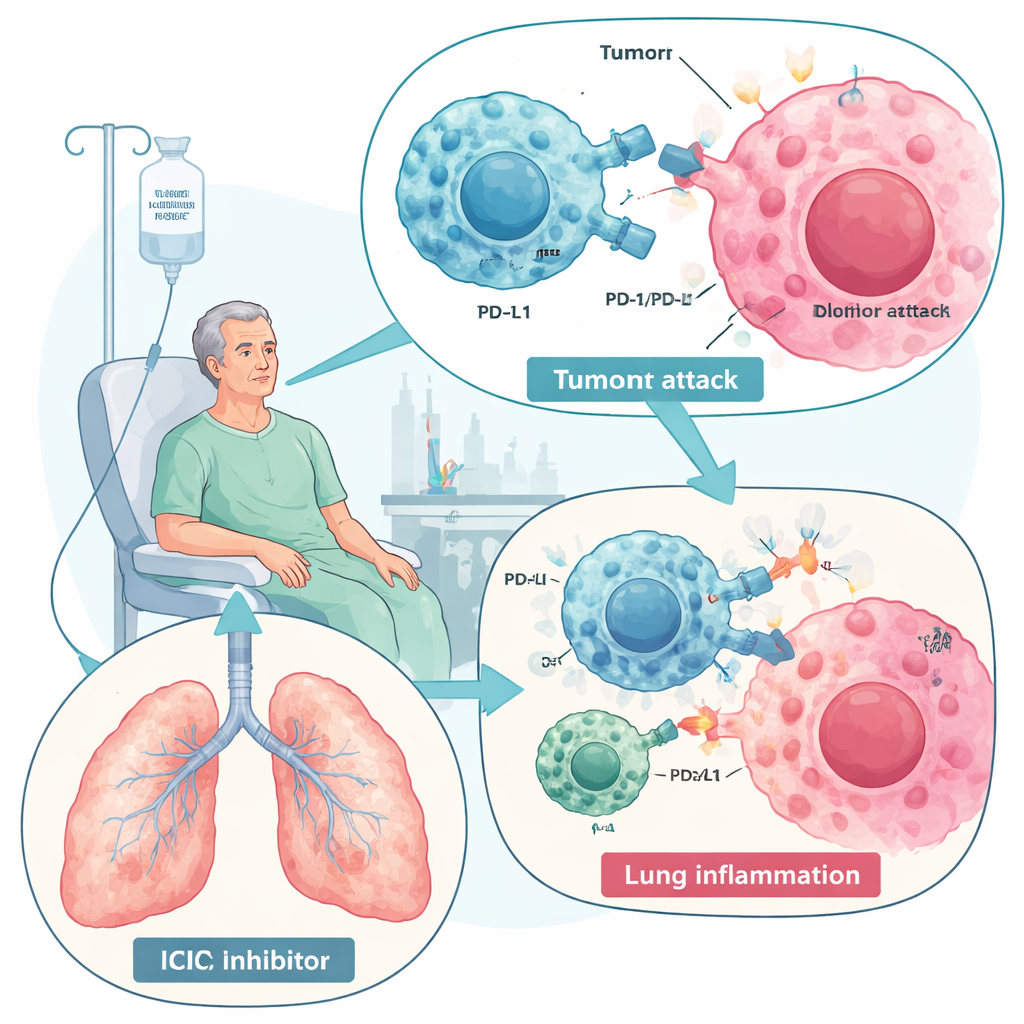
Mocne leki przeciwnowotworowe z ukrytym ryzykiem dla płuc
Inhibitory punktów kontrolnych odporności, zwłaszcza blokujące PD-1 i PD-L1, działają poprzez usunięcie molekularnych „hamulców”, które normalnie ograniczają reakcje immunologiczne. Po zdjęciu hamulców komórki T lepiej rozpoznają i niszczą komórki nowotworowe, poprawiając przeżycie w wielu typach nowotworów. Ten sam wzrost aktywności może jednak zaburzyć tolerancję i wywołać działania niepożądane związane z układem odpornościowym w różnych narządach. ICIP jest najpoważniejszym powikłaniem płucnym tych leków i jedną z wiodących przyczyn zgonów związanych z terapią immunologiczną. Występowanie w badaniach rzeczywistych waha się od kilku procent do niemal jednej trzeciej pacjentów, szczególnie u osób z rakiem płuca lub z chorobami płuc przed leczeniem, takimi jak POChP czy choroby śródmiąższowe. Objawy obejmują od łagodnego kaszlu i duszności po zagrażającą życiu niewydolność oddechową.
Jak układ odpornościowy uszkadza płuca
Przegląd opisuje ICIP jako wynik zaburzonej równowagi immunologicznej w obrębie płuc. Nadaktywne „komórki bojowe” — limfocyty CD8, niektóre podtypy limfocytów pomocniczych, zapalne makrofagi, neutrofile i komórki NK — zalewają tkankę płucną i wydzielają agresywne białka sygnałowe, w tym interferon‑gamma, TNF‑alfa oraz interleukiny takie jak IL‑6 i IL‑17. Równocześnie zmniejsza się liczba komórek ochronnych tłumiących zapalenie, jak komórki T regulatorowe i makrofagi ukierunkowane na naprawę. U niektórych pacjentów przed lub w trakcie leczenia obserwuje się też wzrost poziomu autoprzeciwciał, co sugeruje, że ICIP może częściowo przypominać chorobę autoimmunologiczną. W płynie z płuc po płukaniu stwierdza się wzorzec zapalny bogaty w komórki T i mieszaninę cytokin odmienną od zakażenia lub progresji nowotworu, co może pomóc w diagnostyce.
Obrazowanie, stopniowanie i leczenie uszkodzeń
W tomografii komputerowej ICIP najczęściej ujawnia się jako zamglone obszary typu „ground‑glass” lub plamiste przejaśnienia rozsiane w obu płucach, wzory różniące się od zmian pourazowych po radioterapii, które ograniczają się do napromienionego pola. Rozpoznanie ICIP opiera się na połączeniu zmian obrazowych, objawów oraz starannym wykluczeniu zakażenia i innych przyczyn. Wytyczne międzynarodowe stopniują nasilenie od 1 (łagodne, często tylko radiologiczne) do 4 (zagrażająca życiu niewydolność oddechowa). Głównym sposobem leczenia są obecnie glikokortykosteroidy — silne sterydy przeciwzapalne — czasami łączone z innymi lekami tłumiącymi immunologię, jak tocilizumab (blokujący IL‑6) czy infliksymab (blokujący TNF‑alfa) w ciężkich lub opornych na sterydy przypadkach. Te metody mogą ratować życie, lecz są narzędziami grubymi — sterydy niosą wiele działań niepożądanych, nie wszyscy pacjenci odpowiadają na leczenie, a szerokie tłumienie układu odpornościowego może osłabić samą przeciwzaporową odpowiedź przeciwnowotworową, którą chciano wzmocnić.
Dlaczego w dyskusji pojawiają się komórki macierzyste
Mezenchymalne komórki macierzyste, które można pozyskać ze szpiku kostnego, tkanki tłuszczowej lub tkanki pępowinowej, pojawiły się jako obiecujący „modulator immunologiczny”, a nie tylko proste budowniczowie tkanki. Po wprowadzeniu do krwiobiegu wiele z tych komórek ulega czasowemu uwięzieniu w drobnych naczyniach płucnych — tzw. efekt pierwszego przejścia — co jest wadą w leczeniu narządów odległych, lecz potencjalną zaletą w chorobach płuc. W modelach zwierzęcych i wczesnych badaniach u ludzi w schorzeniach takich jak ciężkie zapalenie płuc, ARDS, choroby zapalne jelit czy choroba przeszczep przeciw biorcy, MSC łagodzą nadmierne odpowiedzi immunologiczne, przesuwają populacje komórek odpornościowych w kierunku bardziej zrównoważonego stanu i wydzielają czynniki wzrostu sprzyjające naprawie tkanki przy ograniczaniu bliznowacenia. Co ważne, ich korzyści często wynikają nie z przekształcania się w komórki płuc, lecz z mieszaniny cząsteczek sygnałowych i drobnych pęcherzyków (egzosomów), które uwalniają. 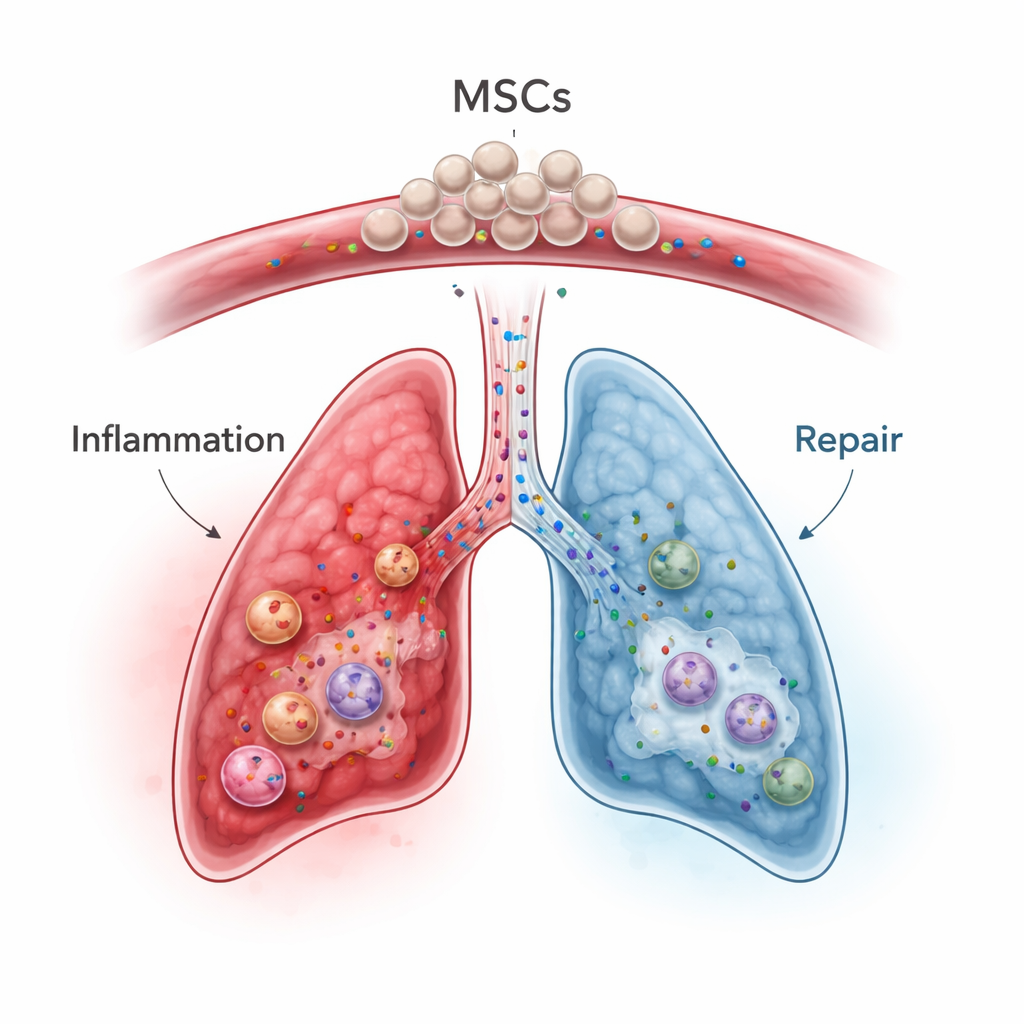
Jak MSC mogłyby uciszyć ICIP, nie burząc terapii przeciwnowotworowej
W kontekście ICIP MSC mogłyby teoretycznie rozwiązać kilka problemów jednocześnie. Mogą bezpośrednio hamować aktywowane komórki T, wspierać wzrost i funkcję komórek T regulatorowych oraz przesuwać makrofagi z agresywnego, niszczącego tkankę fenotypu ku trybowi sprzyjającemu gojeniu. Obniżają też kluczowe mediatory zapalne, takie jak IL‑6, IL‑1β i TNF‑alfa, oraz zwiększają czynniki przeciwzapalne i białka ochronne, jak TSG‑6, które pomagają ograniczać uszkodzenie płuc i włóknienie. Prace przedkliniczne sugerują, że MSC lub inżynierowane egzosomy pochodzące od MSC mogą redukować burze cytokin i uszkodzenia narządów wywołane inhibitorami punktów kontrolnych lub radioterapią, a w niektórych ustawieniach zachowywać aktywność przeciwnowotworową lepiej niż standardowe immunosupresanty. Autorzy jednak ostrzegają, że MSC mogą także wchodzić w złożone interakcje z guzami i krzepliwością krwi, a ich efekty silnie zależą od otaczającego środowiska zapalnego i źródła MSC (szpik kostny, tkanka tłuszczowa lub pępowina).
Perspektywy: obietnica wymagająca ostrożnego testowania
Dla pacjentów, u których leczenie nowotworu jest przerwane lub zagrożone przez ciężką toksyczność płucną, terapie oparte na MSC mogłyby w przyszłości zapewnić bardziej ukierunkowany sposób schładzania zapalenia, naprawy tkanki płucnej i zapobiegania długotrwałemu włóknieniu — najlepiej bez unieważniania ratujących życie korzyści immunoterapii. Jednak dotąd nie zakończono badań klinicznych specyficznych dla ICIP z użyciem MSC. Autorzy argumentują, że pilnie potrzebne są starannie zaprojektowane badania na zwierzętach i próby kliniczne, aby określić, który typ MSC lub produkt z egzosomów działa najlepiej, jakie dawki stosować, kiedy podawać je względem steroidów i immunoterapii oraz jak monitorować ryzyka, takie jak wzrost guza czy zakrzepica. Do tego czasu MSC pozostają obiecującą, lecz wciąż eksperymentalną opcją na horyzoncie w zarządzaniu tym poważnym skutkiem ubocznym nowoczesnej opieki onkologicznej.
Cytowanie: Li, Z., Zheng, X., Xia, H. et al. Immune checkpoint inhibitor-related pneumonitis: current advances and the putative role of mesenchymal stem cell therapy. Cell Death Dis 17, 200 (2026). https://doi.org/10.1038/s41419-026-08440-7
Słowa kluczowe: skutki uboczne immunoterapii, zapalenie płuc, inhibitory punktów kontrolnych, mezenchymalne komórki macierzyste, zapalenie płuc