Clear Sky Science · pl
c-Myc/GRPEL1 utrzymuje syntezę kwasów tłuszczowych przez FASN, wspierając proliferację komórek PDAC
Dlaczego zachcianki tłuszczowe komórek nowotworowych mają znaczenie
Rak trzustki jest jednym z najbardziej śmiertelnych nowotworów, częściowo dlatego, że jego komórki świetnie przestawiają własny metabolizm, by przetrwać i rosnąć. W badaniu przyjrzano się zaskakującemu aspektowi tej historii: w jaki sposób komórki guzów trzustki nasilają wewnętrzne „tłuszczowe fabryki”, by zasilać nieustanny wzrost, i jak zablokowanie tego procesu może otworzyć nowe opcje terapeutyczne dla pacjentów.
Trudny przeciwnik z metaboliczną przewagą
Większość raków trzustki należy do typu gruczolakoraka przewodowego trzustki (PDAC), który zwykle wykrywany jest późno i słabo reaguje na dostępne terapie. Komórki PDAC żyją w surowym środowisku o niskiej zawartości tlenu i ograniczonych składnikach odżywczych, a mimo to radzą sobie, przepinając sposoby wykorzystania cukrów, tłuszczów i innych paliw. Ich mitochondria — maleńkie elektrownie w komórkach — odgrywają centralną rolę w tej przebudowie. Aby utrzymać te „elektrownie” w ruchu, komórki nieustannie kontrolują i naprawiają tysiące mitochondrialnych białek w procesie zwanym jakość kontroli białek mitochondrialnych. Dotąd nie było jasne, jak ta machina kontroli jakości łączy się ze sposobem, w jaki guzy trzustki pozyskują paliwo.
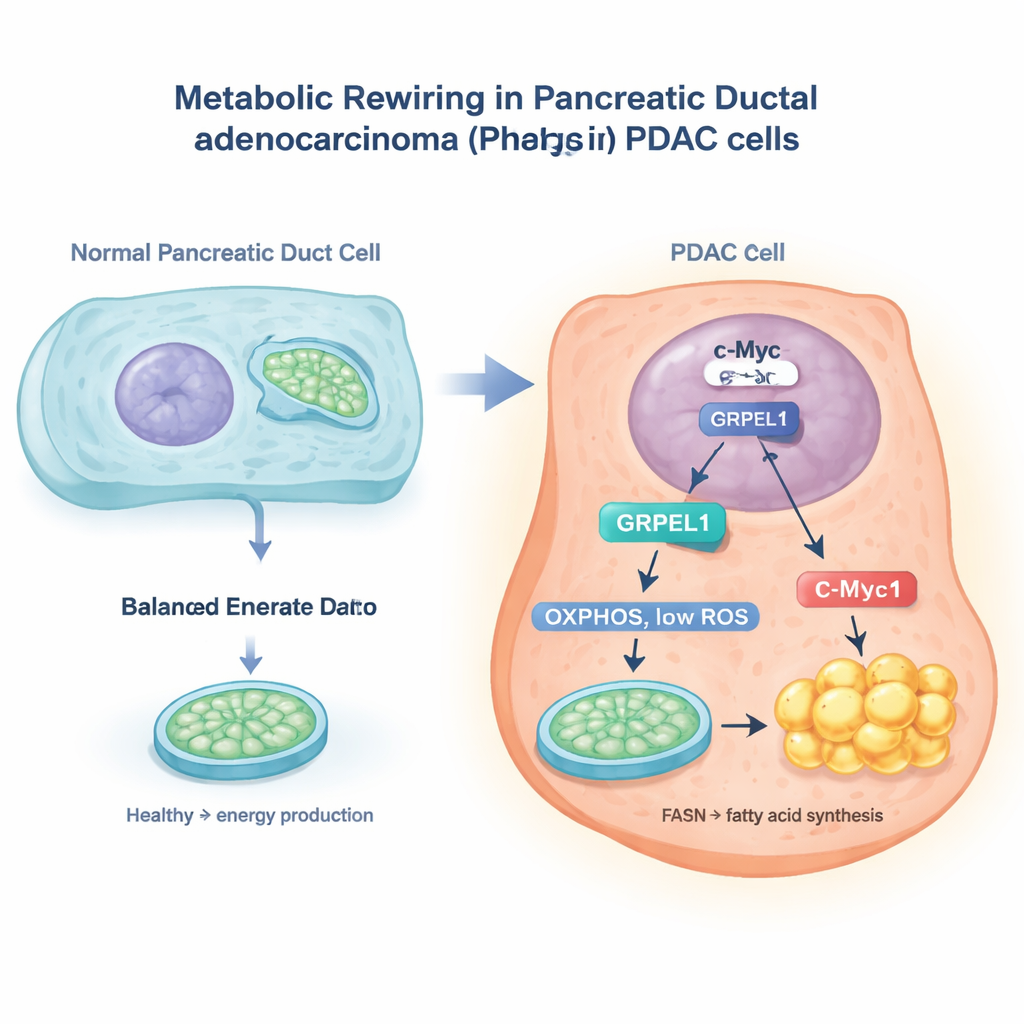
Przełącznik c-Myc i pomocnik mitochondrialny
Naukowcy wykorzystali obszerne bazy danych dotyczące nowotworów oraz eksperymenty na komórkach raka trzustki, aby skupić się na białku nazwanym GRPEL1, pomocniku zaangażowanym w obsługę białek mitochondrialnych. Odkryli, że dobrze znany gen nowotworowy c-Myc działa jak molekularny przełącznik w jądrze komórkowym, który włącza gen GRPEL1. Gdy poziomy c-Myc były obniżone, spadały też poziomy GRPEL1; gdy c-Myc był podwyższony, GRPEL1 rosło. Próbki guzów pacjentów wykazywały również, że c-Myc i GRPEL1 często występują razem na wysokim poziomie, a oba korelowały z gorszym rokowaniem. W hodowlach komórkowych PDAC obniżenie GRPEL1 spowalniało podziały komórek i wzrost kolonii, podczas gdy dodanie dodatkowego GRPEL1 przyspieszało proliferację, zwłaszcza gdy c-Myc był zablokowany.
Z mitochondriów do produkcji tłuszczu
Bliższe analizy wykazały, że GRPEL1 robi więcej niż tylko dba o porządek białek w mitochondriach. Przy deplecji GRPEL1 mitochondria w komórkach PDAC były mniej wydajne w produkcji energii, traciły normalną morfologię i uwalniały więcej reaktywnych form tlenu (ROS) — reaktywnych chemicznie produktów ubocznych nazywanych czasem „rdzą” komórkową. Ten wzrost ROS miał skutek pośredni: obniżał poziom syntazy kwasów tłuszczowych (FASN), kluczowego enzymu budującego nowe kwasy tłuszczowe wewnątrz komórek. Przy obniżonym poziomie FASN komórki wytwarzały mniej tłuszczów, magazynowały mniej lipidów i ich wzrost zwalniał. Gdy badacze zneutralizowali ROS za pomocą przeciwutleniacza, poziomy FASN wracały do normy, co pokazało, że związek GRPEL1–FASN jest napędzany przez ROS. Co ciekawe, samo c-Myc nie wydawało się bezpośrednio włączać genu FASN w tym układzie, lecz wpływało na FASN pośrednio przez GRPEL1 i stres mitochondrialny.
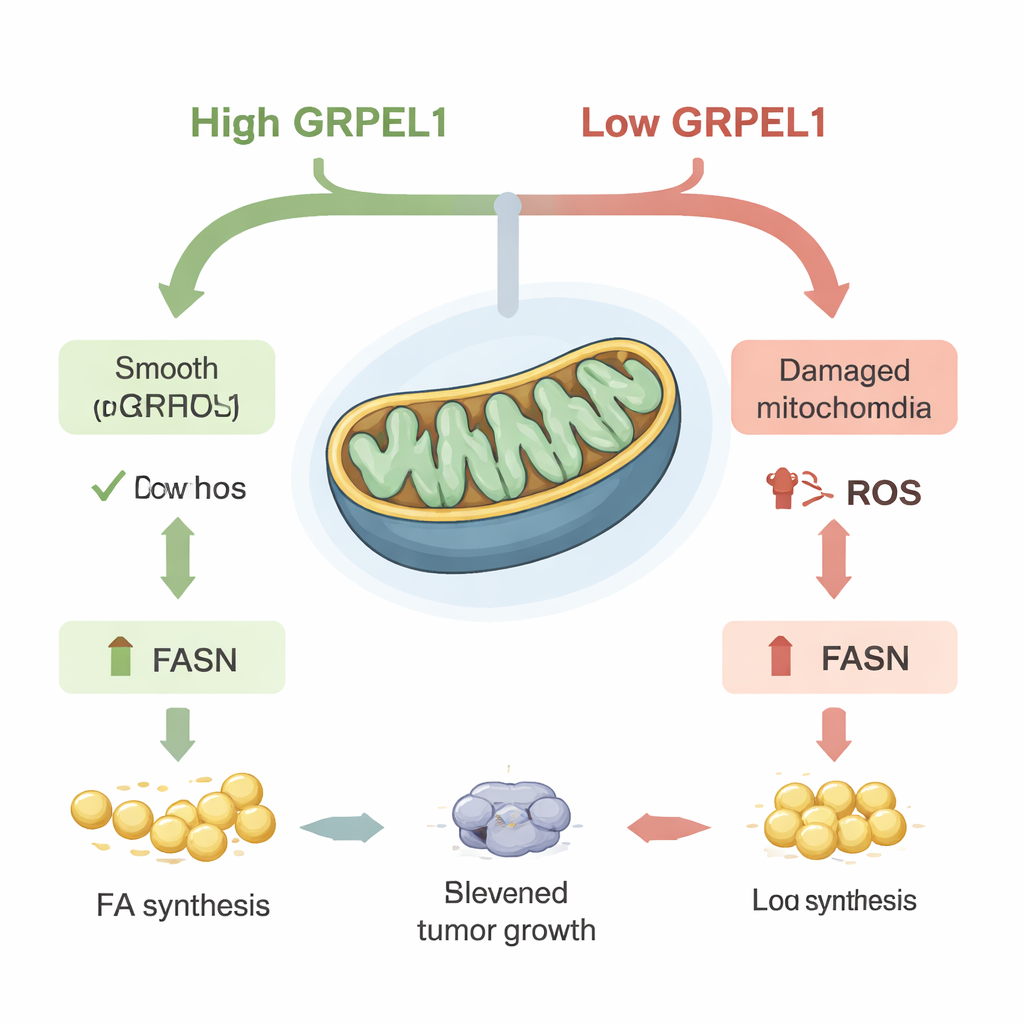
Tłuszcz jako paliwo wzrostu guza
Ponieważ FASN leży w centrum budowy tłuszczów, naukowcy sprawdzili, czy przywrócenie jego aktywności może uratować wzrost komórek nowotworowych przy niskim GRPEL1. W hodowlach komórkowych wymuszone zwiększenie FASN częściowo odwracało spowolnienie wzrostu i formowanie kolonii spowodowane utratą GRPEL1. To samo zaobserwowano u myszy: guzy utworzone z komórek o obniżonym GRPEL1 rosły wolniej, ale ponowne wprowadzenie FASN przywracało zarówno rozmiar guza, jak i zawartość tłuszczu. Szczegółowe analizy metabolitów i lipidów wykazały szerokie spadki wielu związków związanych z tłuszczami przy zmniejszeniu GRPEL1 lub c-Myc. Co ważne, dostarczenie zewnętrznych kwasów tłuszczowych lub mieszanki lipidowej częściowo przywracało wzrost zarówno w liniach komórkowych nowotworu, jak i w organoidach trzustkowego raka pochodzących od pacjentów — miniaturowych guzach hodowanych w 3D — sugerując, że głównym problemem była utrata endogennej syntezy tłuszczów.
Przekształcenie słabości w terapię
W sumie praca układa klarowny obraz: w raku trzustki c-Myc podnosi poziom GRPEL1, co pomaga mitochondriom funkcjonować sprawnie i utrzymuje ROS na niskim poziomie. To spokojne środowisko mitochondrialne pozwala komórkom utrzymać wysokie poziomy FASN, produkując nowe kwasy tłuszczowe, które służą jako składniki błon, magazyn energii i sygnały wzrostu. Gdy GRPEL1 jest zablokowany, mitochondria zawodzą, ROS wzrasta, FASN spada, a komórki nowotworowe mają trudności z proliferacją — efekt, który można częściowo obejść przez zewnętrzne dostarczenie tłuszczów. Dla czytelników nieposługujących się terminologią naukową wniosek jest taki, że guzy trzustki polegają na wewnętrznym obwodzie „fabryki tłuszczu” napędzanym przez c-Myc, GRPEL1 i FASN. Leki zaburzające tę oś syntezy kwasów tłuszczowych, szczególnie w guzach, gdzie jest ona silnie aktywna, mogą stanowić obiecujący sposób na „zagłodzenie” komórek raka trzustki przy relatywnie mniejszym wpływie na tkanki prawidłowe.
Cytowanie: Wang, J., Zhang, L., Chen, K. et al. c-Myc/GRPEL1 maintains fatty acid synthesis via FASN to support PDAC cell proliferation. Cell Death Dis 17, 205 (2026). https://doi.org/10.1038/s41419-026-08439-0
Słowa kluczowe: rak trzustki, metabolizm nowotworu, synteza kwasów tłuszczowych, mitochondria, c-Myc